Clear Sky Science · it
Modelli di deep learning interpretabili e generativi chiariscono i motivi intrinsecamente disordinati che separano le fasi
Perché contano i segmenti proteici minuscoli
All'interno di ciascuna delle nostre cellule, molecole vitali spesso si radunano in ammassi simili a gocce chiamati condensati biomolecolari. Queste gocce aiutano a organizzare la chimica senza le pareti di una membrana, influenzando come i geni vengono attivati, come i segnali vengono trasmessi e come le cellule rispondono allo stress. Molti di questi condensati sono formati da tratti flessibili delle proteine noti come regioni intrinsecamente disordinate. Tuttavia i biologi faticano ancora a individuare i brevi pezzi di sequenza che effettivamente determinano la formazione di queste gocce. Questo studio presenta un framework di deep learning, PhaSeMotif, in grado sia di trovare questi segmenti chiave sia di progettarne di nuovi, offrendo ai ricercatori un nuovo e potente strumento per sondare e rimodulare i condensati cellulari.
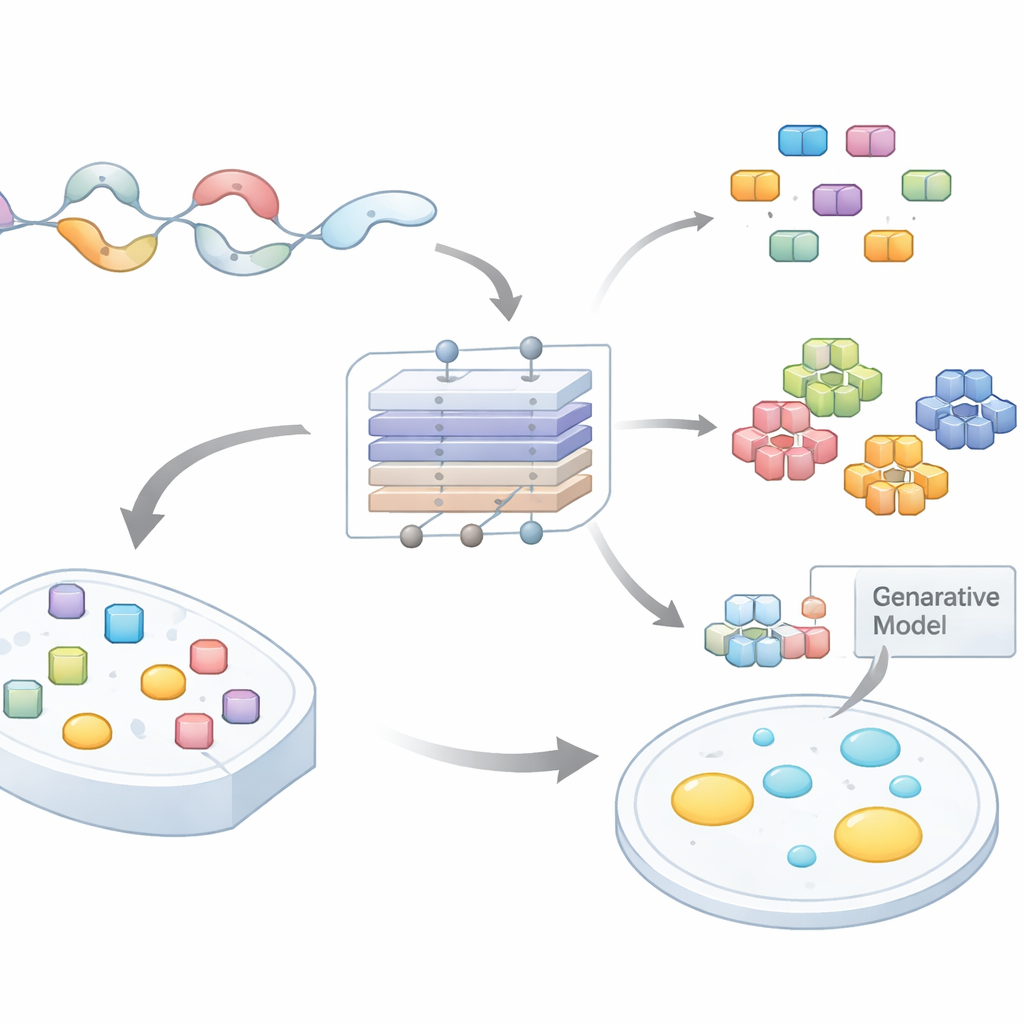
Dai code proteiche disordinate a ipotesi testabili
Molte proteine contengono lunghe code flessibili che non si ripiegano in forme fisse. Queste regioni disordinate sono arricchite in alcuni amminoacidi e spesso contengono motivi ripetuti o brevi sequenze ricorrenti. Un numero crescente di lavori mostra che tali motivi promuovono la condensazione consentendo numerose interazioni deboli simultanee. Tuttavia scandire interi proteomi per trovare quali brevi tratti siano importanti e perché è stato un grande collo di bottiglia. Gli strumenti computazionali esistenti di solito valutano proteine complete o grandi regioni, offrendo scarsa indicazione su dove mutare o cosa testare in laboratorio. Gli autori si sono posti l'obiettivo di costruire un modello che predicesse non solo se una regione disordinata possa formare gocce, ma anche quali esatte sottosequenze svolgono il lavoro principale.
Una mappa deep learning dei motivi che guidano le gocce
Il team ha compilato ampi set di dati di regioni disordinate in diverse specie e le ha etichettate in base alla probabilità che le proteine ospitanti subissero separazione di fase. Hanno quindi addestrato una rete neurale basata sull'attenzione, PhaSeMotif, che prende in input una sequenza di amminoacidi di qualsiasi lunghezza e restituisce un punteggio di formazione di gocce. Crucialmente, la rete usa una combinazione di strati convoluzionali e meccanismi di attenzione per valutare quanto ogni finestra corta della sequenza contribuisca a quel punteggio. Tracciando a ritroso attraverso il modello (con tecniche analoghe alla backpropagation guidata), gli autori hanno estratto patch di alta importanza—brevi motivi spesso di meno di 20 residui—che il modello ha ritenuto essenziali per la formazione di gocce.
Mettere le predizioni alla prova nelle cellule vive
Per verificare se questi motivi fossero davvero importanti, i ricercatori hanno utilizzato un sistema attivabile dalla luce nelle cellule umane. Hanno fuso le regioni disordinate previste come capaci di formare gocce a un modulo di oligomerizzazione sensibile alla luce e a un marcatore fluorescente. Sotto luce blu, questi costrutti condensavano rapidamente in puntini luminosi, segnalando la separazione di fase in tempo reale. Il team ha poi rimosso chirurgicamente singoli motivi sostituendoli con linker neutrali e flessibili della stessa lunghezza. Nell'82% delle 17 sequenze alterate testate, la formazione di gocce è risultata drasticamente ridotta o scomparsa del tutto, mentre mutazioni di controllo al di fuori dei segmenti identificati da PhaSeMotif spesso avevano scarso effetto. È importante che molti di questi motivi chiave sovrapponessero siti in cui mutazioni associate a malattie sono note per perturbare la condensazione, sottolineandone la rilevanza biologica.
Scoprire un vocabolario di tipi di motivo
Con più di 17.000 motivi a disposizione, gli autori si sono poi chiesti se esistessero “sapore” comuni tra i segmenti che guidano le gocce. Hanno analizzato composizione e patterning degli amminoacidi, quindi hanno raggruppato i motivi in nove cluster. Alcuni cluster risultavano ricchi di residui aromatici e glicina, coerenti con interazioni π–π appiccicose e interazioni catione–π. Altri contenevano patch separate di cariche positive e negative, favorendo attrazione elettrostatica e partizionamento selettivo in condensati particolari. Ulteriori cluster erano dominati da prolina e glicina, che favoriscono la flessibilità, o da lunghe tratti di glutamina che possono formare reti dense di legami a idrogeno. Differenti compartimenti cellulari e tipi di condensato presentavano miscele caratteristiche di queste classi di motivi, suggerendo che la composizione dei motivi aiuti a determinare dove e con quali partner una proteina si condenserà.
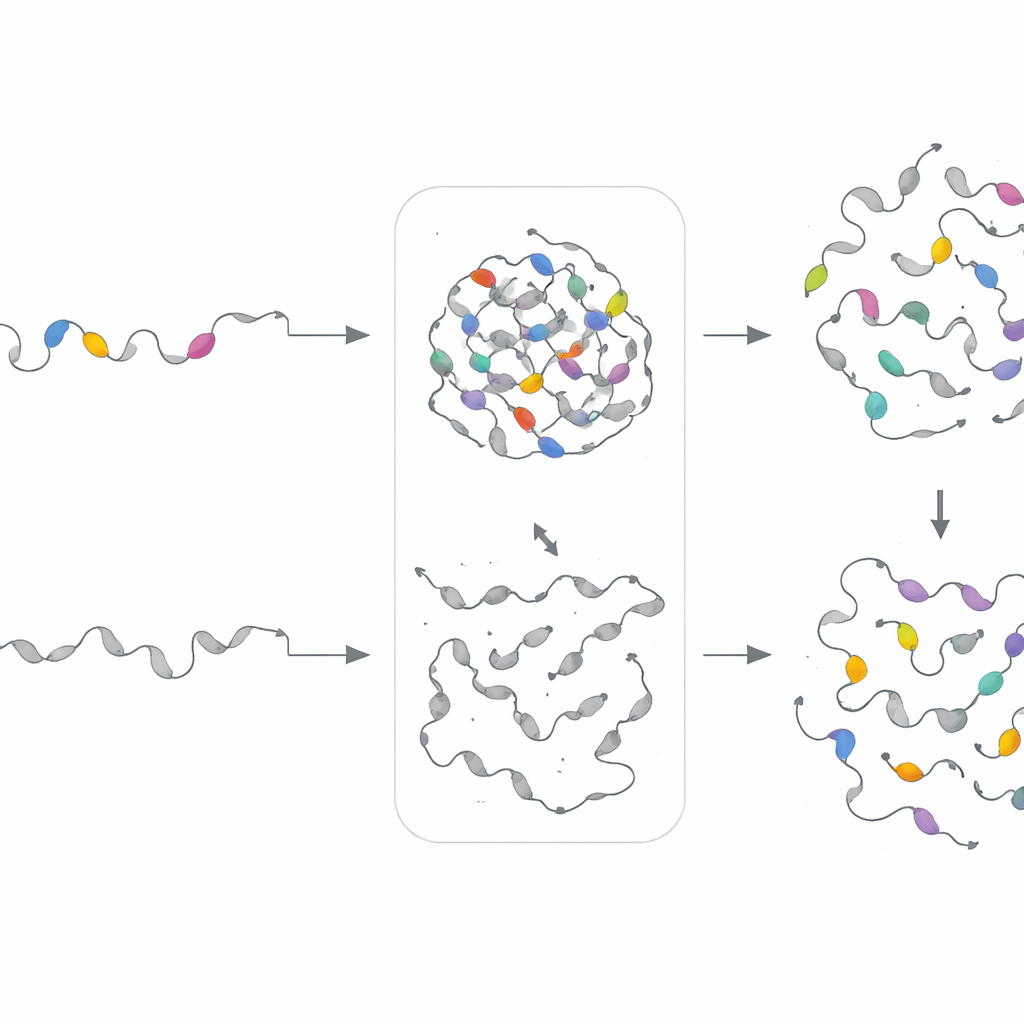
Progettare nuovi motivi per dimostrare le regole
Per verificare se le “ricette” di motivo—piuttosto che le sequenze esatte—governino il comportamento delle gocce, il team ha costruito modelli generativi separati per ciascun cluster di motivi. Questi autoencoder variazionali hanno appreso i pattern statistici di un dato cluster e poi prodotto nuove sequenze artificiali che condividono le stesse impronte composizionali ma con ordine diverso. I ricercatori hanno sperimentalmente sostituito questi motivi sintetici in proteine dove i segmenti originali erano stati eliminati. Sorprendentemente, in 18 dei 21 casi i motivi ingegnerizzati hanno ripristinato la separazione di fase nelle cellule, talvolta regolando anche la velocità o la densità della formazione delle gocce. Ciò dimostra che PhaSeMotif cattura regole di progettazione sottostanti che possono essere riutilizzate per costruire o riparare regioni capaci di formare gocce.
Cosa significa per la biologia e le malattie
Collegando deep learning interpretabile con progettazione generativa e test cellulari diretti, questo lavoro trasforma la vaga nozione di “regioni disordinate che formano gocce” in un insieme concreto di brevi motivi componibili. Per il pubblico non specialista, la conclusione è che gli scienziati possono ora leggere e scrivere i minuscoli segmenti proteici che controllano come i condensati cellulari si assemblano, si mescolano e si guastano. Questo apre la strada a una scoperta più rapida di mutazioni che causano malattie in questi segmenti, a studi meccanicistici più chiari su come i condensati organizzano la fisiologia cellulare e, in ultima analisi, all’ingegneria razionale di proteine che dirigano i condensati per applicazioni terapeutiche o di biologia sintetica.
Citazione: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Parole chiave: condensati biomolecolari, proteine intrinsecamente disordinate, separazione di fase, deep learning, motivi proteici