Clear Sky Science · it
Gli epatociti riprogrammati funzionalmente da cellule di cancro colorettale con KIAA1199 elevato favoriscono l’accumulo di neutrofili Egr1+ pro‑metastatici
Quando il cancro del colon prende di mira il fegato
La maggior parte delle persone immagina la diffusione del cancro come cellule fuori controllo che semplicemente si staccano e raggiungono nuovi organi. Questo studio racconta una storia più inquietante: i tumori colorettali possono silenziosamente riprogettare il fegato molto prima che qualsiasi cellula cancerosa arrivi, preparando un “terreno” accogliente in cui i futuri tumori possono attecchire facilmente. Capire questa fase nascosta di preparazione potrebbe aprire la strada a trattamenti che impediscano le metastasi epatiche — la principale causa di morte nel cancro colorettale — prima ancora che comincino.
Un allestimento furtivo prima dell’arrivo dei tumori
Il cancro colorettale si diffonde spesso al fegato, ma solo alcuni tumori lo fanno in modo aggressivo. Gli autori si sono concentrati su una molecola chiamata KIAA1199, abbondante nei tumori colorettali ad alto rischio. Nei modelli murini e nei campioni di pazienti, i tumori con alti livelli di KIAA1199 non solo crescevano più rapidamente; primavano anche il fegato a diventare una “nicchia pre‑metastatica”, un microambiente particolarmente favorevole alle cellule tumorali in arrivo. Anche quando le metastasi epatiche venivano impiantate sperimentalmente da una fonte separata, gli animali portatori di tumori del colon con KIAA1199 elevato sviluppavano molte più metastasi epatiche e morivano prima. Questo dimostrava che segnali provenienti dal tumore primario, non solo cellule tumorali vaganti, rimodellavano il fegato in anticipo.
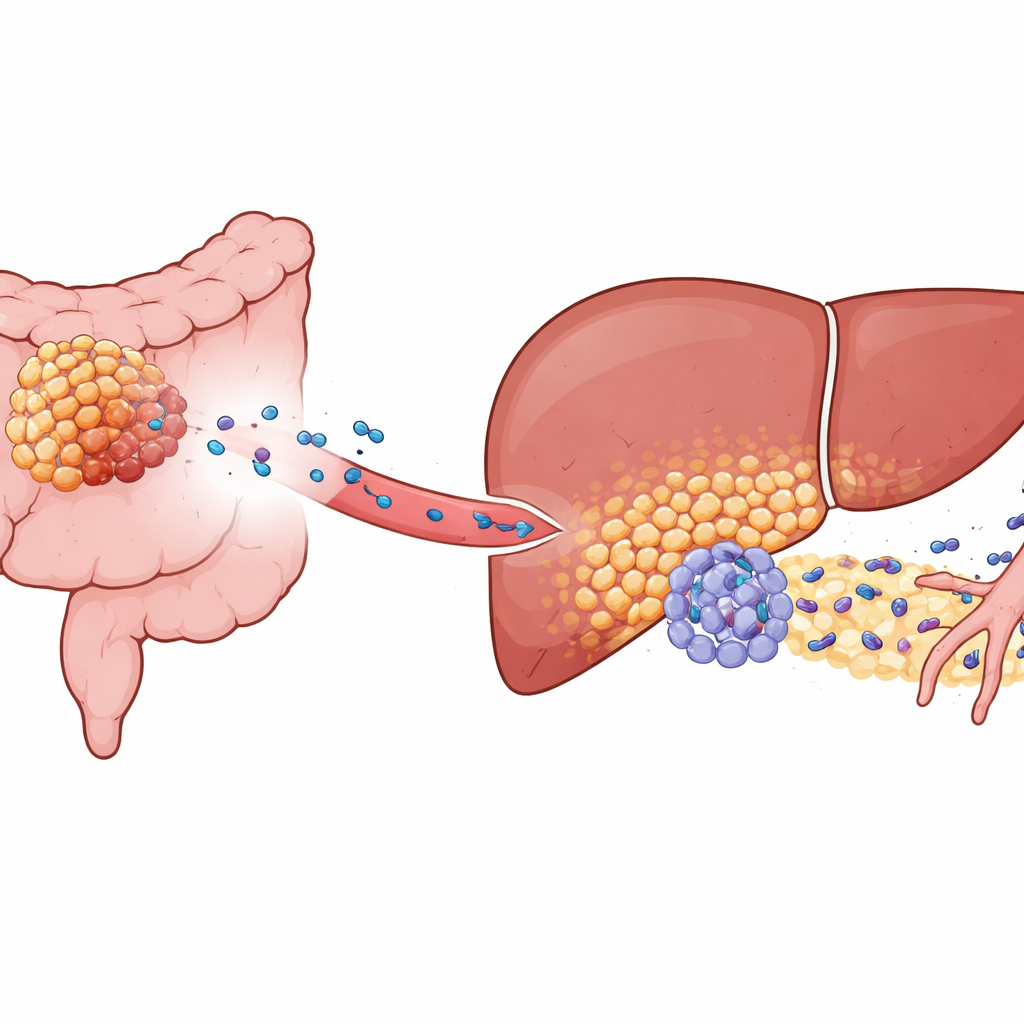
Cellule epatiche riprogrammate in aiuti del tumore
Approfondendo, i ricercatori hanno usato il sequenziamento a singola cellula e il mappaggio spaziale per esaminare il tessuto epatico ad alta risoluzione. Hanno scoperto un sottogruppo distinto di epatociti — normalmente le cellule lavoratrici del fegato — che erano stati “riprogrammati funzionalmente”. Queste cellule comparivano solo in presenza di tumori con alto KIAA1199. Invece di occuparsi discretamente del metabolismo, gli epatociti alterati passavano a uno stile metabolico più simile a quello maligno e riducevano l’attività di un regolatore protettivo chiamato PPARγ, che di norma contribuisce a contenere infiammazione e risposte allo stress. Con PPARγ represso, questi epatociti cominciavano a produrre alti livelli di una proteina chiamata SAA2, che veniva rilasciata nell’ambiente circostante, in particolare al confine dove il tessuto epatico incontra le cellule tumorali invasive.
Trasformare difensori ordinari in neutrofili pro‑metastatici
I neutrofili — globuli bianchi noti per combattere le infezioni — si comportavano anch’essi in modo anomalo in questo fegato primed. Gli autori hanno individuato un sottotipo speciale con una firma “Egr1+”, chiamata così per un fattore di trascrizione che rimodella il funzionamento di queste cellule. Piuttosto che arrivare dal flusso sanguigno già alterati, i neutrofili sembravano essere ri‑educati localmente dagli epatociti riprogrammati. La SAA2 rilasciata dagli epatociti si legava a un recettore chiamato FPR2 sui neutrofili vicini, attivando un circuito di segnalazione interno PI3K‑AKT che stabilizzava l’attività di Egr1. Il risultato era un neutrofilo più longevo e altamente attivo che secernava grandi quantità di VEGFA, un potente promotore della crescita dei nuovi vasi sanguigni. Questi neutrofili Egr1+ si concentravano all’interfaccia tumore‑fegato, esattamente dove spuntavano nuovi e fragili vasi.
Costruire vasi sanguigni che accolgono le cellule tumorali
Lo studio mostra che questi neutrofili ri‑educati non sono spettatori: rimodellano attivamente la vascolarizzazione del fegato. In colture cellulari, i fattori rilasciati dai neutrofili Egr1+ inducevano le cellule endoteliali a proliferare, migrare e formare strutture tubolari simili a nuovi vasi. Nei topi, l’aggiunta di neutrofili Egr1+ aumentava le metastasi epatiche e accelerava la morte. Bloccare passaggi chiave della catena — sia il segnale SAA2–FPR2 ai neutrofili sia la via PI3K‑AKT a valle — interrompeva la sopravvivenza dei neutrofili e la produzione di VEGFA, riducendo la crescita vascolare e la diffusione metastatica. Allo stesso modo, ripristinare l’attività di PPARγ negli epatociti con il farmaco per il diabete rosiglitazone abbassava i livelli di SAA2, frenava l’emergere dei neutrofili Egr1+ e riduceva nettamente le metastasi epatiche nei modelli preclinici.
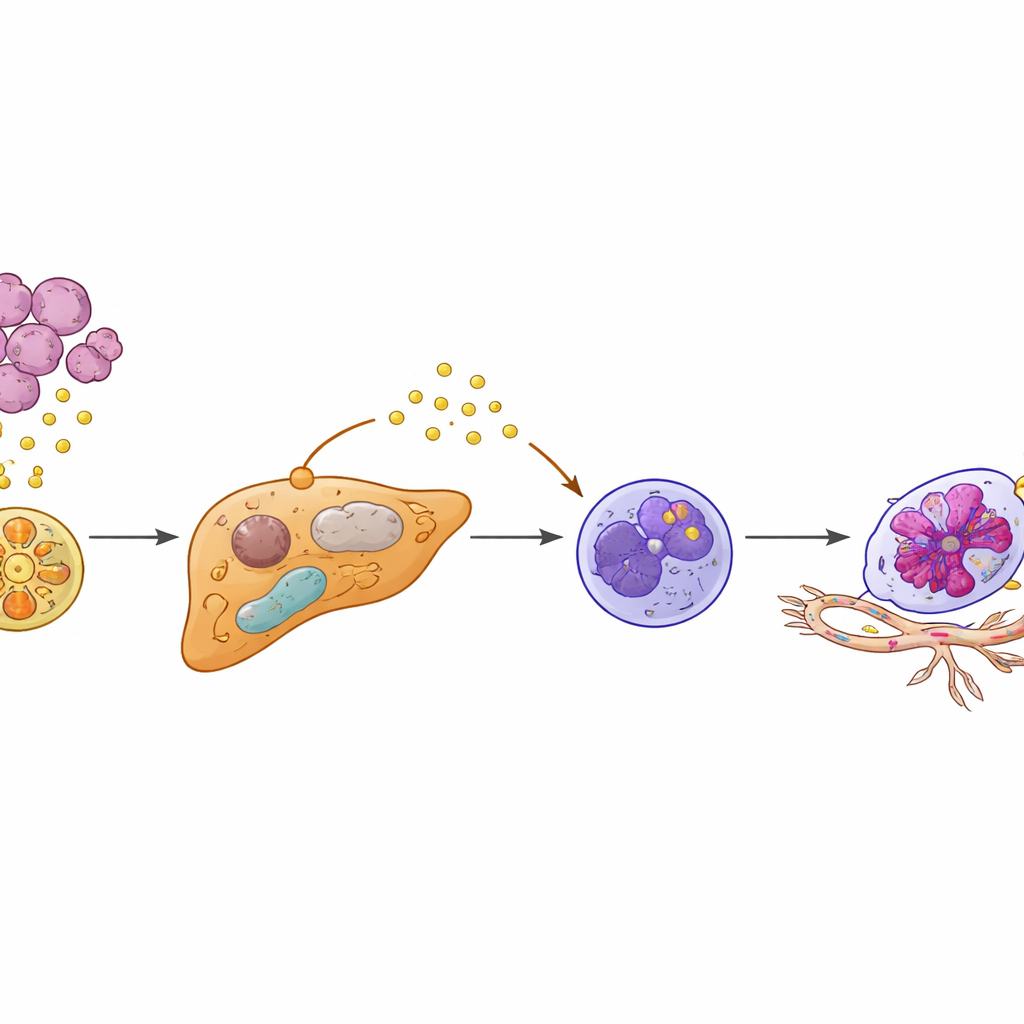
Dal meccanismo alla previsione e alla prevenzione
Poiché KIAA1199 nei tumori e SAA2 nel fegato occupano una posizione di rilievo in questa cascata, gli autori hanno verificato se queste proteine potessero aiutare a identificare i pazienti ad alto rischio di metastasi epatiche. In diverse coorti di pazienti, le persone con livelli ematici elevati di entrambi i markers avevano una probabilità molto più alta di sviluppare metastasi al fegato e di farlo più rapidamente. Un semplice punteggio combinato KIAA1199–SAA2 ha superato ciascun marker preso singolarmente nella predizione del rischio ed è stato incorporato in un «nomogramma» clinico che stima la probabilità individuale di diffusione epatica nei successivi due anni. Nel complesso, i risultati delineano un quadro vivido: i tumori del colon con KIAA1199 elevato inviano segnali veicolati da vescicole che riprogrammano gli epatociti, i quali a loro volta convertono i neutrofili vicini in complici longevi e promotori di neo‑vascolarizzazione. Mirando a questo asse KIAA1199–PPARγ/SAA2–Egr1 — con farmaci metabolici, agenti che modulano il sistema immunitario, o entrambi — potrebbe essere possibile non solo trattare le metastasi epatiche esistenti, ma prevenirne l’insediamento fin dall’inizio.
Citazione: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Parole chiave: metastasi epatiche del cancro colorettale, nicchia pre‑metastatica, neutrofili, riprogrammazione degli epatociti, microambiente tumorale