Clear Sky Science · it
Ridurre la metilazione della lisina 4 dell'istone 3.3 nell'eminenza gangliare mediale e nell'ipotalamo ricapitola i fenotipi dei disturbi neuroevolutivi
Come piccole etichette chimiche modellano cervello e corpo
Perché alcune alterazioni genetiche provocano sia difficoltà di apprendimento sia crescita insolita, come una bassa statura nell'infanzia seguita da obesità nell'età adulta? Questo studio esamina piccole etichette chimiche sulle proteine che impacchettano il DNA nel cervello e mostra come disturbare queste etichette in soltanto due aree chiave possa propagare effetti che portano a crisi epilettiche, comportamenti simili all'ansia, problemi di memoria e cambiamenti drammatici nella dimensione corporea nei topi.
Interruttori sulle manopole del genoma
All'interno di ogni cellula cerebrale, il DNA è avvolto attorno a proteine a forma di bobina chiamate istoni. Marche chimiche poste su questi istoni funzionano come manopole dimmer, aumentando o diminuendo l'espressione di gruppi di geni. Una di queste marche, aggiunta in un sito chiamato H3K4, è fortemente associata all'attivazione genica. Studi genetici umani hanno rivelato che persone nate con difetti negli enzimi che aggiungono o rimuovono questa marca spesso presentano disturbi neuroevolutivi che combinano disabilità intellettiva, epilessia e crescita corporea anomala. Tuttavia, non era chiaro quali cellule cerebrali fossero più sensibili a questa perturbazione e come il loro malfunzionamento potesse collegare l'eccitabilità cerebrale al metabolismo dell'intero organismo.
Colpire due hub cerebrali critici
I ricercatori hanno creato topi in cui una versione mutante di una proteina istonica (H3.3K4M) veniva attivata solo nelle cellule originate da due regioni cerebrali embrionali: l'eminenza gangliare mediale, che produce molte delle cellule inibitorie «freno» del cervello, e l'ipotalamo in sviluppo, che regola appetito, ormoni e bilancio energetico. Questa mutazione blocca specificamente la metilazione di H3K4 senza eliminare gli istoni stessi. I test hanno confermato che la proteina mutante era ampiamente presente nelle aree bersaglio e che i normali segni di H3K4 erano fortemente ridotti lì, mentre i livelli complessivi di istoni restavano stabili. Questo disegno sperimentale imita molte condizioni umane in cui è difettosa solo una copia di un gene correlato a H3K4, piuttosto che la sua completa assenza.
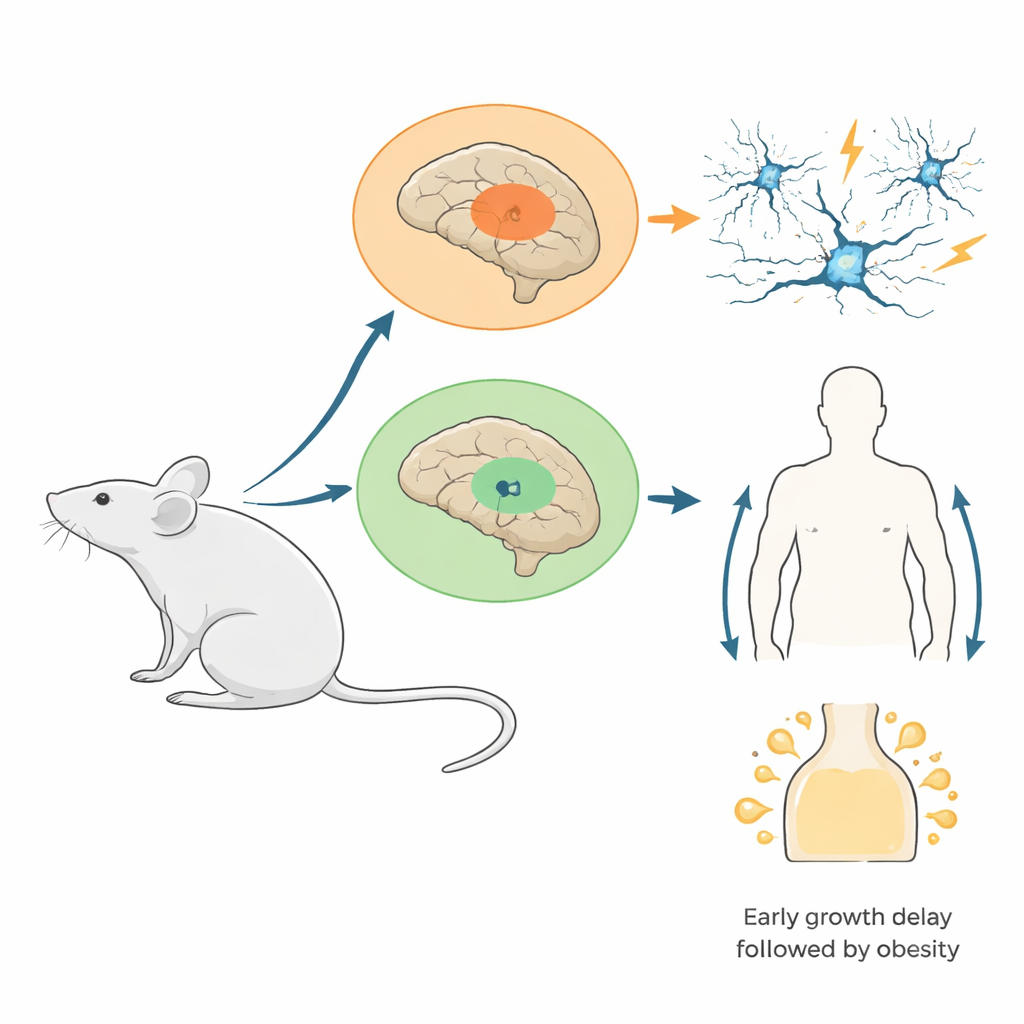
Dalla perdita delle cellule freno a circuiti proclivi alle crisi
Con la crescita di questi topi, le conseguenze sui circuiti cerebrali sono diventate evidenti. I giovani mutanti avevano meno interneuroni inibitori nella corteccia e nell'ippocampo, in particolare un tipo a scarica rapida che normalmente mantiene i ritmi neurali strettamente temporizzati. Registrazioni dettagliate hanno mostrato che gli interneuroni rimanenti erano presenti ma più variabili nelle loro proprietà elettriche, suggerendo un'alterata maturazione. Quando l'ippocampo veniva stimolato in fette cerebrali, le abituali oscillazioni ad alta frequenza «gamma» — ritmi elettrici legati all'elaborazione dell'informazione — erano più deboli e più lente, e comparivano eventi anomali a gruppi. Negli animali vivi, molti mutanti, in particolare le femmine, hanno sviluppato crisi spontanee ed erano molto più sensibili a crisi indotte da farmaci. Nelle fasi precoci dello sviluppo, il team ha rintracciato questa perdita cellulare principalmente in una scarsa migrazione degli interneuroni verso la corteccia, non in un aumento della morte cellulare o in una ridotta divisione cellulare.
Rimappare l'attività genica nelle cellule legate alle crisi
Per collegare questi cambiamenti fisici al controllo genico, il gruppo ha usato il sequenziamento a nucleo singolo che legge sia l'attività genica sia l'accessibilità del DNA nelle singole cellule. Nell'eminenza gangliare mediale embrionale, la maggior parte dei geni modificati nei mutanti era downregolata, inclusi regolatori chiave che indirizzano le cellule verso destini inibitori specifici. Negli interneuroni adulti, l'equilibrio tra sottotipi si è spostato e gruppi di geni coinvolti nella formazione delle connessioni e nel controllo dei correnti del potassio — i flussi che contribuiscono a determinare la velocità di scarica — erano regolati in modo anomalo. L'analisi di rete ha evidenziato una disturbata coordinazione dei geni dei canali del potassio noti per influenzare epilessia e ritmi cerebrali, fornendo un collegamento molecolare diretto tra la perdita di una marca istonica, l'alterazione dell'identità degli interneuroni e la suscettibilità alle crisi.
Sbilanciamento ipotalamico e una curva di crescita a due fasi
L'ipotalamo ha raccontato una storia complementare incentrata sulla crescita corporea. Da cuccioli, i topi mutanti erano più piccoli e una frazione sostanziale moriva precocemente. I sopravvissuti, tuttavia, in seguito mangiavano di più, accumulavano grasso e sviluppavano alti livelli dell'ormone leptina, segnali di obesità e probabile resistenza alla leptina. L'analisi a cellula singola dell'ipotalamo embrionale ha rivelato più progenitori in divisione ma meno cellule destinate ai nuclei chiave implicati nell'alimentazione, in particolare regioni che normalmente rilevano lo stato nutrizionale e regolano l'ormone della crescita. Nell'ipotalamo adulto, il mix cellulare è stato rimodellato: gli astrociti sono aumentati bruscamente, gli oligodendrociti sono diminuiti e cellule specializzate di barriera chiamate taniciti e i glia vicini hanno perso la disposizione ordinata all'interfaccia cerebrale con ormoni e nutrienti circolanti. Questi cambiamenti strutturali ed espressivi probabilmente alterano il modo in cui il cervello percepisce le riserve energetiche e controlla l'appetito.
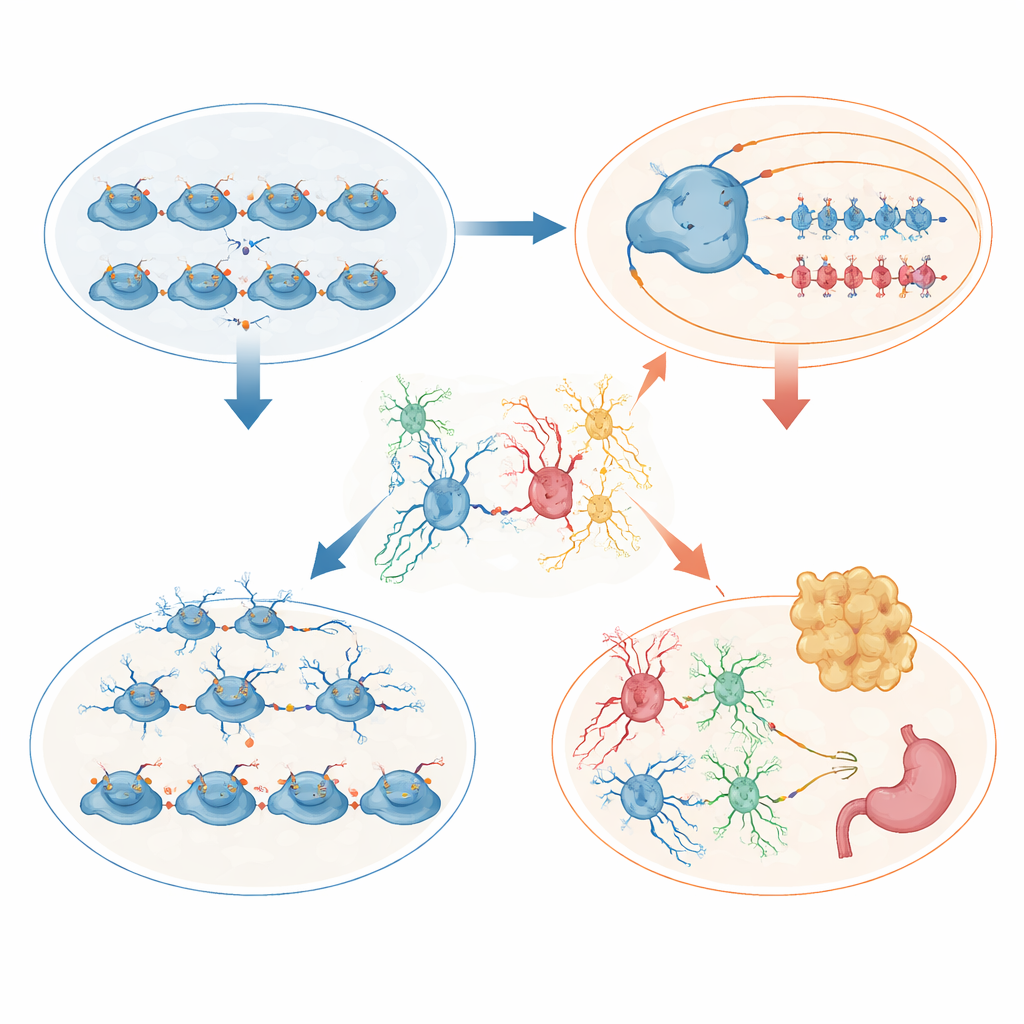
Echi comportamentali dei disturbi neuroevolutivi umani
Il comportamento dei topi richiamava sintomi osservati in molti disturbi neuroevolutivi. Mostravano un maggiore comportamento simile all'ansia, un'andatura alterata, ridotta attività spontanea a casa e scarse prestazioni in compiti che valutano memoria, riconoscimento di oggetti e filtraggio di suoni di startling. In alcuni test è emerso un aumento di comportamenti impulsivi. In molte misure, le femmine tendevano a essere più gravemente colpite rispetto ai maschi, suggerendo che sistemi ormonali e regolazione genica specifici del sesso possano interagire con le marche istoniche per modellare la vulnerabilità.
Cosa significa per la salute umana
Nel complesso, i risultati mostrano che indebolire un insieme di marche istoniche in sole due aree cerebrali embrionali è sufficiente a riprodurre una vasta costellazione di problemi: meno «freni» inibitori, reti cerebrali instabili, crisi epilettiche, circuiti alimentari disturbati e crescita corporea anomala. Per i non specialisti, il messaggio chiave è che le marche epigenetiche come la metilazione di H3K4 non sono aggiunte vaghe ma precise manopole di controllo che aiutano le cellule cerebrali in sviluppo a diventare il tipo giusto, nel posto giusto, al momento giusto. Quando queste manopole sono impostate in modo scorretto, come in molte sindromi genetiche rare, il risultato può essere una combinazione strettamente collegata di sintomi cognitivi, comportamentali e metabolici. Comprendere queste radici comuni potrebbe alla fine guidare terapie che correggano non solo un sintomo, come le crisi o l'obesità, ma il sistema interconnesso che li genera.
Citazione: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Parole chiave: epigenetica, interneuroni, ipotalamo, crisi epilettiche, obesità