Clear Sky Science · it
Disaccoppiare la separazione di fase e la fibrillizzazione preserva l’attività dei condensati biomolecolari
Perché è importante per la salute del cervello
Molte malattie cerebrali, compreso l’Alzheimer, coinvolgono proteine che nel tempo si aggregano in noduli duri e fibrosi. Quelle stesse proteine possono anche formare strutture più morbide, simili a goccioline, all’interno delle cellule che aiutano a organizzare la chimica cellulare, un po’ come piccole postazioni liquide di lavoro. Questo studio pone una domanda cruciale: possiamo fermare l’indurimento dannoso di queste goccioline in fibre senza distruggere la loro funzione utile nella quotidianità? Gli autori mostrano che un metabolita cellulare comune, l’amminoacido L-arginina, può fare esattamente questo per una proteina chiave legata all’Alzheimer chiamata Tau.
Da proteina libera a minuscole goccioline
All’interno delle cellule, certe proteine non restano sempre omogeneamente disperse nel fluido interno. Possono invece aggregarsi in goccioline, chiamate condensati biomolecolari, che si comportano come gel molto morbidi o liquidi densi. Il team si è concentrato su Tau, una proteina che normalmente aiuta a costruire e stabilizzare i microtubuli—filamenti cavi che fungono da strade all’interno dei neuroni. Tau è anche famosa per formare fibrille amiloidi, le fibre rigide presenti nei grovigli che caratterizzano molte malattie neurodegenerative. Per studiare come le goccioline di Tau evolvono nel tempo, i ricercatori hanno ingegnerizzato una versione della proteina, chiamata SynTag-Tau, che forma condensati attivi che invecchiano fino a formare fibrille amiloidi in un arco temporale sperimentalmente comodo, senza additivi aggressivi.
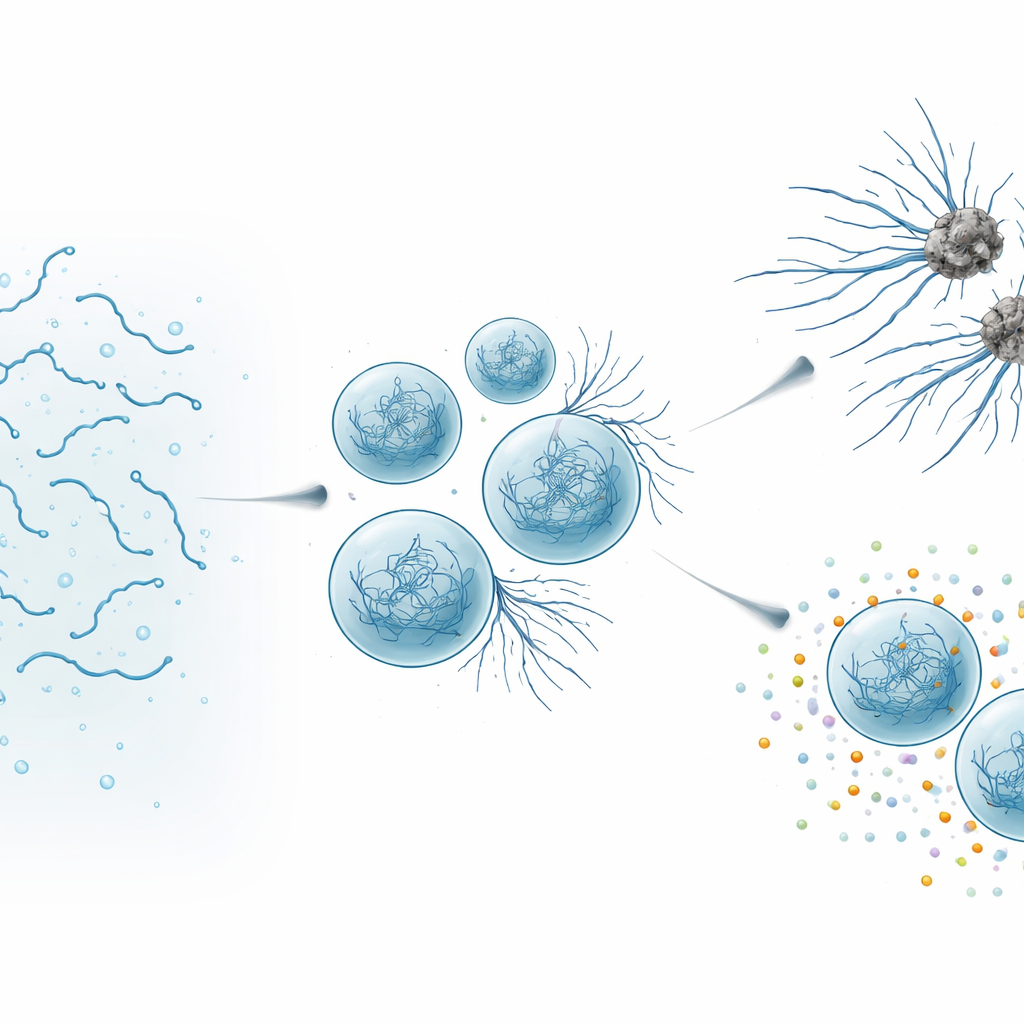
Quando le goccioline utili diventano dannose
Usando microscopia ad alta risoluzione e misure biofisiche, gli autori hanno osservato i cambiamenti delle goccioline di SynTag-Tau nell’arco di ore. Le goccioline fresche si comportavano come liquidi: si fondevano facilmente, le loro molecole si muovevano rapidamente e non c’era traccia di strutture ordinate. Col tempo le goccioline rallentavano e si irrigidivano, e sottili fibre cominciavano a spuntare dalle loro superfici verso la soluzione circostante. Metodi ottici sensibili hanno mostrato che queste fibre contenevano l’architettura “cross–beta” strettamente impaccata tipica degli amiloidi. È importante che l’interfaccia—il confine tra la gocciolina densa e il fluido circostante—si sia comportata come un punto caldo dove le fibrille apparivano per prime. Con l’invecchiamento e la formazione di sempre più fibre, la funzione normale di Tau peggiorava: i condensati diventavano meno efficaci nell’attrarre la tubulina, il mattoncino dei microtubuli, e infine perdevano del tutto la capacità di sostenere l’assemblaggio dei microtubuli.
Piccole molecole che alterano l’equilibrio
I ricercatori si sono poi chiesti se semplici metaboliti potessero rallentare o prevenire questa transizione da liquido a fibra lasciando intatte le goccioline. Testando diversi piccoli composti naturali, hanno scoperto che gli amminoacidi carichi positivamente L-arginina e L-lisina ritardavano fortemente o bloccavano la formazione di fibrille amiloidi dalle goccioline di SynTag-Tau, pur senza impedire la formazione delle goccioline a concentrazioni realistiche, nell’ordine dei millimolari bassi. Al contrario, amminoacidi carichi negativamente come glutammato e aspartato acceleravano la formazione delle fibrille, e agenti chimici in grado di denaturare le proteine o non aiutavano o disturbavano le goccioline stesse. Un analogo fluorescente della L-arginina ha rivelato che questa molecola preferisce localizzarsi all’interno dei condensati di Tau piuttosto che all’esterno, suggerendo che agisce dove è più necessaria.
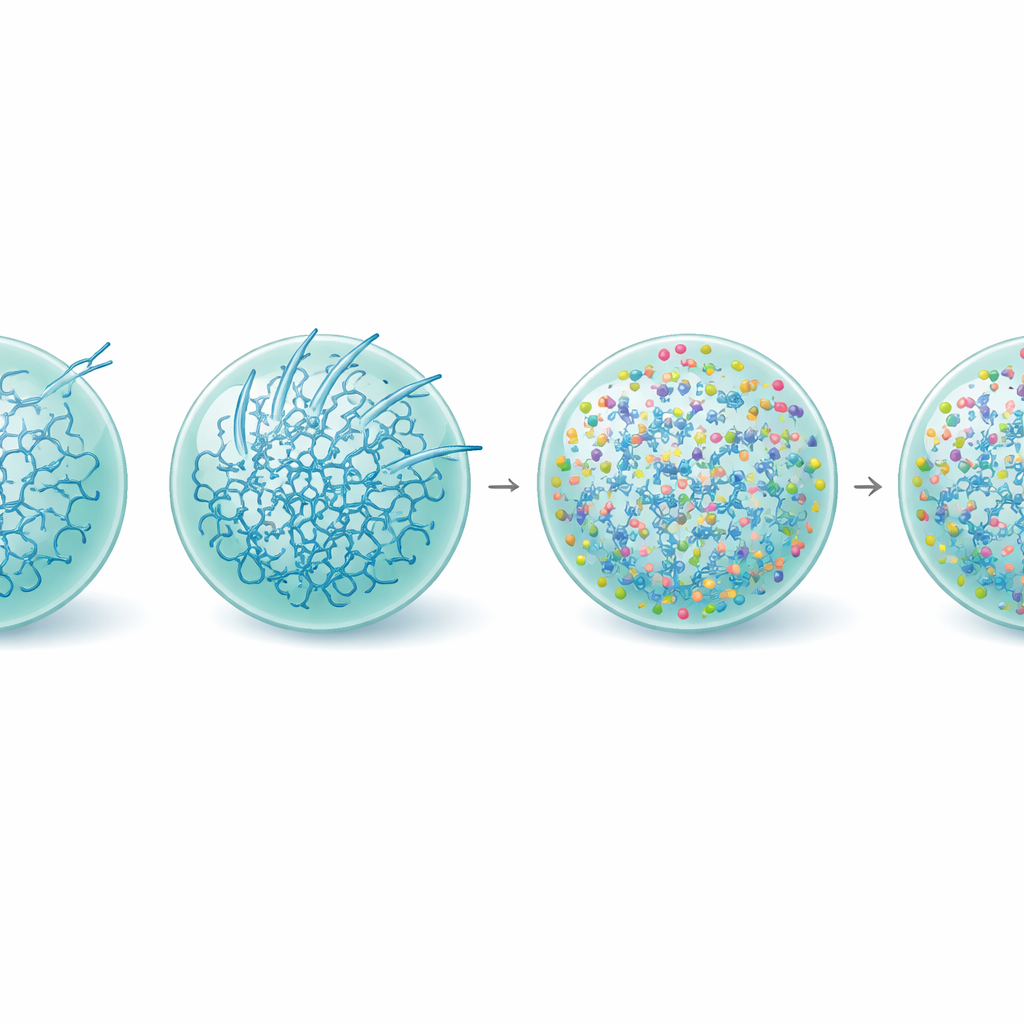
Irrigidire la gocciolina, salvare la funzione
Approfondendo, il team ha esaminato come la L-arginina rimodelli la vita interna delle goccioline di Tau. Misure sulla struttura proteica hanno mostrato che, in presenza di L-arginina, la frazione di molecole di Tau che assumevano le forme rigide ricche di beta tipiche dell’amiloide era ridotta, anche nelle goccioline più vecchie. La nanorheologia video-based—monitorando il movimento di piccole sfere all’interno dei condensati—ha rivelato che la L-arginina rendeva in realtà le goccioline di Tau più viscoelastiche, cioè la loro rete interna diventava più forte e interconnessa pur restando di tipo fluido. Questo rafforzamento sembra mantenere il sistema in uno stato metastabile e funzionale e aumenta la barriera energetica alla formazione di fibrille, in particolare alla superficie della gocciolina. Coerentemente con ciò, i condensati trattati con L-arginina continuavano a reclutare tubulina in modo uniforme e sostenevano la crescita dei microtubuli molto dopo che le goccioline non trattate erano diventate inattive.
Cosa significa per le terapie future
Il lavoro dimostra che le forze che guidano la formazione delle goccioline proteiche e quelle che portano alla formazione di fibre dannose sono correlate ma separabili. Modulando la chimica all’interno dei condensati con un metabolita come la L-arginina, è possibile preservare lo stato benefico e di tipo liquido mentre si ritarda o si previene la transizione verso fibrille amiloidi legate alla malattia. Sebbene questo studio usi un sistema Tau appositamente ingegnerizzato in vitro, offre una prova di principio: piccole molecole che fortificano selettivamente la stabilità dei condensati potrebbero un giorno aiutare a proteggere le cellule dall’accumulo graduale di aggregati proteici tossici senza bloccare i ruoli organizzativi normali dei condensati biomolecolari.
Citazione: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Parole chiave: Proteina Tau, condensati biomolecolari, fibrille amiloidi, L-arginina, neurodegenerazione