Clear Sky Science · it
Varianti di FOXJ3 associati all’epilessia collegano un programma trascrizionale della via PTEN-mTOR alla specificazione neuronale e alla laminazione corticale
Quando il cablaggio cerebrale devia leggermente
L’epilessia spesso esordisce durante l’infanzia, ma in molti giovani pazienti i medici non riescono a rilevare nulla di evidentemente anomalo nelle scansioni cerebrali. Questo studio affronta una causa nascosta: piccole alterazioni in un gene chiamato FOXJ3 che rimodellano in modo sottile il modo in cui si costruisce lo strato esterno del cervello, la corteccia. Seguendo l’attività di questo gene in famiglie con epilessia focale e nei cervelli in via di sviluppo del topo, i ricercatori mostrano come passi falsi precoci nella nascita, nel movimento e nella stratificazione delle cellule possano alla lunga dare origine a crisi epilettiche.
Una malformazione sottile dietro crisi difficili da trattare
Molti bambini con epilessia focale resistente ai farmaci presentano una condizione detta displasia corticale focale (FCD), in cui aree di corteccia sono malformate. Queste regioni contengono cellule nervose dislocate e anormalmente grandi e sono una causa comune per cui i farmaci non riescono a controllare le crisi. Tuttavia la causa molecolare della FCD è spesso sconosciuta e la risonanza magnetica standard può non rilevare difetti piccoli o superficiali. Gli autori hanno iniziato da una famiglia in cui diversi membri avevano epilessia focale e segni di FCD. Un’analisi genomica accurata ha indicato cambiamenti rari in FOXJ3, un gene non precedentemente associato all’epilessia. Casi aggiuntivi da grandi banche genetiche hanno rivelato altre persone con varianti insolite di FOXJ3 e crisi focali, suggerendo che questo gene possa essere un protagonista ricorrente in tali disturbi.
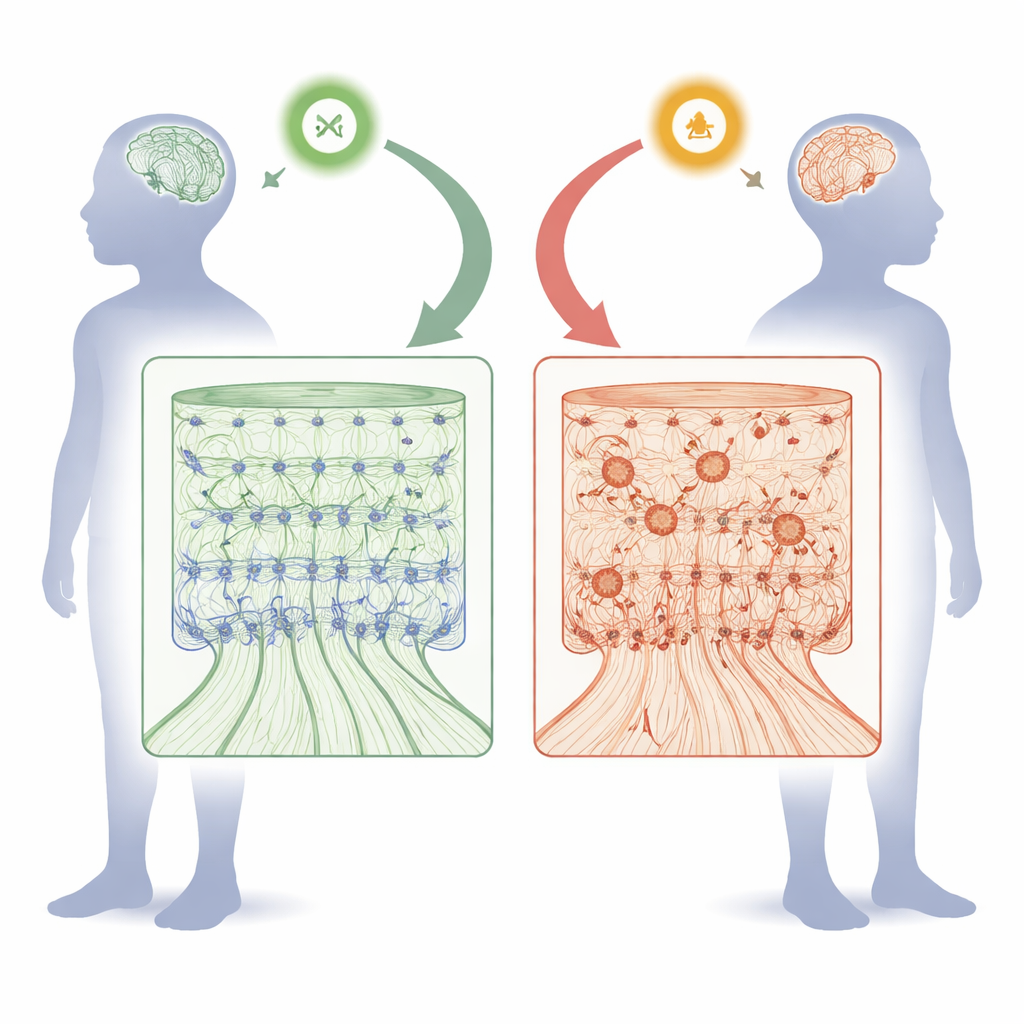
Come FOXJ3 contribuisce a plasmare la superficie pensante del cervello
Durante lo sviluppo fetale la corteccia si assembla come un edificio a più piani. Cellule simili a staminali che rivestono la superficie interna del cervello si dividono, poi inviano i neuroni neonati verso l’esterno lungo “impalcature” radiali per formare sei strati ordinati. Il gruppo ha scoperto che FOXJ3 è attivo sia in questi progenitori simili a staminali sia nei neuroni giovani, ma la sua attività nei progenitori diminuisce naturalmente dopo un preciso momento a metà gestazione. Usando strumenti di silenziamento genico negli embrioni di topo, i ricercatori hanno ridotto i livelli di Foxj3 in fasi diverse e osservato cosa accadeva. La perdita precoce di Foxj3 ha rallentato la migrazione dei neuroni neonati e ha determinato il loro posizionamento in strati errati. Cellule che avrebbero dovuto diventare neuroni degli strati profondi hanno invece assunto identità tipiche degli strati superiori, e i neuroni a proiezione callosale, che collegano i due emisferi cerebrali, sono stati prodotti in eccesso. Più avanti nello sviluppo, tuttavia, la riduzione di Foxj3 aveva effetti molto più lievi, mostrando che il suo ruolo è fortemente sensibile al tempo.
Mantenere l’equilibrio tra divisione cellulare e crescita
Per capire perché FOXJ3 esercita tale influenza, i ricercatori hanno combinato diversi approcci su larga scala. Hanno mappato dove FOXJ3 si lega al DNA e quali geni sono attivi in migliaia di singole cellule corticali. Questo ha evidenziato in modo netto geni che regolano il ciclo cellulare e la crescita cerebrale, in particolare PTEN, un freno importante su una via di crescita nota come mTOR. Nei progenitori, il legame di FOXJ3 favoriva l’attività di PTEN, che a sua volta aiutava le cellule a uscire dal ciclo di divisione, trasformarsi in neuroni e migrare verso l’esterno in modo ordinato. Quando Foxj3 veniva silenziato, più progenitori restavano in uno stato di divisione, meno uscivano dal ciclo nei tempi giusti e la migrazione si arrestava nelle zone intermedie. Crucialmente, ripristinare i livelli di PTEN nei cervelli carenti di Foxj3 ha in gran parte invertito i problemi di migrazione, stratificazione e destinazione cellulare, mentre potenziare un altro regolatore della crescita, TSC1, non lo ha fatto. Questo colloca PTEN al centro del controllo esercitato da FOXJ3 sulla costruzione corticale.
Dalle vie malregolate a neuroni ingrossati
Il gruppo ha poi esaminato come si comportano varianti di FOXJ3 simili a quelle riscontrate nei pazienti. Una versione associata a malattia di FOXJ3 non riusciva ad aumentare i livelli di PTEN e permetteva alla via mTOR di diventare iperattiva, come dimostrato dall’aumentata fosforilazione di una proteina chiave legata alla crescita. In topi adolescenti ingegnerizzati per esprimere questa forma mutante nella corteccia in sviluppo, i neuroni apparivano successivamente visibilmente rigonfiati, con corpi cellulari e perimetri più grandi, imitando le cellule dismorfiche osservate nella FCD umana. Tuttavia la proteina mutante raggiungeva comunque correttamente il nucleo, indicando che il problema risiede nella regolazione genica difettosa e non in una errata localizzazione. Nel complesso, questi risultati collegano le mutazioni di FOXJ3 a una cascata di eventi—meno PTEN, più segnalazione mTOR, ritardo nell’uscita dal ciclo cellulare, migrazione confusa e neuroni ipertrofici—che possono predisporre alla formazione di reti epilettiche.
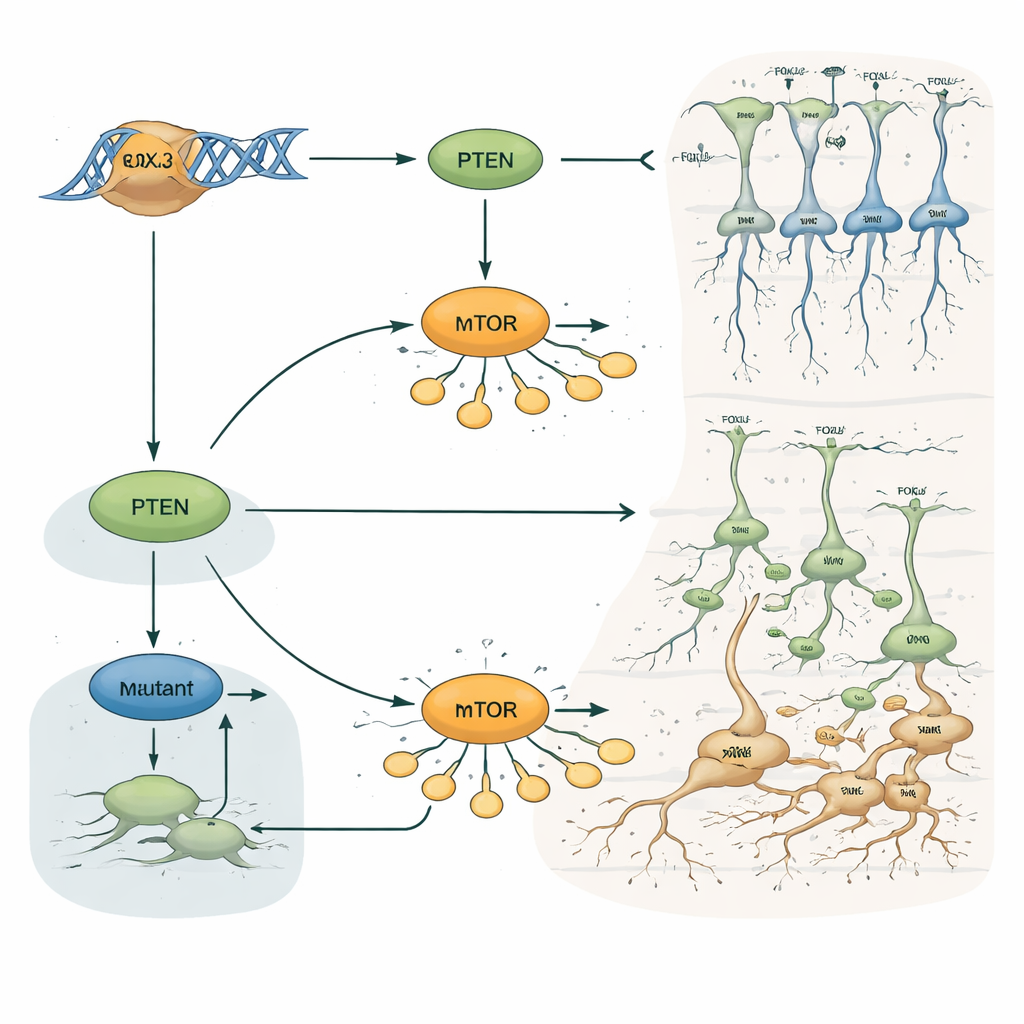
Perché questo è importante per l’epilessia e le lesioni cerebrali nascoste
Per un non specialista, il messaggio chiave è che un singolo fattore di trascrizione, FOXJ3, contribuisce a decidere quando e dove nascono i neuroni corticali, come si muovono e in quale strato finiscono. Agendo tramite la via di crescita PTEN–mTOR, FOXJ3 mantiene la costruzione cerebrale nei tempi previsti. Variazioni rare in questo gene possono sbilanciare tale equilibrio, causando piccole aree di corteccia con connettività e stratificazione errate, anche quando le scansioni MRI sembrano normali. Questo lavoro non solo propone FOXJ3 come nuova causa genetica della displasia corticale focale e dell’epilessia, ma illustra anche come spostamenti sottili nello sviluppo cerebrale precoce possano riverberare decenni dopo sotto forma di crisi difficili da trattare.
Citazione: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Parole chiave: displasia corticale focale, gene FOHJ3, via PTEN mTOR, sviluppo corticale, epilessia focale