Clear Sky Science · it
Base molecolare della galattosilazione del collagene da parte di GLT25D1
Come piccoli tag di zucchero aiutano a costruire tessuti resistenti
Il collagene è la proteina più comune del corpo, formando l’impalcatura per pelle, ossa, vasi sanguigni e molti altri tessuti. Ma il collagene non funziona da solo: deve essere decorato con piccole molecole di zucchero in punti precisi per acquisire la giusta resistenza e flessibilità. Questo studio rivela, in dettaglio atomico, come un enzima chiave, GLT25D1, collega uno zucchero specifico al collagene e come difetti in questo processo possano portare a vasi fragili, problemi muscolari e forse anche al cancro.
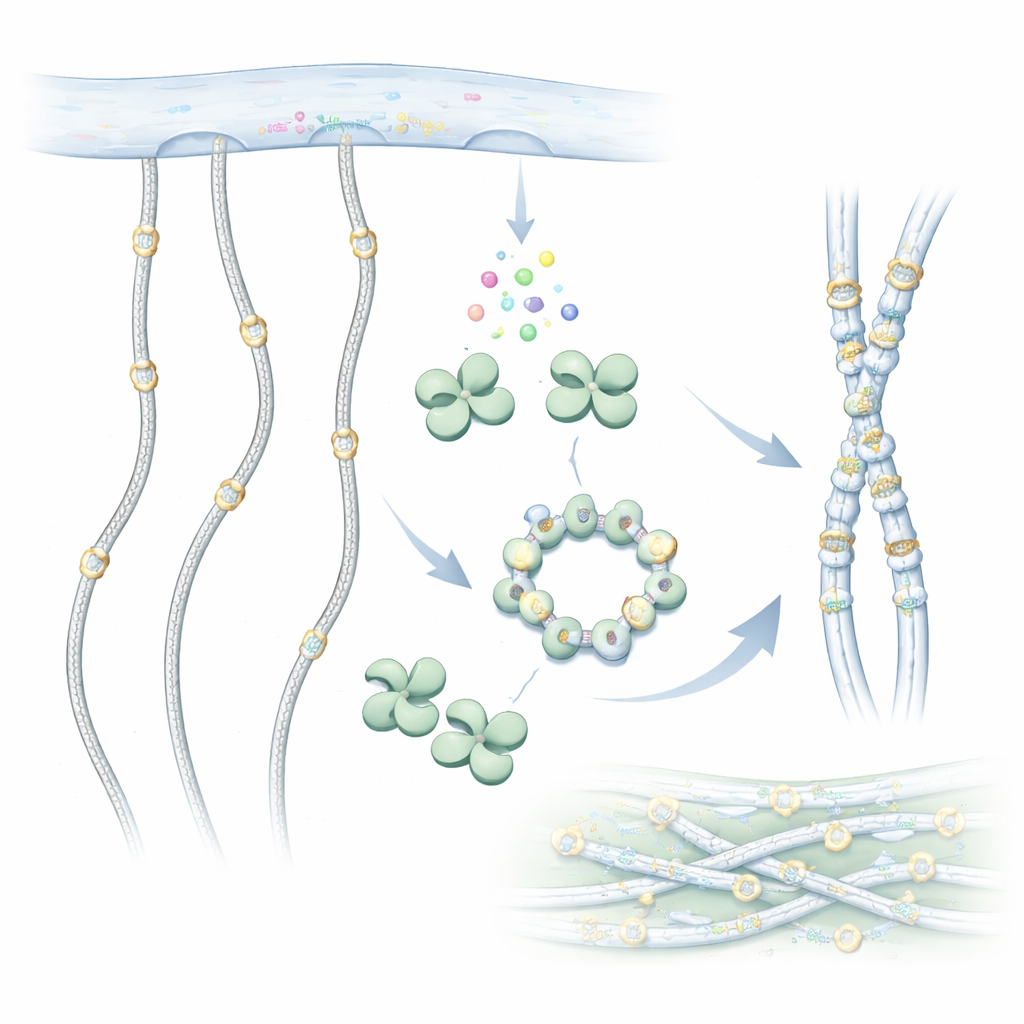
Uno sguardo ravvicinato alla ristrutturazione nascosta del collagene
Le molecole di collagene sono catene lunghe e simili a corde che si assemblano in fibre robuste fuori dalle cellule. Prima di essere esportate, però, vengono modificate chimicamente. Una modifica importante è l’aggiunta di gruppi zuccherini a particolari mattoni chiamati idrossilisine lungo la catena di collagene. GLT25D1 esegue il primo passo in questo marchio zuccherino, trasferendo una molecola di galattosio da un donatore sull’idrossilisina. Questa decorazione zuccherina è conservata dagli animali più semplici fino all’uomo e aiuta il collagene a ripiegarsi correttamente, a interagire con le cellule e a resistere all’usura.
Rivelare la forma di un decoratore del collagene
Per capire come funziona GLT25D1, i ricercatori hanno utilizzato la criomicroscopia elettronica per ottenere immagini dell’enzima umano a risoluzione quasi atomica. Hanno scoperto che ogni molecola di GLT25D1 presenta due lobi simili, entrambi riconducibili a un comune ripiegamento enzimatico osservato nelle proteine trasferenti di zuccheri. Questi lobi si accoppiano per formare dimeri allungati e tre dimeri possono ulteriormente assemblarsi in un esamer ovale a forma di anello. In questi complessi, i veri motori — i centri catalitici — sono posti a distanza, una disposizione che potrebbe permettere a diversi siti di aggiunta di zucchero di operare lungo una catena di collagene tesa contemporaneamente.
Le parti operative: dove avviene davvero il trasferimento dello zucchero
Il gruppo ha risolto le strutture di GLT25D1 legata sia al donatore di zucchero sia a un breve peptide simile al collagene contenente idrossilisina. Questo complesso ternario ha mostrato che solo il secondo lobo, chiamato dominio C-terminale, svolge effettivamente la chimica. Lì, la molecola donatrice si alloggia in una tasca stabilizzata da uno ione metallico, mentre il peptide giace in una stretta scanalatura che impone un motivo locale specifico: un’idrossilisina seguita immediatamente da una minuscola glicina. Un singolo residuo di aspartato agisce da base chimica, attivando il gruppo ossidrile dell’idrossilisina in modo che possa attaccare lo zucchero e completare il trasferimento. Alterazioni di uno qualsiasi di questi amminoacidi chiave riducono drasticamente o annullano l’attività, confermandone i ruoli essenziali.
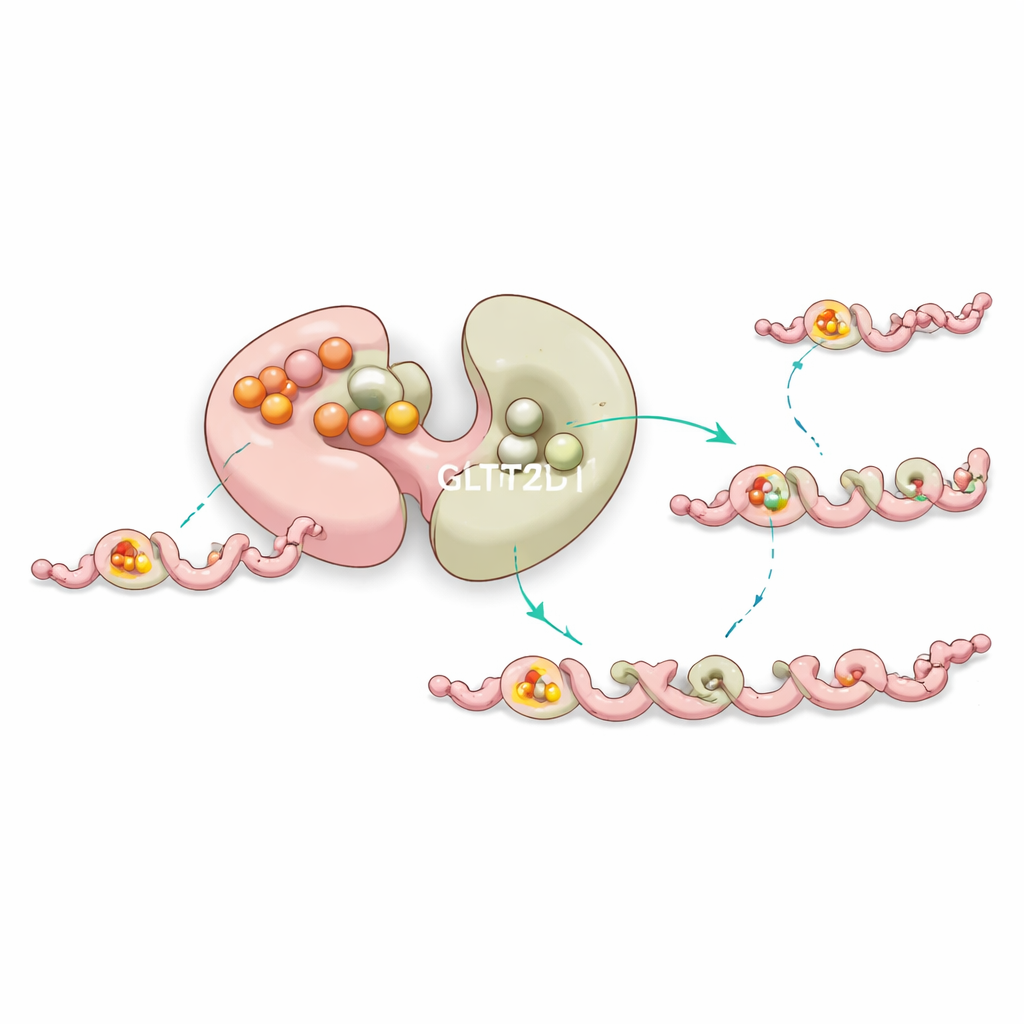
Uno stabilizzatore incorporato e controllo a lunga distanza
Curiosamente, il primo lobo di GLT25D1 lega molto saldamente un donatore di zucchero ma non esegue il trasferimento. Esperimenti e simulazioni al computer suggeriscono invece che questo sito “silente” aiuti a stabilizzare l’enzima e moduli sottilmente il comportamento del lobo attivo tramite comunicazione a lungo raggio all’interno della proteina. Mutazioni vicino a questa tasca non catalitica spesso destabilizzano l’enzima o ne spostano l’efficienza, suggerendo che la natura utilizza questo sito di legame aggiuntivo come una forma di controllo qualità interno per mantenere la modifica del collagene fluida.
Quando il decoratore fallisce: collegamenti con le malattie
Mappando le mutazioni ricavate da pazienti sul loro modello strutturale, gli autori hanno potuto spiegare come errori in GLT25D1 conducano a malattie umane. Alcune mutazioni eliminano completamente il lobo catalitico, altre destabilizzano il nucleo proteico e altre ancora colpiscono direttamente i siti di legame dello zucchero o del collagene. Questi difetti riducono o annullano l’aggiunta di zucchero al collagene e sono stati collegati a malattie dei piccoli vasi cerebrali, problemi cognitivi e difetti muscoloscheletrici. Mutazioni associate al cancro si raggruppano anch’esse in regioni cruciali, suggerendo che una decorazione alterata del collagene possa influenzare la crescita e la diffusione tumorale.
Perché questo è importante per la salute e i trattamenti futuri
Tracciando una mappa tridimensionale dettagliata di GLT25D1 in azione, questo lavoro spiega come vengono aggiunti i precisi tag zuccherini al collagene e perché questo passaggio sia fondamentale per l’integrità dei tessuti. Per i non specialisti, il messaggio chiave è che piccole modifiche chimiche sul collagene possono avere effetti molto ampi su vasi sanguigni, ossa e possibilmente sul rischio di cancro. La mappa strutturale di GLT25D1 offre ora una guida per diagnosticare varianti dannose e per progettare terapie — sia piccole molecole che stabilizzino enzimi difettosi sia strategie basate sul gene — che un giorno potrebbero correggere alla fonte i difetti di marcatura zuccherina del collagene.
Citazione: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Parole chiave: glicosilazione del collagene, GLT25D1, matrice extracellulare, malattia vascolare, struttura cryo-EM