Clear Sky Science · it
La carenza di sclerostina rende gli adipociti bianchi più sensibili ai segnali termogenici che inducono il beiging nei topi
Perché riscaldare il grasso potrebbe raffreddare le malattie
La maggior parte di noi considera l'osso e il tessuto adiposo come mondi separati: l'uno ci dà struttura, l'altro immagazzina energia. Questo studio sui topi rivela che osso e grasso sono in costante conversazione chimica e che una proteina prodotta dalle cellule ossee può decidere se il nostro grasso «bianco» rimane inattivo a immagazzinare calorie o si trasforma in un grasso «beige» più attivo e consumatore di energia. Comprendere questo dialogo nascosto potrebbe aprire nuove strade per affrontare contemporaneamente obesità, diabete e perdita di densità ossea.
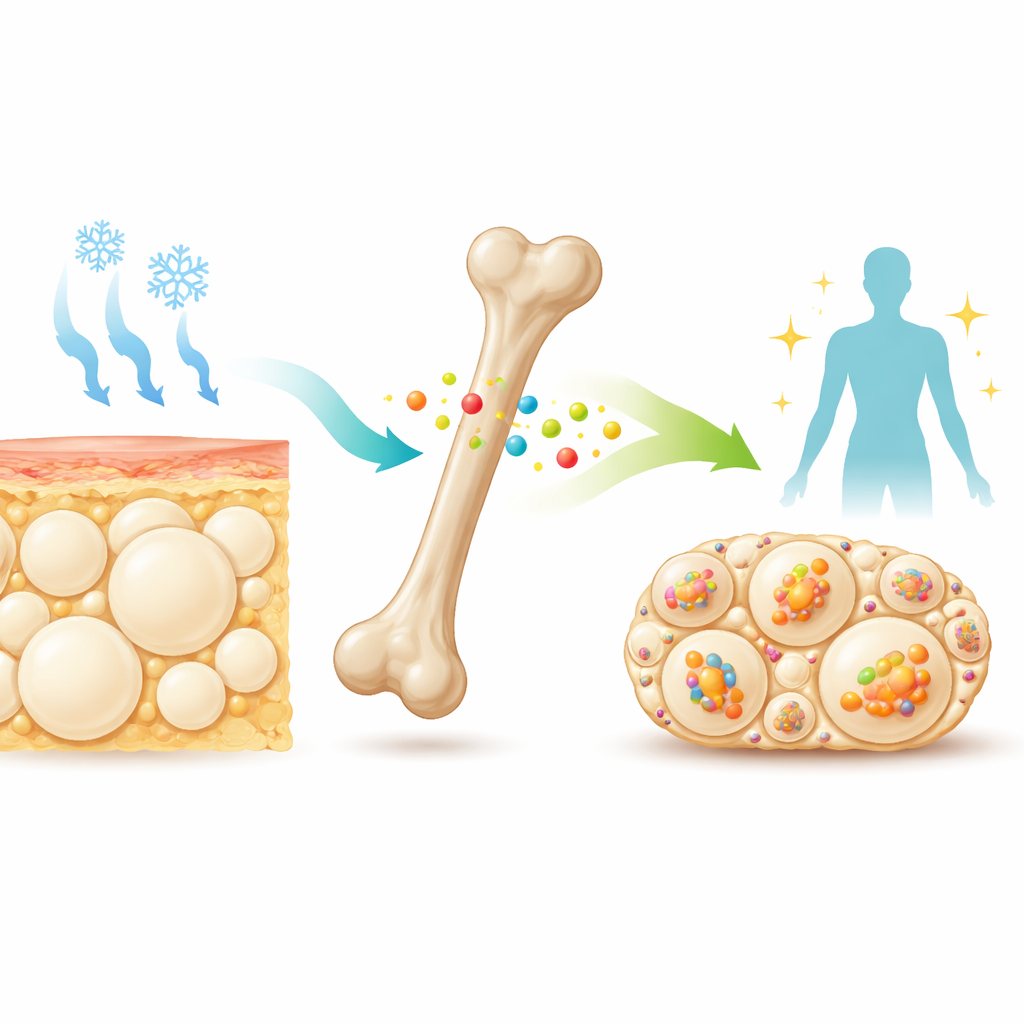
Un messaggero silenzioso dall'osso
Nel profondo delle ossa, cellule specializzate rilasciano nel flusso sanguigno una piccola proteina chiamata sclerostina. I medici già prendono di mira la sclerostina con farmaci per rafforzare le ossa nei pazienti a rischio di fratture. Lavori precedenti avevano mostrato che i topi privi di sclerostina non sono solo più robusti nelle ossa, ma anche più magri e più sensibili all'insulina. Il loro tessuto adiposo sottocutaneo, in particolare quello attorno ai fianchi (grasso bianco inguinale), contiene piccole cellule adipose a compartimenti multipli che ricordano il grasso beige, capace di bruciare carburante per produrre calore. Questi indizi hanno spinto i ricercatori a chiedersi se la sclerostina agisca normalmente come un freno alla capacità dell'organismo di convertire il grasso bianco in beige quando esposto al freddo o a farmaci che mimano i segnali nervosi al tessuto adiposo.
Segnali freddi, segnali dall'osso e accensione del grasso
Il gruppo ha esposto topi normali e topi privi del gene della sclerostina (Sost-/-) a un farmaco che attiva un recettore specifico delle cellule adipose (recettore β3-adrenergico), oppure a un freddo lieve. Negli animali normali, questi segnali termogenici aumentavano la produzione di sclerostina nell'osso e il suo livello nel sangue. Questo aumento si associava a una perdita di osso spugnoso ma solo a cambiamenti modesti nel grasso sottocutaneo. Al contrario, i topi carenti di sclerostina mostravano una risposta molto più marcata: il loro grasso inguinale assorbiva più glucosio, rilasciava più acidi grassi, si riduceva di dimensione e si riempiva di cellule simili al beige, ricche di mitocondri, le centrali energetiche cellulari. I geni termogenici chiave si attivavano più intensamente in questi topi, specialmente nel grasso sottocutaneo, mentre il classico grasso bruno rimaneva in gran parte invariato.
Regolare la combustione del grasso tramite un interruttore condiviso
Per capire come la sclerostina eserciti questo controllo, i ricercatori si sono concentrati sulla β-catenina, una proteina coinvolta nella via di segnalazione Wnt che la sclerostina normalmente sopprime nelle ossa. Nel tessuto adiposo, l'attivazione postnatale della β-catenina spingeva le cellule bianche verso uno stato simile al beige e aumentava la loro risposta ai segnali β3-adrenergici, ma questo effetto scompariva quando i topi venivano tenuti a temperatura termoneutrale, dove il corpo non ha più bisogno di calore aggiuntivo. Al contrario, la delezione specifica della β-catenina nelle cellule adipose di topi carenti di sclerostina cancellava il tessuto beige, ripristinava cellule adipose bianche più grandi e invertiva i miglioramenti nei livelli di insulina e acidi grassi. Questi esperimenti suggeriscono che, quando la sclerostina è bassa, la β-catenina nelle cellule adipose diventa una leva interna importante che rende il grasso bianco più reattivo agli stimoli termogenici.
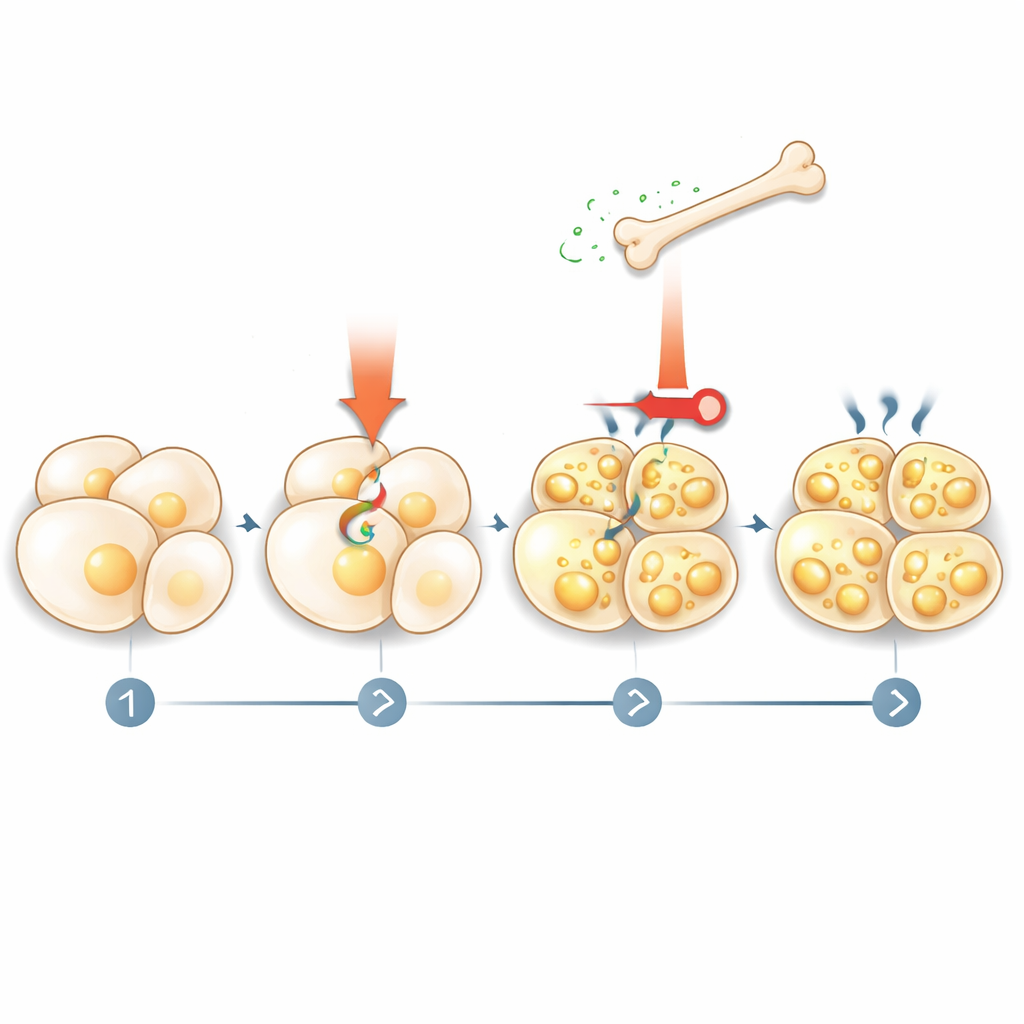
Come il grasso risponde all'osso
La storia non si è fermata all'osso che dice al grasso cosa fare. Il team ha scoperto che la stimolazione termogenica attiva la degradazione del grasso (lipolisi), rilasciando acidi grassi nel sangue. Questi acidi grassi, a loro volta, agiscono sulle cellule ossee tramite un recettore nucleare chiamato PPARγ, aumentando la produzione di sclerostina. Quando i ricercatori bloccarono la lipolisi nelle cellule adipose o rimossero il PPARγ dalle cellule ossee, i farmaci che mimavano il freddo non riuscivano più ad aumentare i livelli di sclerostina. Questo rivela un circuito di feedback: i segnali termogenici inducono il grasso a rilasciare carburante, questo carburante istruisce l'osso a secernere più sclerostina, e la sclerostina a sua volta limita ulteriori attivazioni del grasso e il beiging.
Abbinare farmaci per osso e grasso a vantaggio del metabolismo
Infine, i ricercatori testarono se interrompere questo circuito potesse aiutare in un contesto simile alla malattia. Topi obesi sottoposti a una dieta ricca di grassi ricevettero una dose bassa di mirabegron (un farmaco β3-adrenergico già usato per problemi della vescica), un anticorpo che neutralizza la sclerostina (romosozumab, approvato per l'osteoporosi), o entrambi. Mentre ciascun farmaco da solo aveva effetti modesti, la combinazione ridusse la massa grassa in depositi chiave, spostò il tessuto verso cellule più piccole e più attive, abbassò insulina, trigliceridi e colesterolo e preservò la robustezza ossea. L'alloggio in ambiente caldo, che riduce il bisogno di calore del corpo, cancellò in gran parte i benefici metabolici della perdita di sclerostina, sottolineando che questa via è importante soprattutto quando sono presenti segnali termogenici.
Cosa significa per i trattamenti futuri
In termini semplici, questo lavoro mostra che l'osso non è solo uno scheletro passivo ma un regolatore attivo di quanta energia bruciano le cellule adipose. La sclerostina funziona come una manopola che mantiene sotto controllo l'attività del grasso termogenico e quindi l'uso di carburante. Abbassare quella manopola — per via genetica o farmacologica — rende alcuni depositi di grasso bianco più propensi a passare a uno stato produttore di calore quando l'organismo viene stimolato dal freddo o da farmaci specifici. Poiché la stessa intervento può rafforzare le ossa e migliorare la salute metabolica nei topi, combinazioni attentamente studiate di terapie mirate all'osso e al grasso potrebbero un giorno aiutare a trattare insieme obesità, diabete e osteoporosi, anziché una malattia alla volta.
Citazione: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Parole chiave: sclerostina, grasso beige, crosstalk osso–grasso, termogenesi, malattie metaboliche