Clear Sky Science · it
Sintesi locale di PI(4,5)P2 da isoforme PIPKIγ associate ai settini controlla l’associazione del centralspindlin con il midbody durante la citocinesi
Come le cellule completano la separazione in due
La citocinesi — il pizzicamento finale che divide una cellula in due — è facile da dare per scontata, ma quando fallisce può contribuire allo sviluppo del cancro e di altre malattie. Questo studio rivela come un insieme specifico di molecole agisca come capisquadra di cantiere sul sottile ponte che collega due cellule neonate, assicurando che la separazione si completi correttamente invece di arrecare un ripristino o bloccarsi.
L’ultimo ponte tra cellule figlie
Dopo che una cellula ha duplicato il materiale genetico e separato i cromosomi, deve dividersi fisicamente. Un anello contrattile di filamenti proteici si stringe attorno alla metà della cellula, creando una profonda scissura detta solco di divisione. Man mano che questo solco si richiude, le due cellule figlie restano collegate da un sottile ponte intercellulare che contiene un nucleo denso, il midbody. Il midbody è una struttura piccola ma complessa composta da microtubuli impaccati, proteine impalcature e lipidi segnalatori; funge sia da legame sia da centro di controllo che coordina gli ultimi passaggi della divisione e il taglio finale tra le cellule. 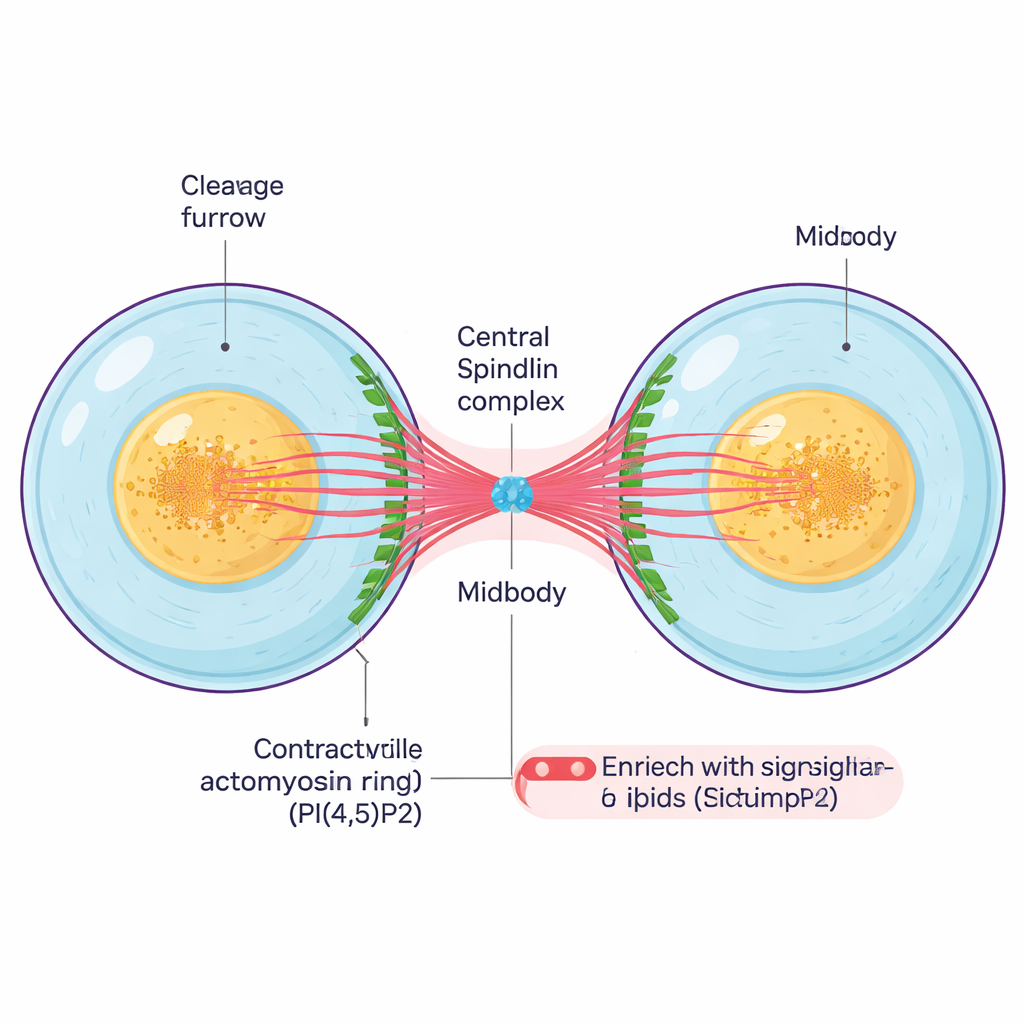
Un segnale lipidico che deve trovarsi nel posto giusto
Un attore chiave in questo processo è una molecola grassa segnalatrice nella membrana cellulare chiamata PI(4,5)P2. Questo lipide aiuta ad ancorare molte proteine che costruiscono e restringono l’anello contrattile e stabilizzano il ponte. Il quesito è come le cellule regolino dove e quando compare PI(4,5)P2, dato che può diffondere nella membrana. Gli autori si sono concentrati su enzimi detti chinasi PIP di tipo I, che sintetizzano PI(4,5)P2, e in particolare su un gene, PIPKIγ, che esiste in diverse isoforme da splicing. Riducendo selettivamente ciascuna chinasi in cellule umane e osservando gli effetti con microscopia avanzata, hanno scoperto che PIPKIγ ha un ruolo specifico nelle fasi tardive della citocinesi, quando si formano il ponte e il midbody, pur non alterando fortemente i livelli complessivi di PI(4,5)P2 sulla superficie cellulare.
Le impalcature dei setti reclutano un enzima specializzato
Il gruppo ha scoperto che due varianti di splicing di PIPKIγ, chiamate i3 e i5, funzionano come strumenti di precisione portati nel punto giusto da proteine strutturali note come settini (septins). I settini formano filamenti e anelli che aiutano a modellare il ponte e a organizzare altri componenti. Pull-down biochimici e imaging cellulare hanno mostrato che PIPKIγ-i3 e PIPKIγ-i5 si legano fisicamente ai complessi di settini e decorano i filamenti di settini, mentre altre varianti di PIPKIγ non lo fanno. Quando i ricercatori hanno mutato due specifici amminoacidi negli inserti di questi splicing, le chinasi non potevano più legare i settini. Nelle cellule in divisione, le forme normali PIPKIγ-i3/i5 passano da un pattern diffuso di membrana a concentrarsi nel solco di divisione e poi a delineare il ponte intercellulare e il midbody in sincronia con i settini e un’altra proteina impalcatura, anillina. Rimuovendo soltanto le varianti i3 e i5, anillina e settini si disperdevano lungo il ponte lontano dal midbody, e molte cellule fallivano la citocinesi, terminando con più nuclei.
La produzione locale di lipidi fissa il macchinario della divisione
Per verificare se questi effetti dipendessero dalla produzione locale di PI(4,5)P2, gli autori misurarono il PI(4,5)P2 attorno al midbody e manipolarono enzimi che aggiungono o rimuovono questo lipide. La deplezione di PIPKIγ-i3/i5 ridusse PI(4,5)P2 al midbody, mentre il blocco di un enzima degradante PI(4,5)P2 provocò l’effetto opposto. Importante, il ripristino di una forma di splicing cataliticamente attiva di PIPKIγ in grado di legare i settini rescue la corretta concentrazione di anillina e settini al ponte, ma varianti cataliticamente inattive o incapaci di legare i settini non lo facevano. Con imaging in vivo e una tecnica di microscopia di espansione che gonfia fisicamente il campione per rivelare dettagli fini, il gruppo ha mostrato che senza PIPKIγ-i3/i5 i settini non migrano più sui microtubuli del ponte, il ponte diventa più corto e meno impaccato e un complesso cruciale chiamato centralspindlin non rimane strettamente associato al midbody. 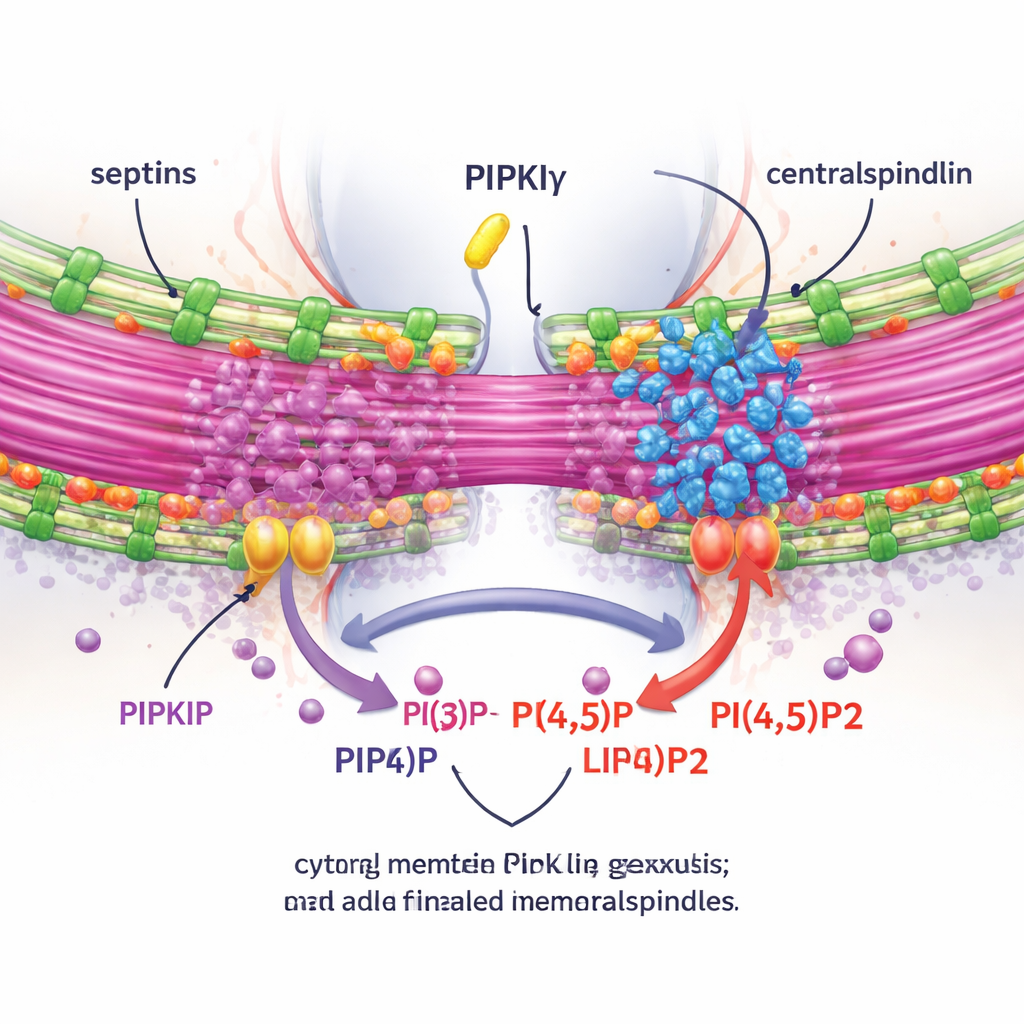
Costruire un checkpoint per un taglio pulito
Il centralspindlin aiuta a collegare i microtubuli del midbody alla membrana circostante e regola piccoli interruttori molecolari che controllano la forma cellulare. Lo studio mostra che il centralspindlin si associa sia ai settini sia a PIPKIγ, e che la perdita di uno dei due partner indebolisce in modo simile la sua presenza al midbody. Gli autori propongono che i settini reclutino PIPKIγ-i3/i5 nel solco increspato, dove questi enzimi generano una patch concentrata di PI(4,5)P2. Questa riserva lipidica locale, a sua volta, stabilizza anillina, centralspindlin e settini vicino al midbody, favorisce l’impacchettamento e la stabilizzazione dei microtubuli del ponte e permette al ponte intercellulare di maturare fino al taglio finale di abscission. Se questo sistema viene perturbato, PI(4,5)P2 compare nei posti sbagliati, le proteine impalcature si disperdono, i microtubuli sono poco impaccati e la citocinesi spesso fallisce.
Perché è importante oltre la biologia cellulare di base
Individuando come varianti specifiche di splicing di PIPKIγ e i settini cooperino per generare un segnale lipidico locale al midbody, questo lavoro spiega come le cellule conferiscano precisione spaziale a una molecola segnalatrice molto mobile. Tale precisione è cruciale per il completamento sicuro della divisione cellulare, contribuendo a prevenire la mis-segregazione dei cromosomi e numeri cellulari anomali che possono favorire lo sviluppo tumorale. Le stesse strutture del midbody influenzano anche il destino cellulare e la proliferazione dopo la divisione, quindi comprendere come si assemblano apre nuove vie per esplorare come errori in queste impalcature nanoscopiche possano contribuire al cancro e, forse, per manipolare cellule staminali.
Citazione: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Parole chiave: divisione cellulare, citocinesi, lipidi segnalatori, settin, biologia del cancro