Clear Sky Science · it
Il pan-RAF inibitore exarafenib prende di mira BRAF di classe II/III in NSCLC e rivela resistenza ARAF-KSR1 e strategie di combinazione
Perché questa ricerca è importante per i pazienti con tumore polmonare
La maggior parte delle persone ha sentito parlare di farmaci oncologici mirati che colpiscono specifiche alterazioni genetiche. Ma per molti pazienti con cancro al polmone, in particolare per quelli i cui tumori presentano mutazioni meno comuni nel gene BRAF, i farmaci mirati attuali semplicemente non funzionano. Questo studio presenta un nuovo farmaco sperimentale, exarafenib, progettato per agire su un più ampio insieme di tumori guidati da BRAF e spiega come le cellule tumorali tentino di sfuggirgli—rivelando combinazioni di trattamento che potrebbero mantenere questi tumori sotto controllo più a lungo.
Una maggioranza nascosta di mutazioni trascurate
I ricercatori hanno iniziato ponendosi una domanda di base: quanto sono comuni i diversi tipi di mutazioni BRAF nei tumori avanzati, e in particolare nel carcinoma polmonare non a piccole cellule (NSCLC)? Utilizzando un vasto database di biopsie liquide con oltre 160.000 pazienti, hanno analizzato frammenti di DNA tumorale circolante nel sangue. Hanno scoperto che nel cancro polmonare le mutazioni BRAF si riscontrano in circa il 4–5% dei pazienti, il che si traduce comunque in molte migliaia di persone nel mondo. Crucialmente, circa due terzi di questi tumori polmonari presentavano le cosiddette mutazioni BRAF di Classe II e Classe III—tipologie che gli attuali farmaci BRAF approvati non riescono a bersagliare efficacemente. I pazienti con una di queste classi, in particolare la Classe II, tendevano a vivere meno a lungo rispetto a quelli con la più nota mutazione di Classe I, verosimilmente perché i pazienti con Classe I hanno accesso a terapie mirate consolidate mentre i pazienti con Classi II/III ricevono per lo più chemioterapia o immunoterapia standard.
Un farmaco di nuova generazione che colpisce l’intera via
BRAF fa parte di un relais di proteine (la via MAPK) che trasmette segnali di crescita dalla superficie cellulare al nucleo. Molti dei farmaci BRAF esistenti sono stati progettati per bloccare solo una forma mutata e possono persino stimolare involontariamente proteine correlate nelle cellule normali. Exarafenib è stato sviluppato in modo diverso: è un inibitore “pan‑RAF” progettato per spegnere diversi membri della famiglia RAF (ARAF, BRAF e CRAF) sia nelle forme monomeriche sia dimeriche, risparmiando la maggior parte delle altre chinasi cellulari. In test biochimici su centinaia di chinasi umane, exarafenib ha bloccato in modo marcato tutti e tre i RAF ma ha mostrato pochi effetti off‑target, suggerendo un profilo di sicurezza più pulito rispetto ai precedenti composti pan‑RAF.
Effetti potenti in modelli di tumori difficili da trattare
Il gruppo ha testato exarafenib in una batteria di linee cellulari e modelli murini che portavano diverse mutazioni di BRAF e RAS, inclusi tumori derivati da pazienti realistici. Nelle colture cellulari, exarafenib ha rallentato la crescita e spento la segnalazione MAPK non solo nelle classiche cellule tumorali BRAF V600E ma anche in quelle con mutazioni di Classe II e Classe III e in molte cellule mutate per RAS che attualmente non hanno buone opzioni mirate. Nei topi portatori di tumori polmonari con queste alterazioni, exarafenib ha ridotto o rallentato la crescita tumorale in modo dipendente dalla dose e ha mostrato chiare correlazioni tra livelli di farmaco, soppressione della via e risposta tumorale. Dati clinici preliminari da due pazienti con cancro polmonare avanzato BRAF‑mutato—uno con una rara fusione BRAF e un altro con una mutazione puntiforme di Classe II—hanno mostrato risposte parziali e sollievo sintomatico significativo, a sostegno della rilevanza del lavoro preclinico.
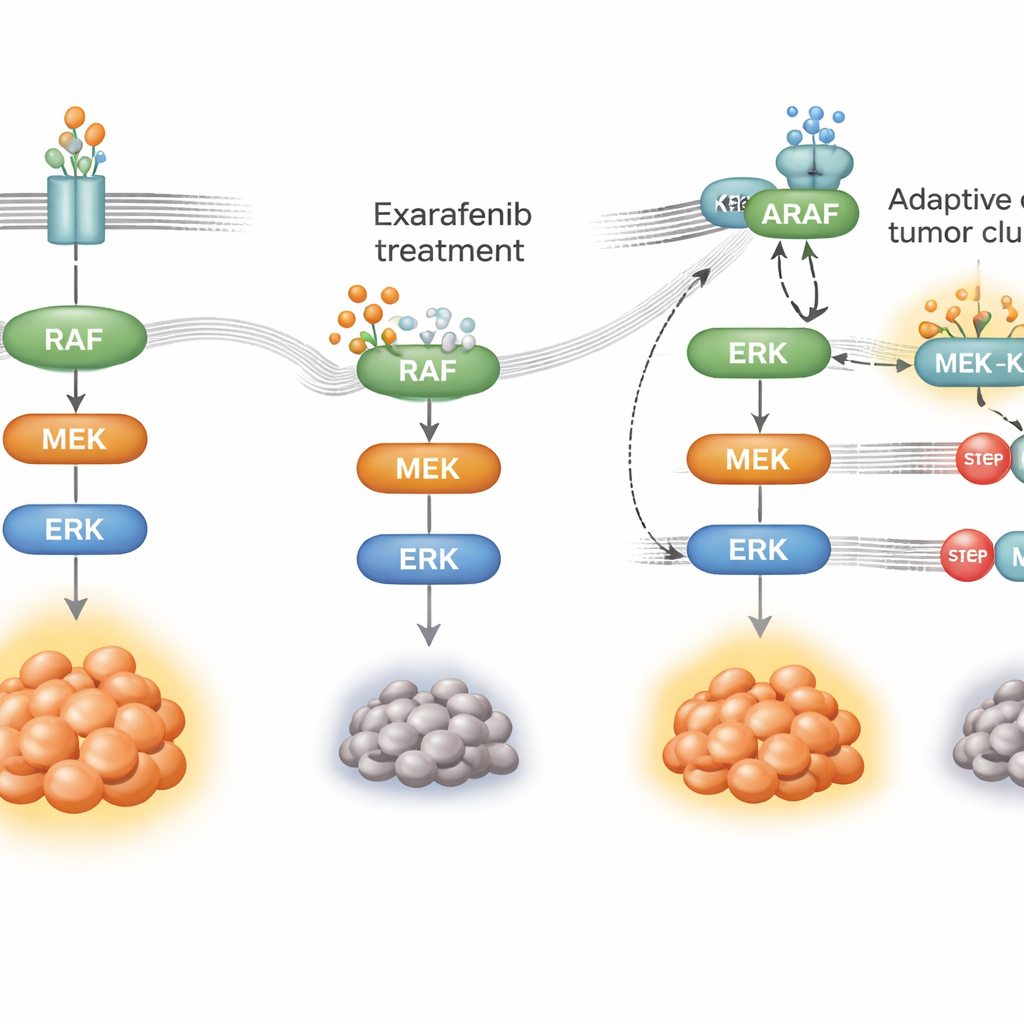
Come il cancro impara a eludere il farmaco
Nessuna terapia mirata funziona per sempre; le cellule tumorali si adattano. Per capire come i tumori possano resistere a exarafenib, i ricercatori hanno esposto cellule di carcinoma polmonare BRAF‑mutato al farmaco per mesi finché non sono emerse popolazioni resistenti. Queste cellule continuavano a dipendere dalla stessa via di crescita ma ne avevano riorganizzato l’uso. Invece di dipendere principalmente dal BRAF mutato, hanno aumentato l’attività di un interruttore a monte chiamato RAS e si sono spostate verso l’uso di un altro membro della famiglia, ARAF, insieme a una proteina impalcatura chiamata KSR1. Sotto la pressione del farmaco, ARAF e KSR1 formavano complessi stretti che aiutavano a mantenere attivo il relais MAPK anche mentre exarafenib era legato. Quando gli scienziati hanno silenziato selettivamente ARAF o KSR1, o hanno ridotto l’attività di RAS, le cellule resistenti sono tornate sensibili a exarafenib e i segnali di sopravvivenza sono crollati.
Strategie di combinazione per anticipare la resistenza
Armati di questa mappa meccanicistica, il team ha cercato farmaci partner che potessero bloccare la via in punti critici condivisi sia dalla rotta originale sia da quella di bypass. Hanno scoperto che associare exarafenib a farmaci che inibiscono MEK o ERK—passi chiave a valle nel relais MAPK—produceva forte sinergia in molti modelli cellulari e murini, inclusi tumori intrinsecamente meno sensibili o che avevano acquisito resistenza. Queste combinazioni mantenevano la via spenta più a lungo, scatenavano maggiore morte cellulare e negli animali spesso funzionavano tanto bene o meglio di dosi più elevate di exarafenib da solo, senza tossicità aggiuntiva evidente. Agenti che mirano direttamente a RAS hanno anche potenziato gli effetti di exarafenib in modelli in cui RAS guidava chiaramente la resistenza, suggerendo un’altra tattica clinicamente promettente.
Cosa significa per i pazienti
Per le persone con NSCLC portatori di mutazioni BRAF di Classe II o Classe III—o di complesse fusioni BRAF e co‑mutazioni RAS—attualmente non esistono terapie mirate approvate e i risultati sono inferiori rispetto a quelli dei pazienti con alterazioni più comuni. Questo studio fornisce una solida base scientifica che exarafenib potrebbe contribuire a colmare questa lacuna spegnendo in modo ampio la segnalazione guidata da RAF. Spiega inoltre come i tumori possano adattarsi tramite un bypass ARAF‑KSR1 e mostra che colpire la via a più livelli, in particolare combinando inibitori RAF e MEK o aggiungendo inibitori di RAS, potrebbe offrire un controllo tumorale più profondo e duraturo. Nel complesso, queste intuizioni tracciano un percorso verso studi clinici mirati a portare terapie mirate combinate e personalizzate a un ampio e precedentemente trascurato gruppo di pazienti con tumore polmonare.
Citazione: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Parole chiave: cancro polmonare BRAF-mutato, inibitore pan-RAF, segnalazione MAPK, resistenza ai farmaci, combinazioni di terapie mirate