Clear Sky Science · it
Ingegnerizzare un enzima citocromo P450 come perossigenasi per l’idrossilazione selettiva di steroidi
Produrre farmaci da molecole difficili da modulare
I farmaci steroidei — dalle compresse antinfiammatorie alle terapie ormonali — sono tra i medicinali più usati al mondo. Tuttavia perfezionare queste molecole, aggiungendo un singolo atomo di ossigeno nel punto esatto, è notoriamente difficile con la chimica tradizionale. Questo studio mostra come gli scienziati hanno riprogettato un enzima naturale in modo che possa “rifinire” con precisione le molecole steroidee usando il semplice perossido di idrogeno, aprendo potenzialmente percorsi più ecologici ed economici per importanti farmaci.
Perché gli steroidi sono così difficili da personalizzare
Gli steroidi sono costituiti da una pila compatta di anelli carboniosi, con molti legami carbonio–idrogeno quasi identici. I metodi chimici convenzionali faticano a colpire un solo di questi legami senza interessarne altri, spesso richiedendo reagenti aggressivi, alte temperature e molteplici passaggi di protezione che generano scarti. Eppure piccole modifiche — come l’aggiunta di un singolo gruppo ossidrile (–OH) in una posizione specifica — possono cambiare drasticamente il comportamento di uno steroide nell’organismo. Gli enzimi della famiglia del citocromo P450 sono gli specialisti naturali per questo tipo di attivazione selettiva dei legami C–H, ma nella loro forma naturale solitamente richiedono costosi cofattori e macchinari per la gestione dell’ossigeno, il che ne limita l’uso diretto in ambito produttivo.
Scoprire un enzima promettente come punto di partenza
Attraverso il genome mining, i ricercatori hanno identificato un P450 autosufficiente, chiamato P450stri, proveniente da un batterio del suolo. Diversamente dal classico enzima d’uso comune P450BM3, che preferisce acidi grassi piccoli, P450stri accetta naturalmente grandi molecole steroidee come il testosterone. Nelle sue condizioni native, alimentato dal cofattore cellulare NADH, P450stri introduce gruppi ossidrilici in tre posizioni del testosterone, producendo una miscela di prodotti. Questa capacità intrinseca di riconoscere gli steroidi ha reso P450stri uno “scheletro di partenza” attraente per l’ingegneria di un catalizzatore più selettivo e adatto all’industria.
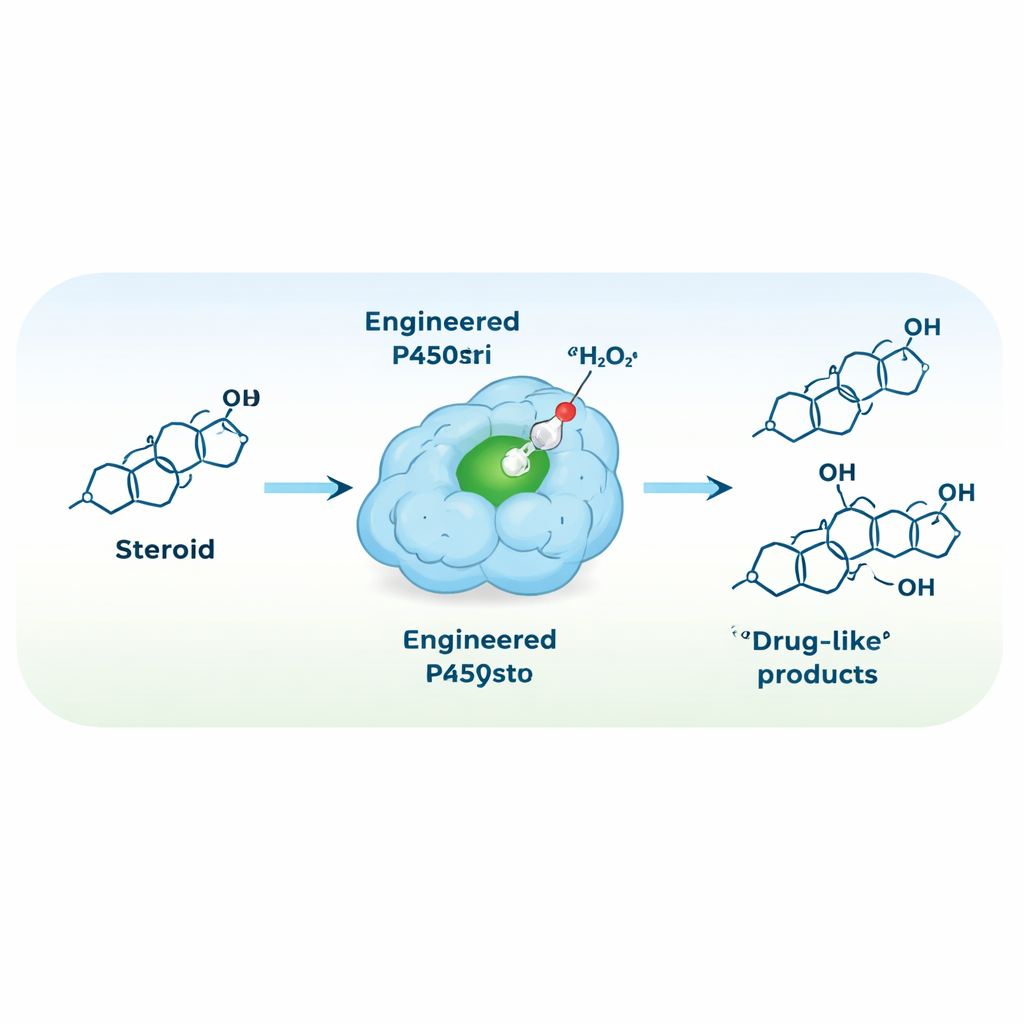
Riprogrammare l’enzima per funzionare con perossido di idrogeno
Per semplificare l’allestimento della reazione, il team ha cercato di convertire P450stri in una perossigenasi — un enzima che usa direttamente il perossido di idrogeno come ossidante, eliminando la necessità di cofattori costosi e proteine ausiliarie. Una singola mutazione strategica, che ha sostituito una voluminosa fenilalanina appena sopra il centro eme con un’alana più piccola, ha creato una variante chiamata M1. Questa modifica ha creato spazio intorno al centro ferro reattivo e, sorprendentemente, ha reso l’enzima sia più tollerante ad alte concentrazioni di perossido sia molto più selettivo. Nel nuovo regime guidato dal perossido, M1 ha convertito il testosterone principalmente in un unico prodotto, idrossilato nella posizione 15β, con circa il 94% di selettività — rispetto al 35% dell’enzima originale.
Un modello a “Fiasco” per progettare enzimi più intelligenti
Per spingere ulteriormente le prestazioni, gli autori hanno introdotto un concetto di progetto che chiamano modello “Fiasco”. Trattano il sito attivo dove avviene la chimica come la base arrotondata e i tunnel di accesso stretti come il collo e il tappo. La base determina quale posizione sullo steroide viene modificata, mentre il collo controlla quanto facilmente lo steroide e il perossido di idrogeno raggiungono il centro reattivo. Guidati da simulazioni al computer e da software di mappatura dei tunnel, hanno modificato in modo sistematico un piccolo insieme di amminoacidi che rivestono questi tunnel, sintonizzandone dimensione e idrofobicità. Questa strategia bidimensionale ha prodotto una variante notevole, M4, che ha mantenuto l’alta selettività per il 15β pur aumentando molto la velocità di reazione e tollerando concentrazioni di perossido di idrogeno fino a qualche centinaio di millimolare.
Dal banco di laboratorio a upgrade steroidei scalabili
L’enzima M4 ingegnerizzato è stato quindi testato in reazioni su scala maggiore con testosterone e uno steroide correlato usato in contesti di miglioramento delle prestazioni. In semplici miscele acquose a temperatura ambiente, alimentato solo dal perossido di idrogeno, M4 ha convertito oltre il 90% del materiale di partenza e ha fornito prodotti 15β-idrossilati isolati con rese intorno al 75–80%. Queste condizioni sono molto più miti e pulite rispetto alle vie chimiche tipiche. Infine, il team ha dimostrato che trapiantando le mutazioni chiave in diversi P450 correlati nello stesso ramo evolutivo, è stato possibile trasformarli in perossigenasi altrettanto selettive ed efficienti, evidenziando la generalità delle loro regole di progettazione.
Cosa significa questo per i futuri farmaci
Per un non specialista, il risultato principale è che i ricercatori hanno insegnato a un enzima naturale ad agire come una “microfabbrica” altamente precisa alimentata a perossido per modificare farmaci steroidei. Combinando un modello concettuale semplice con mutazioni mirate, hanno creato un enzima in grado di aggiungere un gruppo OH nel punto giusto, in condizioni dolci e scalabili, e poi hanno trasferito questa strategia a proteine correlate. Questo approccio potrebbe semplificare la produzione di steroidi esistenti, aprire vie verso nuovi candidati farmacologici e servire da schema per ingegnerizzare altri enzimi che attivano in modo selettivo legami C–H difficili in molecole complesse.
Citazione: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Parole chiave: biocatalisi degli steroidi, ingegneria del citocromo P450, perossigenasi, catalisi con perossido di idrogeno, idrossilazione selettiva