Clear Sky Science · it
Accoppiamento a catena sequenziale su siti click gerarchici permette elettrosintesi dell'urea altamente selettiva
Trasformare i rifiuti in nutrimento per le piante
I fertilizzanti a base di urea nutrono i raccolti in tutto il mondo, ma la loro produzione tradizionale brucia enormi quantità di combustibili fossili e rilascia vaste quantità di anidride carbonica. Questo studio esplora una strada diversa: usare elettricità — preferibilmente da fonti rinnovabili — per unire carbonio e azoto ricavati da gas di scarto e acque inquinate in nuove molecole di urea. Prendendo spunto dalla “click chemistry”, gli autori progettano un catalizzatore intelligente che collega questi ingredienti in modo pulito ed efficiente, indicando la via verso fertilizzanti più ecologici e un migliore utilizzo dei flussi di rifiuti industriali.

Perché ripensare la produzione di urea?
La produzione attuale di urea si basa su processi centenari ad alta temperatura e alta pressione che consumano fino al 2% dell’energia globale ed emettono più di una tonnellata di CO2 per ogni tonnellata di urea prodotta. Allo stesso tempo, centrali elettriche, stabilimenti e flussi di acque reflue rilasciano anidride carbonica e inquinamento da nitrati che spesso rimangono inutilizzati o causano danni ambientali. La sintesi elettrochimica dell’urea offre un modo per fare due cose insieme: ripulire CO2 e nitrati mentre si produce un fertilizzante prezioso a temperatura ambiente. Il problema è che, alle scale molecolari su una superficie metallica, i frammenti contenenti carbonio e azoto tendono a seguire percorsi differenti, formando molti sottoprodotti invece di unirsi ordinatamente nell’urea.
Una linea di assemblaggio molecolare ispirata alla click chemistry
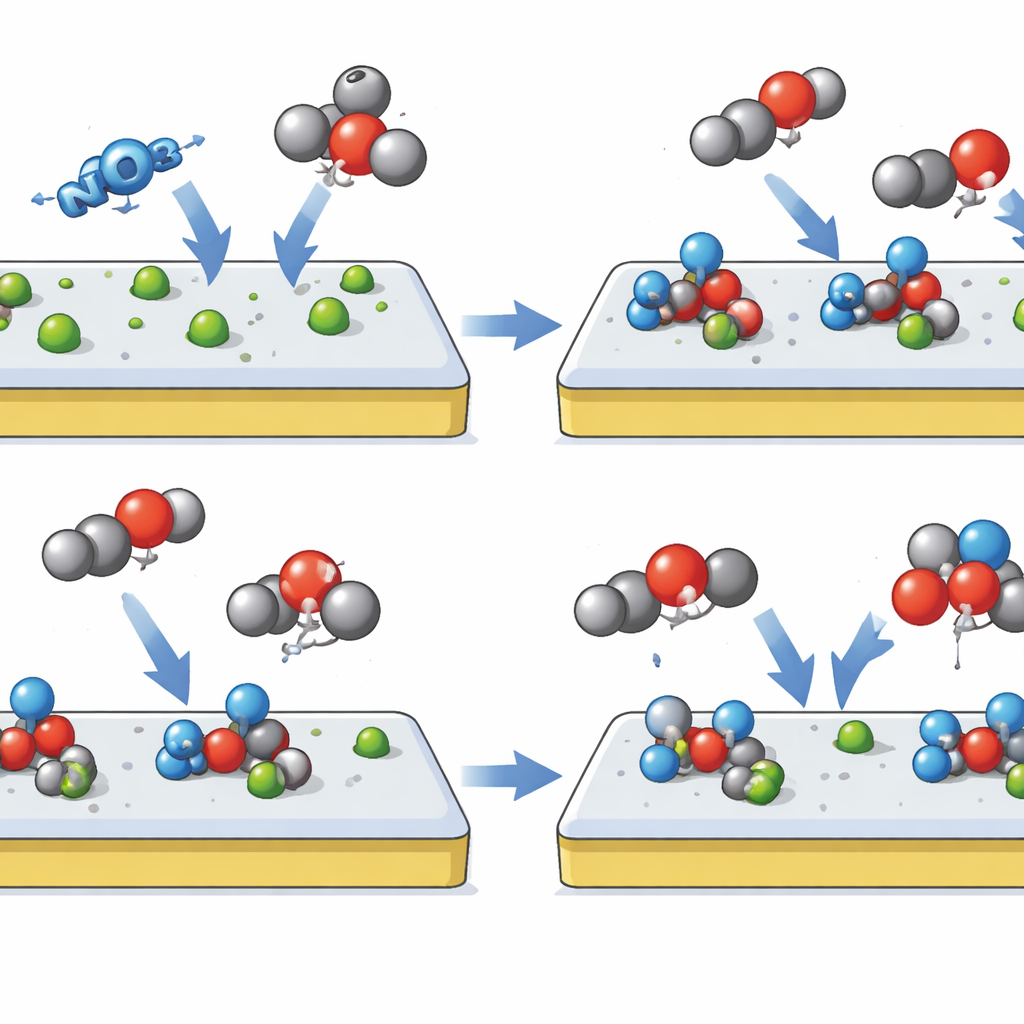
I ricercatori si ispirano alla click chemistry, un repertorio di reazioni apprezzato per collegare rapidamente e selettivamente pezzi molecolari con spreco minimo. Trasferiscono questa idea su una superficie elettrodica costruendo un catalizzatore a “siti click gerarchici” basato su ossido di indio leggermente modificato con il selenio, chiamato Se–InOx. Il progetto crea due stadi sequenziali sulla stessa superficie. Nel primo stadio, il catalizzatore preferisce nettamente catturare i nitrati dalla soluzione e convertirli in un frammento stabile simile al nitrito, rifiutando deliberatamente di legare il CO2 entrante. Nel secondo stadio, quel frammento di azoto ancorato diventa esso stesso un punto di aggancio che incoraggia il CO2 ad avvicinarsi e a connettersi, formando un intermedio chiave con legame carbonio‑azoto che conduce direttamente all’urea.
Come la superficie intelligente svolge il suo compito
Per rendere possibile questo comportamento, il team rimodella sottilmente il paesaggio elettronico dell’ossido di indio sostituendo una piccola frazione dei suoi atomi di ossigeno con il selenio. Questa modifica aumenta la densità elettronica locale e deforma la reticolazione cristallina quanto basta perché il CO2 trovi la superficie poco favorevole, mentre i nitrati e i loro prodotti simili al nitrito si legano più fortemente. Le simulazioni al computer mostrano che, su questa superficie ottimizzata, la formazione del cruciale legame carbonio‑azoto richiede meno energia e supera le reazioni collaterali che altrimenti convertirebbero i nitrati in ammoniaca o il CO2 in acido formico. Misure in situ sofisticate — sondando la superficie con luce infrarossa e risonanza magnetica durante la reazione — rilevano direttamente gli intermedi previsti, incluse le specie congiunte carbonio‑azoto, confermando la linea di assemblaggio passo dopo passo immaginata dai progettisti.
Prodotto più pulito e prestazioni solide
Testato in una cella elettrochimica a flusso, il catalizzatore Se–InOx produce urea sia rapidamente sia con alta purezza. In condizioni ottimali raggiunge una velocità di produzione di urea di circa 255 millimoli all’ora per grammo di catalizzatore e converte quasi il 79% della carica elettrica in urea, con più dell’85% dell’azoto e praticamente il 100% del carbonio nei prodotti che si ritrovano nell’urea anziché in sottoprodotti. I percorsi concorrenti che generano ammoniaca, acido formico o idrogeno sono fortemente soppressi. Il catalizzatore mantiene la sua struttura e attività attraverso cicli ripetuti e in una cella ingrandita da 5 × 5 cm che funziona in continuo per 20 ore, producendo oltre un grammo di urea solida che supera i controlli di purezza mediante risonanza magnetica nucleare.
Costi, impatto climatico e promesse future
Oltre alle prestazioni di laboratorio, gli autori valutano se questo approccio possa avere senso economico e ambientale su scala più ampia. La loro analisi suggerisce che, se alimentata da elettricità rinnovabile a basso costo e ulteriormente migliorata in efficienza, l’urea elettrochimica potrebbe avvicinarsi o addirittura sottocostare i prezzi di mercato attuali, specialmente quando anche i sottoprodotti assumono valore. Una valutazione del ciclo di vita mostra che l’uso di elettricità a bassa intensità di carbonio può ridurre le emissioni di gas serra per chilogrammo di urea al di sotto di quelle della via convenzionale. In termini semplici, questo lavoro dimostra che superfici accuratamente progettate in stile “click” possono orchestrare l’incontro tra carbonio e azoto di scarto, trasformando un problema di inquinamento in una soluzione fertilizzante e offrendo un modello per una produzione più pulita di altri prodotti chimici complessi.
Citazione: Sun, Y., Tian, M., Wu, Q. et al. Sequential-chain coupling over hierarchical click-sites enables highly selective urea electrosynthesis. Nat Commun 17, 2388 (2026). https://doi.org/10.1038/s41467-026-69207-4
Parole chiave: sintesi elettrochimica dell'urea, utilizzo della anidride carbonica, riduzione dei nitrati, catalisi eterogenea, concime verde