Clear Sky Science · it
Biologia strutturale a cellula singola con cristallografia elettronica intracellulare
Osservare la forma della vita, una cellula alla volta
Le proteine sono le piccole macchine che mantengono viva ogni cellula, ma per comprendere davvero come funzionano gli scienziati devono vedere le loro forme tridimensionali con grande precisione. Tradizionalmente ciò ha significato purificare enormi quantità di proteina e far crescere grandi e fragili cristalli al di fuori della cellula—spesso un processo lento e soggetto a insuccessi. Questo studio presenta un nuovo modo per leggere la struttura proteica direttamente da un singolo cristallo all’interno di una singola cellula, usando elettroni invece dei raggi X. Indica un futuro in cui la biologia strutturale ad alta risoluzione potrà essere svolta in laboratori ordinari e persino a livello di singole cellule.
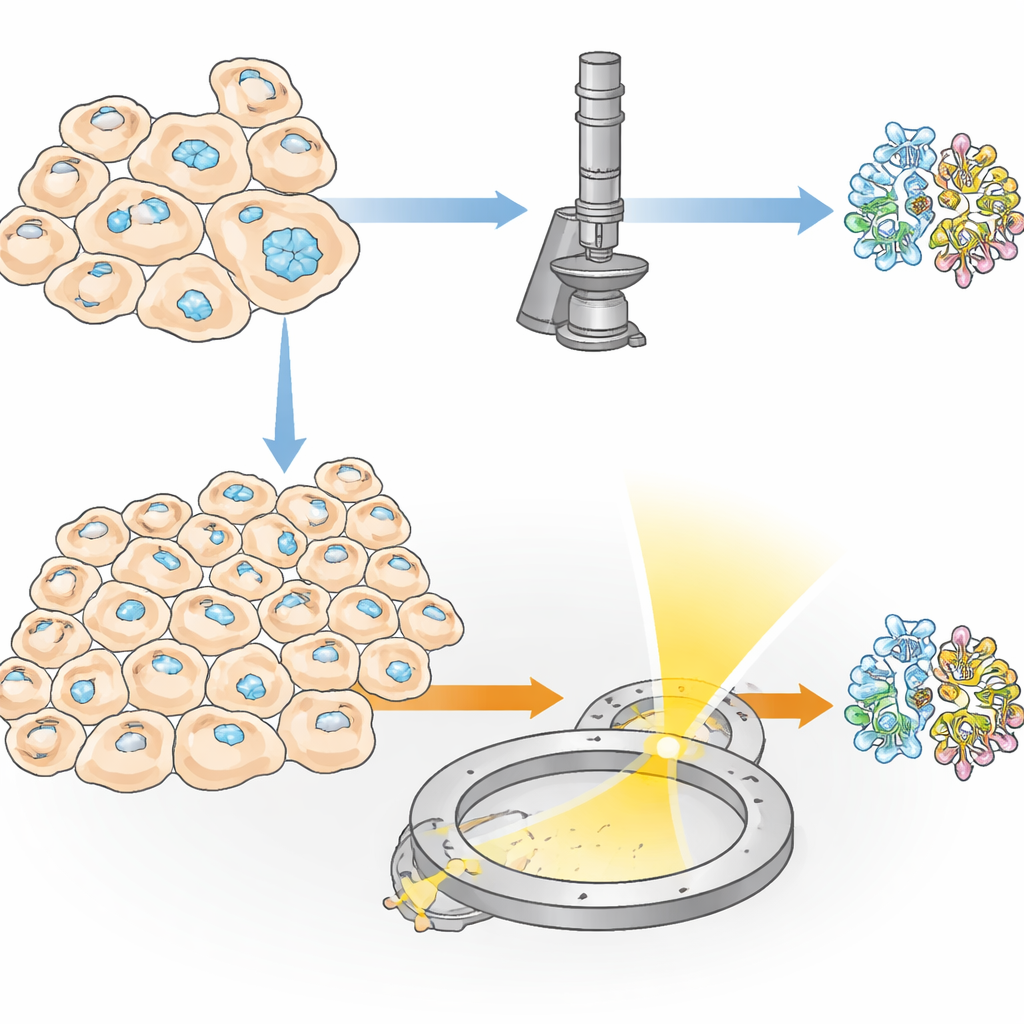
Cristalli nascosti all’interno delle cellule viventi
Alcune proteine si aggregano naturalmente in piccoli cristalli all’interno delle cellule vive, svolgendo funzioni come immagazzinamento, protezione o aiutare le cellule a rispondere allo stress. I ricercatori possono anche indurre le cellule a produrre tali cristalli ingegnerizzandole per sintetizzare grandi quantità di una proteina scelta. Questa cristallizzazione “in cellulo” ha due grandi vantaggi: la proteina non lascia mai un ambiente simile a quello naturale, e caratteristiche delicate—come decorazioni zuccherine o piccole molecole legate—possono essere preservate in modi che spesso falliscono nella cristallizzazione in provetta standard. Tuttavia, è rimasto un ostacolo importante: in molti esperimenti solo una piccolissima frazione di cellule forma cristalli, quindi i metodi tradizionali a raggi X richiedono decine di migliaia di cristalli e, di conseguenza, un numero enorme di cellule.
Una nuova via: elettroni invece dei raggi X
Gli autori introducono un metodo che chiamano IncelluloED, che combina la cristallizzazione in cellulo con la diffrazione elettronica tridimensionale. Gli elettroni interagiscono molto più fortemente con la materia rispetto ai raggi X, il che significa che è possibile raccogliere dati utili da cristalli sia più piccoli sia in numero inferiore. Il team ha scelto una proteina fungina chiamata HEX-1, che normalmente forma cristalli esagonali che aiutano a tappare piccoli pori tra le cellule fungine sotto stress. Prodotte all’interno di cellule di insetto, queste proteine hanno dato cristalli microscopici regolari che hanno servito come caso di prova per la nuova pipeline.
Trasformare un cristallo in una mappa dettagliata
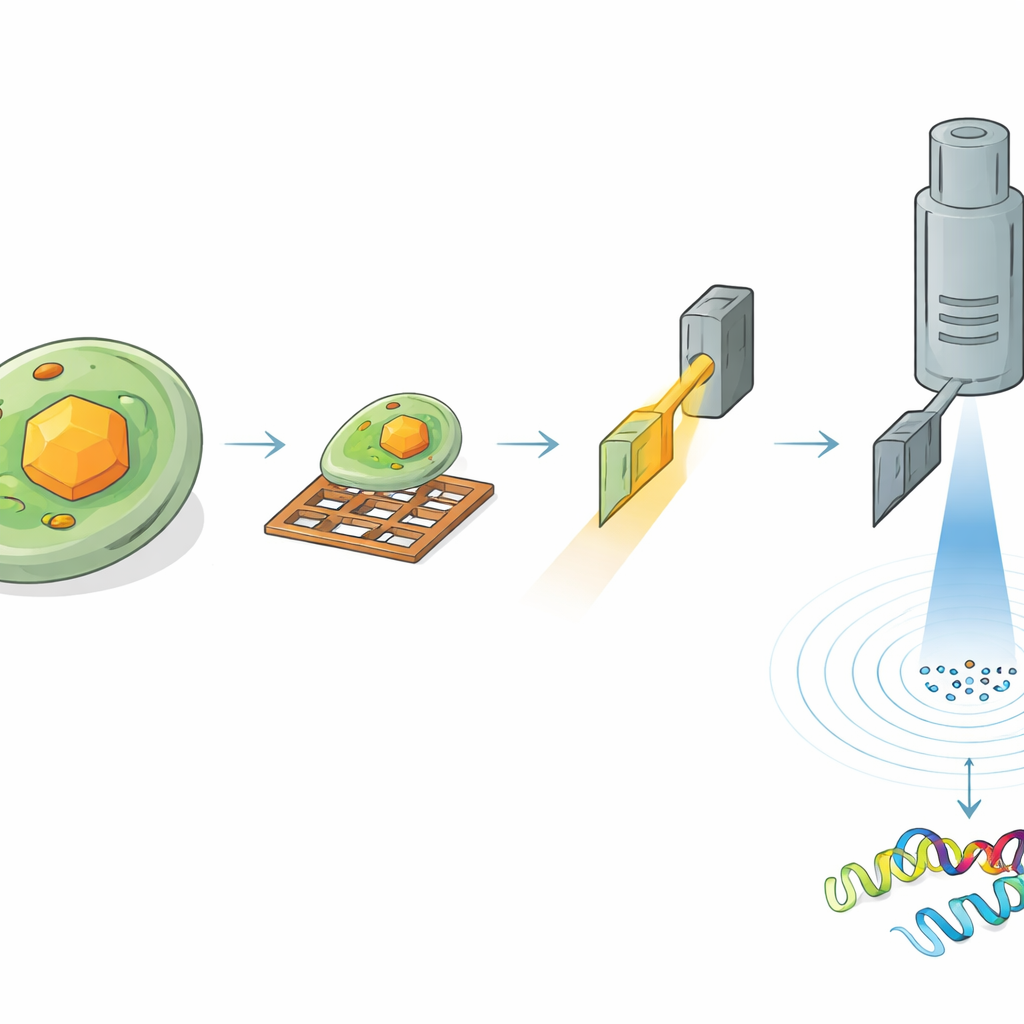
Per leggere la struttura di HEX-1 all’interno di una cellula, i ricercatori hanno dovuto trovare e assottigliare con cura la regione giusta del campione. Per prima cosa hanno congelato le cellule contenenti cristalli su piccole griglie metalliche e rivestito la superficie con un sottile strato di platino. Usando microscopia a luce criogenica, hanno scandito ampie aree della griglia per individuare le cellule con cristalli e misurare le posizioni tridimensionali dei cristalli sotto la superficie. Poi hanno trasferito lo stesso campione in uno strumento specializzato che combina un microscopio elettronico a scansione con un fascio ionico focalizzato. Guidati dalle immagini di luce precedenti, hanno asportato il materiale circostante per ricavare una fetta ultra-sottile, o lamella, che attraversa un cristallo scelto, spessa solo poche centinaia di nanometri—ideale per il passaggio degli elettroni.
Gli elettroni rivelano dettagli atomici da volumi microscopici
Le lamelle preparate sono state poi trasferite in un microscopio elettronico di alta gamma operante a temperature criogeniche. Mentre la fetta di cristallo veniva ruotata lentamente nel microscopio, un fascio di elettroni finemente controllato la attraversava, creando una serie di pattern di diffrazione—delicati arrangiamenti di punti che codificano le posizioni degli atomi. Da un volume di cristallo di circa 1,6 micrometri cubi, il team ha ricostruito l’intera struttura 3D di HEX-1 a 1,9 ångström di risoluzione, abbastanza nitida da modellare la maggior parte delle catene laterali della proteina. Volumi ancora più piccoli, di circa 0,8 micrometri cubi, hanno fornito una struttura quasi identica a risoluzione solo leggermente inferiore. È importante che i modelli risultanti corrispondessero strettamente a quelli ottenuti con un approccio seriale a raggi X convenzionale che richiedeva oltre 60.000 cristalli e un volume totale di cristalli approssimativamente sette milioni di volte maggiore.
Come questo cambia il campo della biologia strutturale
Confronti affiancati hanno mostrato che la struttura determinata da un singolo cristallo ottenuto con diffrazione elettronica in cellulo è essenzialmente la stessa di quella mediata da decine di migliaia di cristalli con i raggi X. Le differenze riscontrate erano minori e per lo più confinate a anse flessibili, dove è previsto un moto naturale. I ricercatori hanno anche dimostrato che le dosi di elettroni usate erano sufficientemente basse da evitare danni da radiazione significativi, e che ogni cristallo processato ha prodotto dati di alta qualità. Sebbene la preparazione delle lamelle sottili richieda ancora abilità e tempo, gli strumenti necessari—microscopi a luce criogenica, sistemi a fascio ionico focalizzato e microscopi elettronici criogenici—sono ormai diffusi in molti centri di ricerca.
Da molte cellule a un laboratorio strutturale a cellula singola
Questo lavoro dimostra che ora è possibile determinare la struttura atomica di una proteina a partire da un solo cristallo all’interno di una sola cellula, senza mai purificare la proteina. IncelluloED potrebbe rivelarsi particolarmente potente quando solo poche cellule formano cristalli, o quando le proteine sono difficili da isolare senza perdere partner importanti o gruppi chimici. Man mano che il flusso di lavoro diventerà più automatizzato e sarà esteso ad altre proteine, potrà permettere ai ricercatori di esplorare come le strutture varino da cellula a cellula, studiare i cambiamenti legati a malattie nel loro contesto nativo e persino supportare la scoperta di farmaci direttamente nelle cellule viventi. Di fatto, lo studio avvicina molto la visione di un “laboratorio strutturale a cellula singola” alla realtà.
Citazione: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Parole chiave: diffrazione elettronica, cristallografia in cellulo, biologia strutturale a cellula singola, struttura proteica, cryo-EM