Clear Sky Science · it
14-3-3ζ interagisce con il dominio legante il DNA di FOXO3a e dissocia competitivamente il DNA mediante un ancoraggio a doppio motivo
Come le cellule tumorali spengono il proprio interruttore di autodistruzione
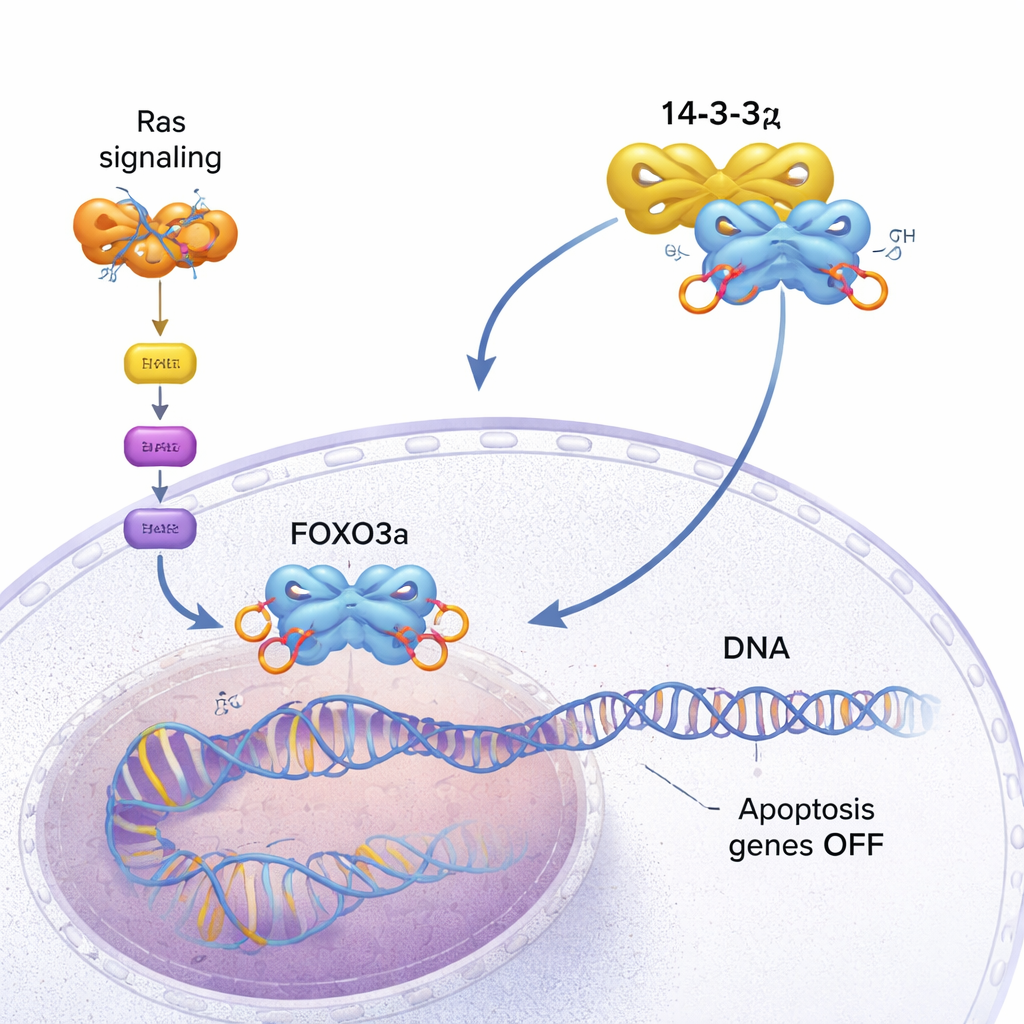
Le nostre cellule possiedono sistemi di sicurezza integrati che possono innescare la loro morte quando diventano troppo danneggiate o pericolose. Uno di questi sistemi è controllato da una proteina chiamata FOXO3a, che attiva geni che inducono le cellule ribelli al suicidio. Molti tumori, tuttavia, trovano modi per mettere a tacere FOXO3a e continuare a crescere. Questo studio indaga i dettagli molecolari di come un’altra proteina, 14-3-3ζ, aiuti le cellule tumorali a staccare FOXO3a dal DNA e a disattivare questo interruttore di autodistruzione.
La proteina guardiana che contrasta il cancro
FOXO3a funziona come un ispettore di sicurezza per la cellula. Si lega a siti specifici sul DNA e attiva geni che rallentano la crescita o innescano la morte programmata della cellula (apoptosi) quando qualcosa va storto. Nelle cellule sane questo aiuta a prevenire la formazione di tumori. In molti tumori, però, una via di segnalazione pro‑crescita guidata da proteine Ras mutate resta permanentemente attivata. Questa via attiva una chinasi chiamata AKT, che marca chimicamente FOXO3a in più siti con gruppi fosfato. Questi marker creano punti di aggancio per 14-3-3ζ, una proteina “adattatrice” dimera che riconosce motivi fosforilati su vari bersagli. Quando 14-3-3ζ si aggancia a FOXO3a, i freni interni della cellula cominciano a cedere.
Perché la semplice forza di legame non poteva spiegare l’effetto
Lavori precedenti su una proteina correlata, FOXO4, avevano suggerito che le proteine 14-3-3 rimuovessero i fattori FOXO dal DNA semplicemente perché si legano più saldamente. Ma FOXO3a preferisce i suoi target naturali sul DNA più fortemente di quanto il modello precedente supponesse. In questo studio i ricercatori hanno prodotto una versione di FOXO3a che include il dominio legante il DNA e due siti chiave di fosforilazione. Hanno misurato quanto saldamente questa proteina si lega al DNA o a 14-3-3ζ e hanno scoperto che le differenze nella forza di legame erano modeste: 14-3-3ζ era solo circa il doppio più forte come partner rispetto al DNA. Eppure, in esperimenti misti che tracciano come le molecole viaggiano attraverso una colonna cromatografica, 14-3-3ζ è stato in grado di causare un rilascio quasi completo del DNA da FOXO3a, come se fosse circa 100 volte più competitivo di quanto previsto. Questo disallineamento suggeriva che fosse in gioco un meccanismo aggiuntivo.
Una presa a tre punti che mette in ombra il DNA
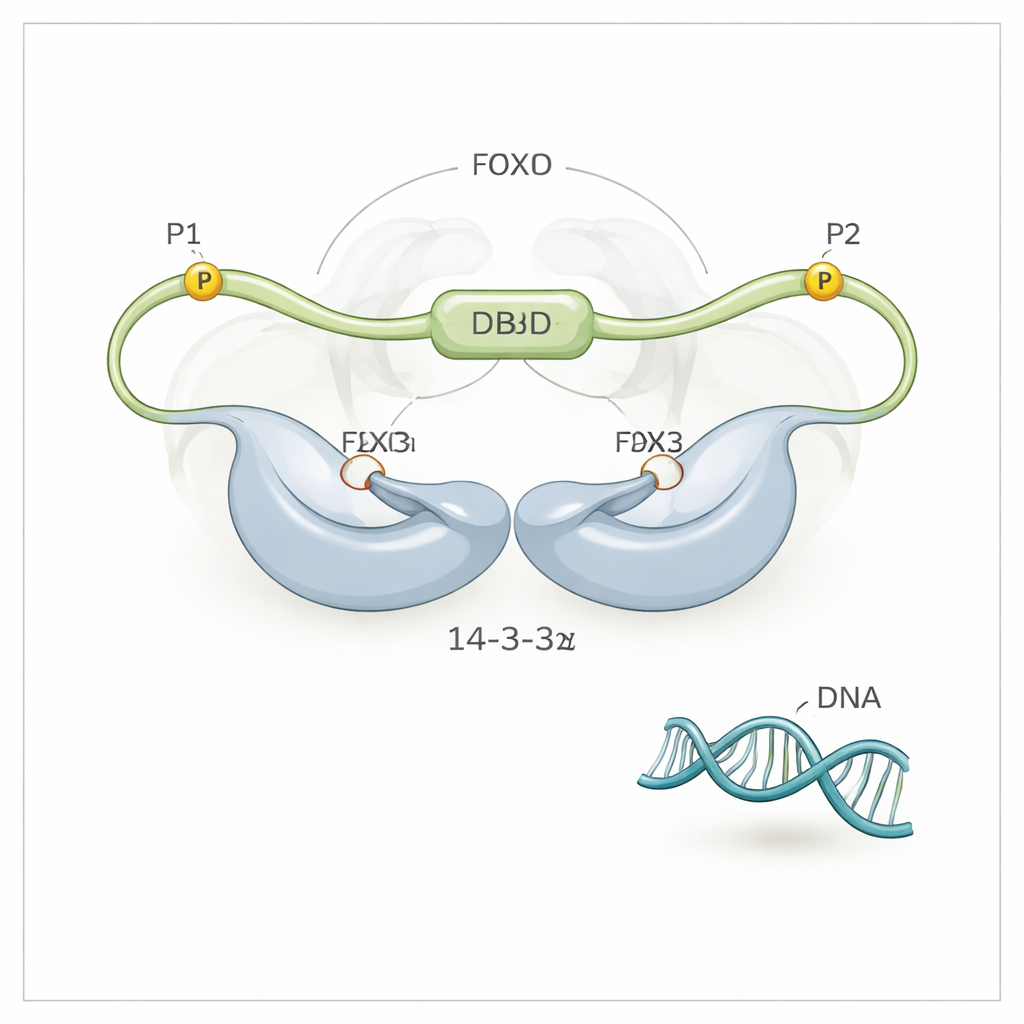
Usando spettroscopia NMR ad alta risoluzione, il gruppo ha scoperto che 14-3-3ζ fa più che afferrare FOXO3a nei suoi due motivi fosforilati (detti P1 e P2). Stabilisce anche un contatto diretto, seppur più debole, con il dominio legante il DNA (DBD) di FOXO3a — la stessa superficie che normalmente si abbraccia al DNA. La proteina 14-3-3ζ forma un dimero simmetrico con due scanalature. Ciascuna scanalatura si aggrappa a uno dei motivi fosforilati su FOXO3a, ancorando FOXO3a a 14-3-3ζ in due punti. Poiché uno di questi motivi (P2) è molto vicino lungo la catena al dominio legante il DNA, questo “ancoraggio a doppio motivo” mantiene di fatto 14-3-3ζ proprio accanto al DBD, incrementando notevolmente la probabilità che il DBD urti e si leghi alla superficie di 14-3-3ζ invece che al DNA. I ricercatori hanno persino osservato che il DBD oscilla tra i due lati del dimero di 14-3-3ζ, trascorrendo la maggior parte del tempo schermato dal DNA.
Quali tag fosfato contano di più
Per separare i ruoli dei due siti fosforilati, il team ha ingegnerizzato varianti di FOXO3a in cui solo un sito poteva essere fosforilato alla volta. Quando era attivo solo il sito P2 vicino al DBD, 14-3-3ζ poteva scalfire parzialmente il DNA ma non rimuoverlo completamente. Quando era attivo solo il sito più distante P1, 14-3-3ζ poteva legarsi a FOXO3a ma influenzava appena la sua presa sul DNA. Il rilascio completo del DNA richiedeva entrambi i siti: P1 fornisce un punto di aggancio iniziale ad alta affinità per 14-3-3ζ, e P2 posiziona il dimero abbastanza vicino al DBD da rendere la concentrazione locale di 14-3-3ζ effettivamente enorme in quel punto. Questo ancoraggio multistep amplifica una preferenza di legame modesta in una potente capacità di espellere il DNA.
Dal tiro alla fune molecolare a nuove idee farmacologiche
Per il non specialista, il messaggio chiave è che le cellule tumorali sfruttano un espediente di geometria molecolare, non solo la forza bruta del legame, per silenziare una proteina oncosoppressiva importante. 14-3-3ζ usa due piccoli tag di aggancio su FOXO3a come punti di ancoraggio, poi si protende per coprire la superficie di FOXO3a che impugna il DNA, impedendole di attivare i geni della morte cellulare. Poiché le stesse famiglie FOXO e 14-3-3 sono ampiamente usate in molti tessuti, questa strategia di doppio ancoraggio è probabilmente comune anche in altri tumori. Interferire con gli ancoraggi dipendenti dal fosfato o con il contatto più debole con la faccia legante il DNA di FOXO3a potrebbe ripristinarne la capacità di attivare i programmi di autodistruzione nelle cellule tumorali, offrendo promettenti nuovi spunti per la progettazione di farmaci anticancro.
Citazione: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Parole chiave: FOXO3a, proteine 14-3-3, apoptosi, segnalazione Ras–AKT, terapie antitumorali