Clear Sky Science · it
Meccanismi molecolari dei complessi di flotillina nell’organizzazione dei microdomini di membrana
Stanze nascoste sulla superficie cellulare
Ogni cellula del tuo corpo è avvolta da una sottile membrana che a prima vista sembra semplice ma in realtà è suddivisa in innumerevoli minuscoli “quartieri”. Questi quartieri controllano come vengono ricevuti i segnali, come entrano i nutrienti e come viene espulso il materiale di scarto. Questo studio svela come una coppia di proteine a lungo enigmatiche, chiamate flotilline, costruisca miniature stanze protette sul lato interno della membrana—strutture che possono influenzare processi tanto diversi quanto la trasmissione del segnale, il trasporto di carico e persino la diffusione del cancro. 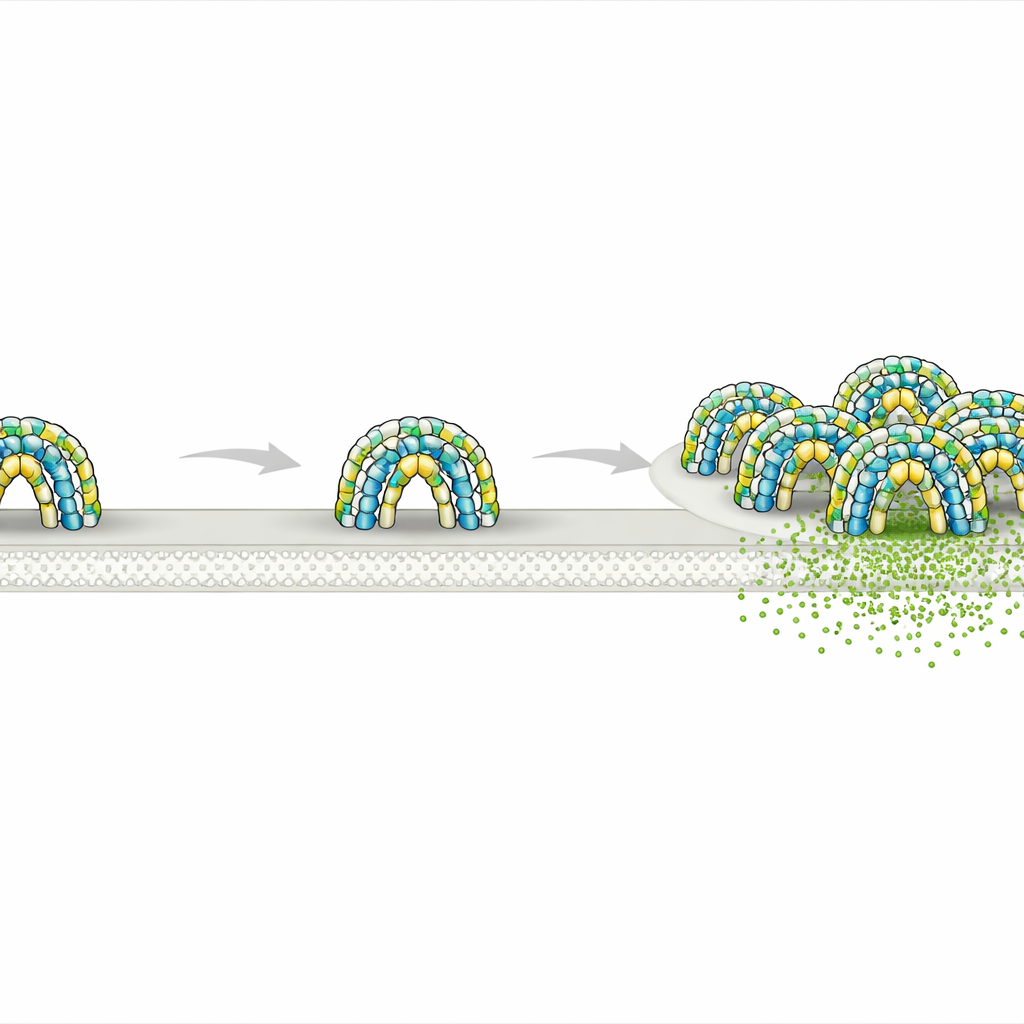
Uno sguardo ravvicinato ai minuscoli quartieri di membrana
I biologi sanno da tempo che le membrane cellulari non sono uniformi. Invece, lipidi e proteine si raggruppano in piccole patch che funzionano come postazioni di lavoro temporanee per compiti specifici come la comunicazione o l’ordinamento del carico. Flotillina‑1 e flotillina‑2 sono due proteine che sembrano sempre segnare queste patch, formando piccoli punti luminosi sulla superficie cellulare e partecipando all’endocitosi—il processo con cui le cellule richiamano materiale verso l’interno—oltre che alla segnalazione e al traffico proteico. Tuttavia nessuno sapeva quale forma assumessero concretamente le strutture di flotillina, né come si ritagliassero il proprio territorio sulla membrana.
Dome che recintano cerchi di membrana
Utilizzando crio‑microscopia elettronica ad alta risoluzione su proteine umane purificate, i ricercatori hanno scoperto che flotillina‑1 e flotillina‑2 si assemblano in un complesso sorprendentemente grande composto da 44 copie proteiche, alternate tra i due tipi. Insieme formano una cupola rigida posta sulla faccia interna della membrana. La base di questa cupola è costruita da segmenti di ancoraggio alla membrana ricchi di amminoacidi idrofobici e di attacchi lipidici che si insinuano parzialmente nella membrana. Sopra di questi, lunghi steli elicoidali formano una parete compatta simile a un barile, e un tetto di segmenti proteici incastrati completa la struttura. L’anello di flotillina alla base definisce una patch circolare di membrana di circa 30 nanometri di diametro—essenzialmente recintando un piccolo disco di membrana e lo spazio immediatamente sopra di esso.
Cupole flessibili osservate all’interno di cellule vive
Per verificare se queste cupole esistono nelle cellule reali, il team ha ingegnerizzato cellule T umane affinché producessero flotillina‑1 e flotillina‑2 con etichette fluorescenti e le ha poi imaged tramite una combinazione di microscopia ottica e crio‑tomografia elettronica. Hanno osservato strutture cave a forma di cupola attaccate alla superficie interna della membrana plasmatica, che corrispondevano da vicino alla forma determinata nei campioni purificati. Molte cupole apparivano leggermente deformate o parzialmente aperte, e alcune contenevano densità aggiuntive all’interno, probabilmente rappresentanti altre proteine temporaneamente intrappolate sotto il tetto. In alcune regioni più cupole si raggruppavano insieme su membrane piatte o curve, inclusi endosomi e piccole vescicole extracellulari, suggerendo che singole cupole possano unirsi per formare piattaforme di membrana più grandi. 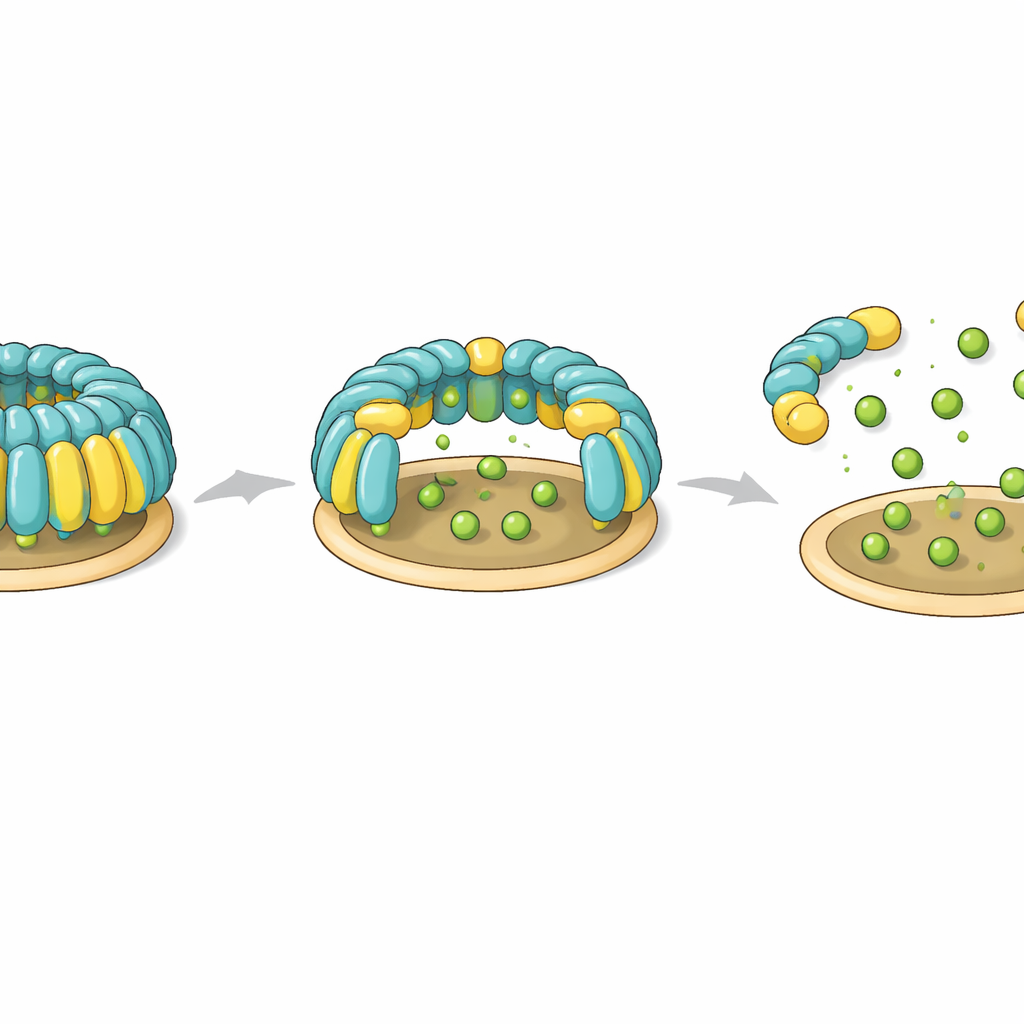
Un interruttore molecolare per costruire e smontare le cupole
Lo studio identifica anche una potenziale manopola di controllo che le cellule potrebbero usare per assemblare o smantellare le cupole di flotillina. Due residui di tirosina specifici—uno su ciascuna proteina di flotillina—si trovano in posizioni simili a cerniere che collegano la base ancorata alla membrana alla parete elicoidale. Nel complesso integro, questi residui contribuiscono a formare un nucleo idrofobico compatto che blocca l’orientamento dei domini. Quando i ricercatori hanno introdotto mutazioni che imitano l’aggiunta di carica negativa, come avverrebbe quando enzimi fosforilano queste tirosine, l’intera cupola non si è assemblata. Mutazioni non cariche hanno lasciato l’assemblaggio intatto. Queste osservazioni suggeriscono che la fosforilazione in questi punti di cerniera potrebbe agire come un interruttore reversibile che destabilizza la cupola, aprendola o frammentandola durante processi come l’endocitosi dipendente da flotilline.
Ridefinire come questi domini modellano la membrana
Le patch di flotillina erano state una volta considerate principalmente come “raft lipidici” ricchi di colesterolo e grassi correlati. Sorprendentemente, quando il team ha esaminato grosse bolle di membrana staccate dalle cellule, le flotilline preferivano le regioni più fluide, non‑raft, piuttosto che quelle rigide e dense di colesterolo. L’analisi lipidica ha mostrato solo un modesto arricchimento di una molecola particolare, la sfingosina, all’interno dei complessi di flotillina, mentre altri lipidi associati ai raft non risultavano concentrati. Questo suggerisce un principio organizzativo diverso: invece di essere passeggeri su raft lipidici preesistenti, le cupole di flotillina fungono esse stesse da contenitori strutturali che segregano lateralmente porzioni di membrana, catturando determinate proteine e lipidi nella loro area recintata.
Perché questa minuscola architettura è importante
In termini pratici, i complessi di flotillina si comportano come tende modulari che le cellule possono dispiegare sulla loro superficie interna per delimitare piccoli lotti circolari di membrana. Ogni cupola può ospitare una miscela distinta di proteine partner e lipidi e, raggruppandosi con altre, può costruire zone funzionali più estese per la segnalazione, l’ordinamento del carico o la formazione di vescicole. Poiché le cupole sono flessibili e sembrano aprirsi e chiudersi, e poiché il loro assemblaggio è sensibile alla fosforilazione, le cellule possono rimodellare dinamicamente queste strutture in risposta a segnali. Questo lavoro quindi ricolloca le flotilline dall’essere vaghi “marcatori di raft” a elementi architettonici concreti che contribuiscono a plasmare la membrana in micro‑spazi di lavoro specializzati.
Citazione: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Parole chiave: flotillina, microdomini di membrana, crio-microscopia elettronica, endocitosi, raft lipidici