Clear Sky Science · it
La sopravvivenza dei macrofagi residenti nei tessuti dipende dalla funzione mitocondriale regolata da SerpinB2 nell’infiammazione cronica
Perché contano le cellule immunitarie del grasso
La maggior parte delle persone considera il grasso corporeo come un deposito passivo, ma in realtà è un tessuto animato pieno di cellule immunitarie che aiutano a controllare l’infiammazione e la glicemia. Questo studio rivela come un gruppo specifico di cellule immunitarie a lunga vita nel grasso addominale profondo agisca da guardiano contro il diabete di tipo 2 — e come l’infiammazione cronica nell’obesità le elimini silenziosamente danneggiando i loro piccoli impianti energetici, i mitocondri.
Due tipi di guardiani del grasso
Il tessuto adiposo viscerale — il grasso che circonda gli organi interni — contiene due principali tipi di cellule immunitarie chiamate macrofagi. Un tipo è a vita breve e viene costantemente rifornito dal sangue; questi macrofagi “infiammatori” tendono ad alimentare il gonfiore e la resistenza all’insulina. L’altro tipo è a lungo termine, residente nel tessuto, nasce precocemente nella vita e normalmente contribuisce a mantenere il tessuto calmo, supportare un deposito di grasso sano e promuovere la sensibilità all’insulina a livello dell’intero organismo. Seguendo queste cellule nei topi e confrontando l’attività genica, i ricercatori hanno dimostrato che i macrofagi residenti sono arricchiti in geni antinfiammatori e che favoriscono la sensibilità all’insulina, mentre i macrofagi derivati dai monociti in ingresso esprimono geni che peggiorano il controllo della glicemia.
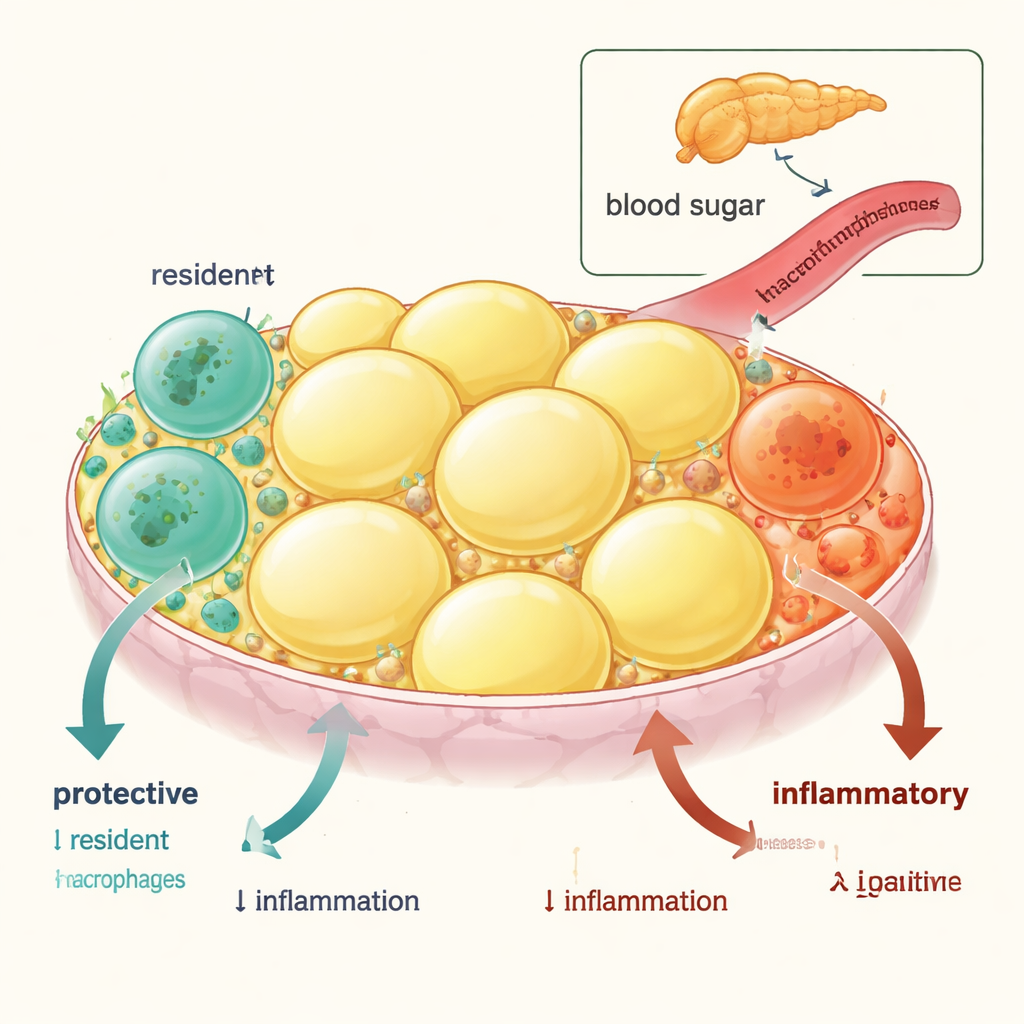
Quando l’infiammazione elimina i buoni
Nell’obesità questo equilibrio protettivo cambia. Il gruppo ha scoperto che sia nei topi obesi sia negli individui obesi o diabetici il numero di macrofagi residenti nel grasso viscerale diminuisce, mentre i macrofagi infiammatori aumentano. Immagini dettagliate e marcatori della morte cellulare hanno rivelato il perché: i macrofagi residenti vanno più spesso incontro a morte programmata (apoptosi), mentre le cellule infiammatorie no. È notevole che, quando i topi obesi sono stati tolti da una dieta ricca di grassi, la popolazione residente si è lentamente ripristinata tramite proliferazione locale e la salute metabolica è migliorata — a mostrare che questa perdita è guidata dallo stato infiammatorio e può essere reversibile.
Una singola proteina collega i mitocondri alla sopravvivenza
Un indizio chiave è stata una proteina chiamata SerpinB2, nota soprattutto per ruoli nella coagulazione del sangue. I ricercatori hanno scoperto che SerpinB2 è prodotta a livelli molto elevati all’interno dei macrofagi residenti, ma molto meno in quelli infiammatori. Negli umani e nei topi obesi, i macrofagi residenti riducevano drasticamente l’espressione di SerpinB2, e un indice di massa corporea più alto era associato a meno cellule positive per SerpinB2. Esperimenti in cellule prive di SerpinB2 hanno mostrato una maggiore fuoriuscita di citocromo c — una proteina cruciale — dai mitocondri al citoplasma, un classico innesco dell’apoptosi. Questi macrofagi privi di SerpinB2 avevano difese antiossidanti ridotte, più specie reattive dell’ossigeno (ROS) mitocondriali e un consumo di ossigeno più elevato: tutti segnali di mitocondri stressati e sovraccarichi che spingono le cellule verso un comportamento infiammatorio e la morte.
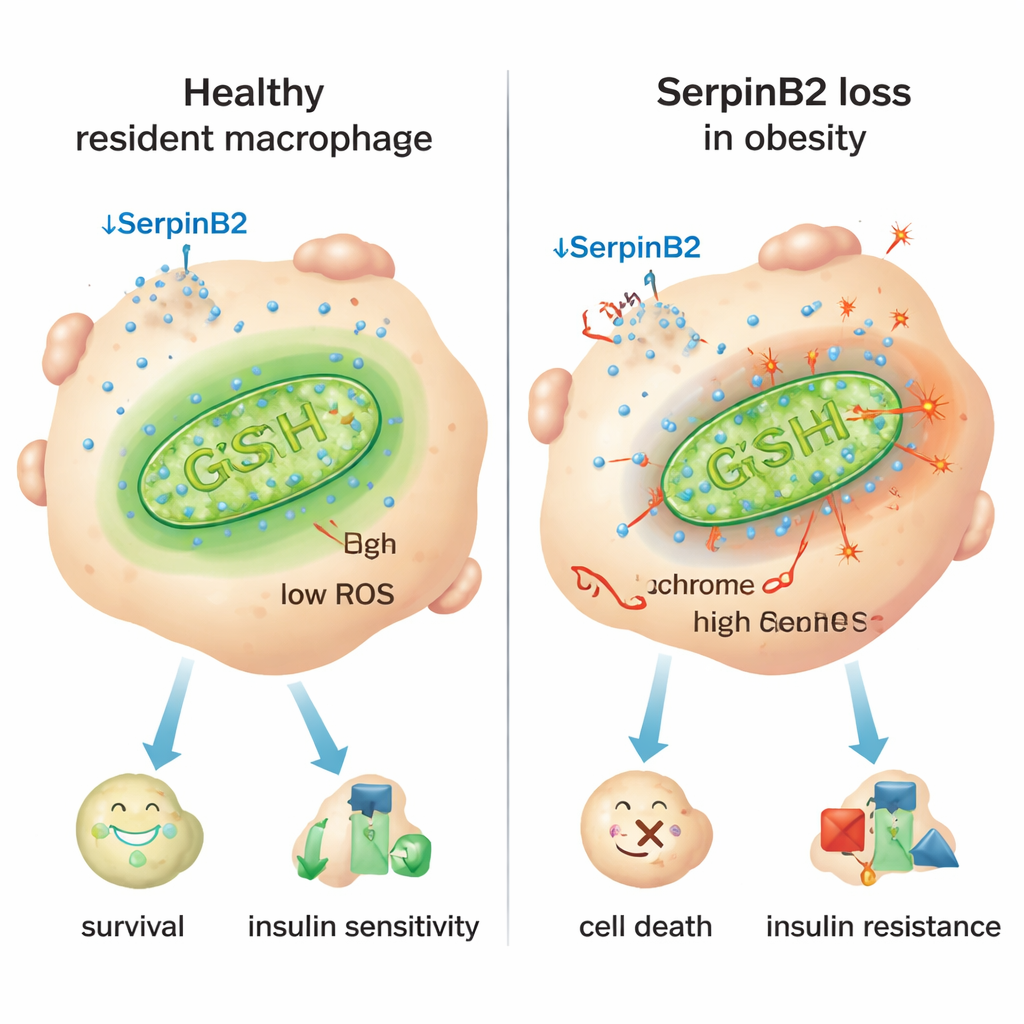
Interruttore infiammatorio e una possibile soluzione
Lo studio ha ricondotto questo stress mitocondriale ai segnali infiammatori cronici nell’obesità, in particolare al mediatore immunitario interferone‑γ (IFN‑γ), prodotto in eccesso nel tessuto adiposo. L’IFN‑γ attiva un repressore trascrizionale chiamato Ikaros che si lega alla regione di controllo del gene SerpinB2 e ne riduce l’espressione. Nei topi ingegnerizzati in modo che le loro cellule mieloidi non potessero rispondere all’IFN‑γ, i macrofagi residenti hanno mantenuto SerpinB2, sono sopravvissuti meglio e gli animali hanno mostrato glicemia più bassa, migliore sensibilità all’insulina e adipociti più piccoli. Al contrario, la cancellazione specifica di SerpinB2 nei macrofagi ha aggravato l’intolleranza al glucosio e la resistenza all’insulina, in parte perché il tessuto adiposo è diventato più infiammato ed espanso. Aumentare i livelli dell’antiossidante glutatione con il supplemento N‑acetilcisteina (NAC) ha ristabilito la protezione mitocondriale, salvato la sopravvivenza dei macrofagi residenti, ridotto le dimensioni degli adipociti e migliorato i parametri metabolici anche quando SerpinB2 mancava.
Cosa significa per la salute metabolica
Per il lettore non specialista, il messaggio centrale è che non tutto il grasso né tutte le cellule immunitarie residenti nel grasso sono dannose. Un gruppo specializzato e a lunga vita di macrofagi nel grasso viscerale ci protegge effettivamente dall’infiammazione incontrollata e dall’iperglicemia mantenendo i loro mitocondri sani tramite le difese antiossidanti indotte da SerpinB2. Nell’obesità, segnali infiammatori cronici spengono SerpinB2, i mitocondri si stressano, queste cellule protettive muoiono e prendono il sopravvento macrofagi più dannosi, contribuendo alla resistenza all’insulina. Il lavoro suggerisce che terapie mirate a preservare i macrofagi residenti — bloccando il freno IFN‑γ/Ikaros su SerpinB2 o sostenendo le difese antiossidanti a base di glutatione — potrebbero aiutare a prevenire o trattare le malattie metaboliche legate all’obesità.
Citazione: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Parole chiave: grasso viscerale, macrofagi, mitocondri, resistenza all’insulina, SerpinB2