Clear Sky Science · it
Ingegneria metabolica della biosintesi della doxorubicina tramite ottimizzazione dei partner redox dei P450 e analisi strutturale di DoxA
Perché conta la storia di origine di un farmaco antitumorale
La doxorubicina è uno dei farmaci di punta della chemioterapia moderna, impiegata per trattare tumori che vanno dalla leucemia ai carcinomi mammari. Eppure, nonostante decenni di impiego, il modo in cui produciamo questa medicina è sorprendentemente tortuoso: l’industria di solito la ricava a partire da un composto correlato invece di lasciare che il microrganismo produttore completi la sintesi. Questo studio rivela perché il batterio che la produce fatica a eseguire gli ultimi passaggi chimici e mostra come la reingegnerizzazione della sua macchina interna possa incrementare nettamente la produzione di doxorubicina completa, aprendo la strada a forniture più affidabili e potenzialmente meno costose.
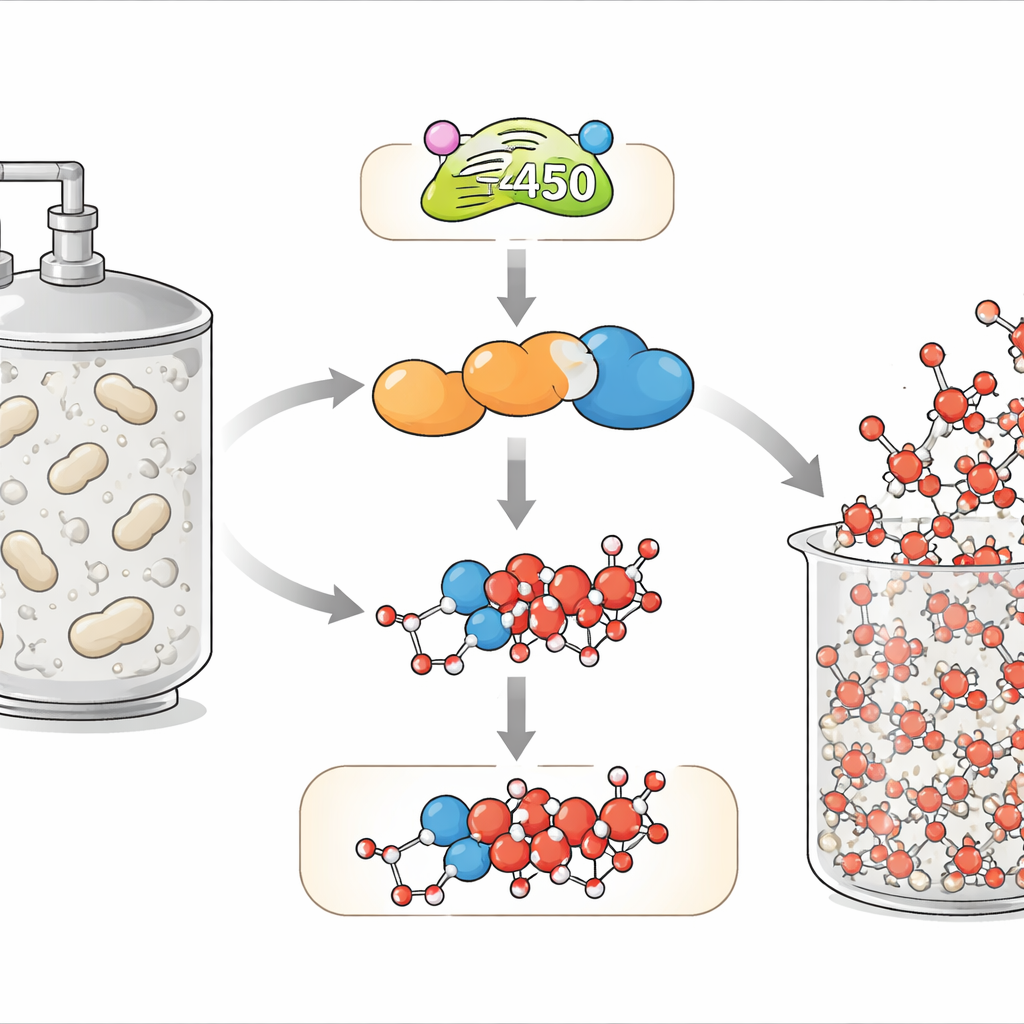
Dai batteri del suolo al farmaco che salva vite
La doxorubicina appartiene agli antracicline, una famiglia di molecole naturali sintetizzate da batteri del suolo del genere Streptomyces. Questi composti condividono uno scheletro carbonioso rigido e piatto che si inserisce tra le basi del DNA, oltre a un’unità zuccherina che si sistema nelle scanalature del DNA. Insieme, queste caratteristiche bloccano la macchina cellulare che gestisce il DNA e infine inducono la morte cellulare – utile contro le cellule tumorali a rapida proliferazione. Il produttore classico, Streptomyces peucetius, sintetizza naturalmente per lo più un precursore chiamato daunorubicina e solo una quantità modesta della più efficace doxorubicina, che differisce per una singola ulteriore funzione contenente ossigeno. Quel minore cambiamento strutturale migliora drasticamente l’attività ma si rivela sorprendentemente difficile da ottenere in modo efficiente per il microrganismo.
Trovare il corretto cablaggio elettrico all’interno della cellula
L’enzima cruciale che esegue gli ultimi tre passaggi di ossidazione sullo scheletro del farmaco si chiama DoxA, un membro della famiglia dei citocromi P450. Come una piccola fabbrica chimica, DoxA necessita di un flusso costante di elettroni per attivare l’ossigeno e inserire nuovi atomi di ossigeno sulla molecola. All’interno del batterio quegli elettroni sono forniti tramite una staffetta di proteine ausiliarie note come partner redox. Il genoma di S. peucetius contiene diversi candidati, rendendo incerto quali effettivamente si accoppino con DoxA. Confrontando l’attività genica e il metabolismo in un ceppo normale, in un mutante ricco di daunorubicina e in un mutante ricco di doxorubicina, i ricercatori hanno individuato un ferredossina (Fdx4) e una ferredossina reduttasi (FdR3) come partner naturali. Ricostruire questo trio in reazioni in vitro ha confermato che DoxA funziona meglio quando collegato a questa precisa catena di trasferimento elettronico, proprio come usare l’adattatore di alimentazione giusto per un dispositivo.
Alleviare il rallentamento autoindotto dell’enzima
Anche con il cablaggio elettrico corretto, DoxA tende a bloccarsi nell’ultimo passaggio che converte la daunorubicina in doxorubicina. Lavori precedenti suggerivano che il prodotto stesso possa inceppare l’enzima. Il team si è concentrato su un gene adiacente, dnrV, la cui funzione era stata poco chiara. Test biochimici hanno mostrato che la proteina DnrV lega saldamente una gamma di molecole antracicliniche, inclusa la doxorubicina, senza alterarle chimicamente. Aggiungere DnrV alle reazioni con DoxA ha migliorato notevolmente il flusso della chimica, permettendo la conversione completa dei precursori al farmaco finale evitando reazioni collaterali dannose. In termini pratici, DnrV agisce come una spugna interna che assorbe la doxorubicina appena formata, impedendole di intasare l’enzima o di danneggiare il DNA all’interno della cellula produttrice.
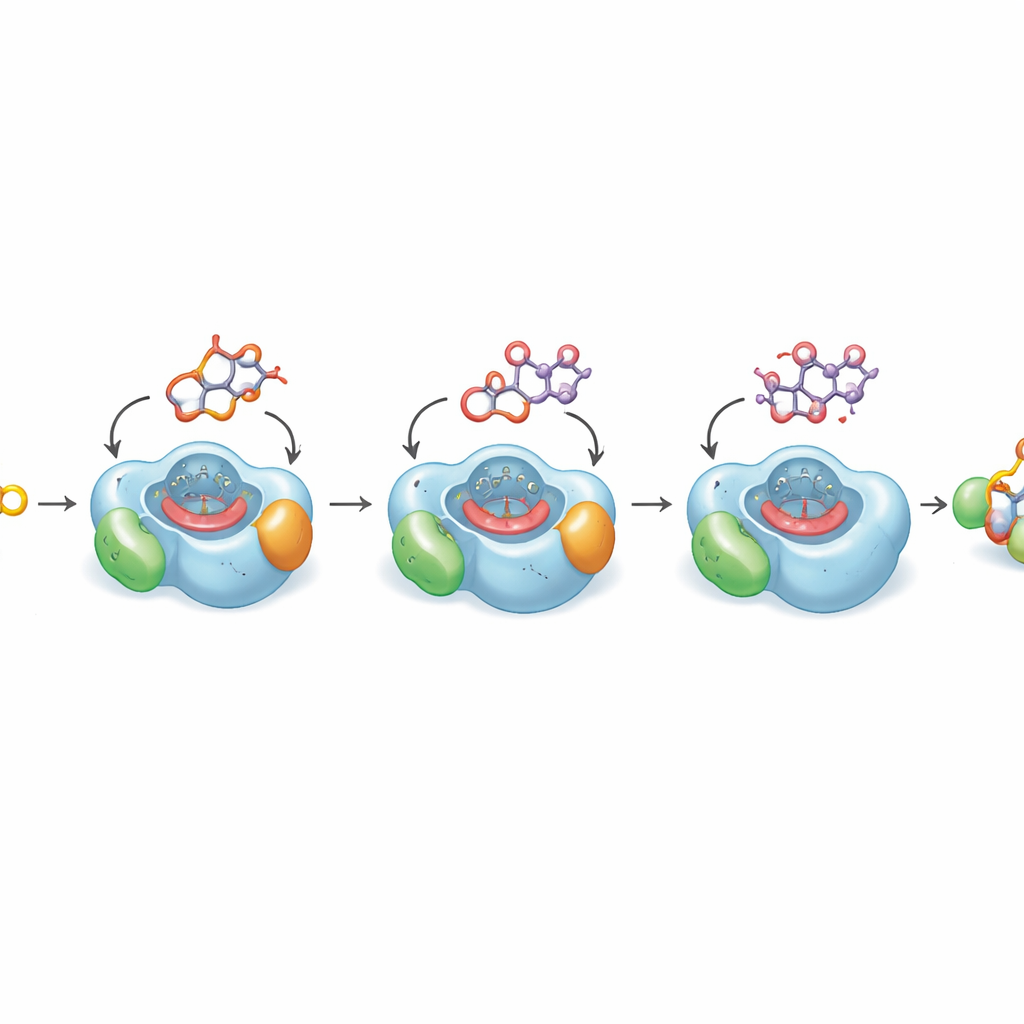
Capire perché l’ultimo passaggio è così lento
Per comprendere perché l’ossidazione finale è intrinsecamente lenta, gli autori hanno risolto strutture cristalline ad alta risoluzione di DoxA legato a tre intermedi successivi. Queste strutture rivelano come il nucleo piatto del farmaco e lo zucchero ad esso attaccato si alloggino in una tasca stretta sopra il gruppo eme dell’enzima, il centro metallico reattivo che esegue l’ossidazione. Nei passaggi precedenti, l’atomo di carbonio che deve essere modificato si trova vicino all’eme in una posizione ideale per la reazione. Ma nel substrato finale, la daunorubicina, la porzione della molecola che necessita dell’idrossilazione si piega lontano dall’eme verso una piccola cavità oleosa, una disposizione che calcoli quantomeccanici mostrano essere energeticamente favorita. Simulazioni al computer su scale temporali di microsecondi confermano che la molecola visita solo occasionalmente una posa produttiva per l’inserimento dell’ossigeno finale. Questo bias strutturale spiega perché la conversione in doxorubicina è naturalmente inefficiente.
Costruire un ceppo migliore per produrre doxorubicina
Con queste informazioni, i ricercatori hanno riprogettato razionalmente il batterio invece di affidarsi a mutagenesi casuale. Hanno introdotto un gene per la riparazione del DNA per stabilizzare la produzione, quindi hanno inserito copie extra di doxA, dei partner redox ottimali fdx4 e fdr3 e del legante utile dnrV sotto promotori selezionati per bilanciarne le quantità. Hanno inoltre ottimizzato le condizioni di coltura e usato resine speciali per assorbire intermedi tossici e appiccicosi. In colture da laboratorio e in un bioreattore da 20 litri, il miglior ceppo ingegnerizzato ha prodotto 336 milligrammi di doxorubicina per litro di coltura con un rapporto doxorubicina:daunorubicina di 81:19 — un aumento di circa il 180% rispetto al ceppo di partenza e una miscela di prodotto molto più pulita.
Cosa significa per la futura fornitura di farmaci antitumorali
Analizzando sia il sistema di supporto elettrico sia la struttura 3D di un enzima chiave, questo lavoro spiega perché un microrganismo di rilevanza medica sia inefficientemente produttivo nel sintetizzare il nostro antracicline più pregiato. Accoppiare DoxA con i suoi partner redox naturali, aggiungere una proteina ausiliaria che lega il farmaco e riequilibrare l’espressione genica ha trasformato un produttore riluttante in uno robusto. Sebbene ulteriori ottimizzazioni dell’enzima potrebbero accelerare ancora il passaggio chimico finale, lo studio avvicina già la produzione completamente biologica di doxorubicina alla realtà industriale. Per i pazienti e i sistemi sanitari, tali progressi potrebbero tradursi in accesso più sicuro, scalabile e conveniente a un farmaco che è un pilastro della chemioterapia.
Citazione: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Parole chiave: produzione di doxorubicina, biosintesi degli antracicline, ingegneria degli enzimi, produzione microbica di farmaci, citocromo P450