Clear Sky Science · it
L'attivazione della proteina chinasi C atipica guida l'escrezione intestinale del glucosio nel diabete mellito
Trasformare l'intestino in una valvola per lo zucchero
Le persone con diabete convivono con un eccesso di zucchero nel sangue. Interventi bariatrici come il bypass gastrico possono normalizzare la glicemia in modo sorprendentemente rapido, anche prima di una perdita di peso significativa, ma il meccanismo di questo effetto è stato a lungo un mistero. Questo studio mette in luce una "valvola dello zucchero" basata sull'intestino: un modo con cui l'intestino sottrae glucosio dal sangue e ne scarica una parte di nuovo nel lume intestinale, suggerendo un nuovo bersaglio farmacologico che potrebbe imitare i benefici chirurgici senza l'operazione.
Perché la chirurgia modifica la glicemia così in fretta
I medici sanno da tempo che il bypass gastrico Roux-en-Y, un intervento comune per la perdita di peso, è anche uno dei trattamenti più efficaci per il diabete di tipo 2. Subito dopo l'intervento, la glicemia dei pazienti spesso migliora in modo notevole, prima ancora di una perdita di peso marcata. Lavori precedenti di questo gruppo avevano mostrato che, dopo il bypass, alcune porzioni dell'intestino tenue cominciano a comportarsi come una spugna, assorbendo glucosio dal circolo sanguigno e rilasciandone una parte nello spazio interno dell'intestino. Questo comportamento insolito, chiamato escrezione intestinale del glucosio, sembrava dipendere da una proteina trasportatrice chiamata GLUT1. La grande domanda era: quale interruttore molecolare istruisce l'intestino a commutare in questa modalità di eliminazione dello zucchero?
Usare i big data per trovare un interruttore molecolare
Per cercare quell'interruttore, i ricercatori hanno utilizzato un sistema computazionale su larga scala per la scoperta di farmaci basato sulla Connectivity Map, un database che descrive come migliaia di composti chimici alterano l'attività genica nelle cellule. Hanno confrontato i profili di espressione genica di cinque situazioni in cui l'escrezione intestinale del glucosio è elevata — incluso tessuto di ratti sottoposti a bypass e cellule trattate con segnali di crescita intestinale — con i profili prodotti da farmaci noti. Una classe di composti è emersa con costanza: gli attivatori della protein chinasi C (PKC), una famiglia di enzimi che trasmettono segnali all'interno delle cellule. Approfondendo, il gruppo si è concentrato sul sottogruppo "atipico" delle PKC, in particolare su un isoenzima chiamato PKCζ, la cui attività nelle cellule intestinali corrispondeva più da vicino allo stato simile al bypass con escrezione di glucosio.
La pompa dello zucchero delle cellule intestinali in azione
Avvicinandosi alle singole cellule intestinali mediante sequenziamento dell'RNA a cellula singola, gli autori hanno scoperto che il bypass aumenta sia PKCζ sia GLUT1 in specifiche cellule assorbenti del tratto distale dell'intestino tenue. In colture cellulari e organoidi intestinali umani, l'aumento artificiale di PKCζ o il trattamento con prostratina — un composto di origine vegetale che attiva in sicurezza queste PKC atipiche — ha indotto il trasportatore GLUT1 a spostarsi sulla superficie cellulare. Lì, GLUT1 ha funzionato come una pompa bidirezionale: attraeva più glucosio dal lato a contatto con il sangue delle cellule e permetteva all'eccesso di uscire nel lume intestinale. È importante notare che questo instradamento dello zucchero non ha accelerato in modo significativo la glicolisi cellulare, indicando che l'effetto principale era lo smaltimento del glucosio, non una maggiore produzione di energia.
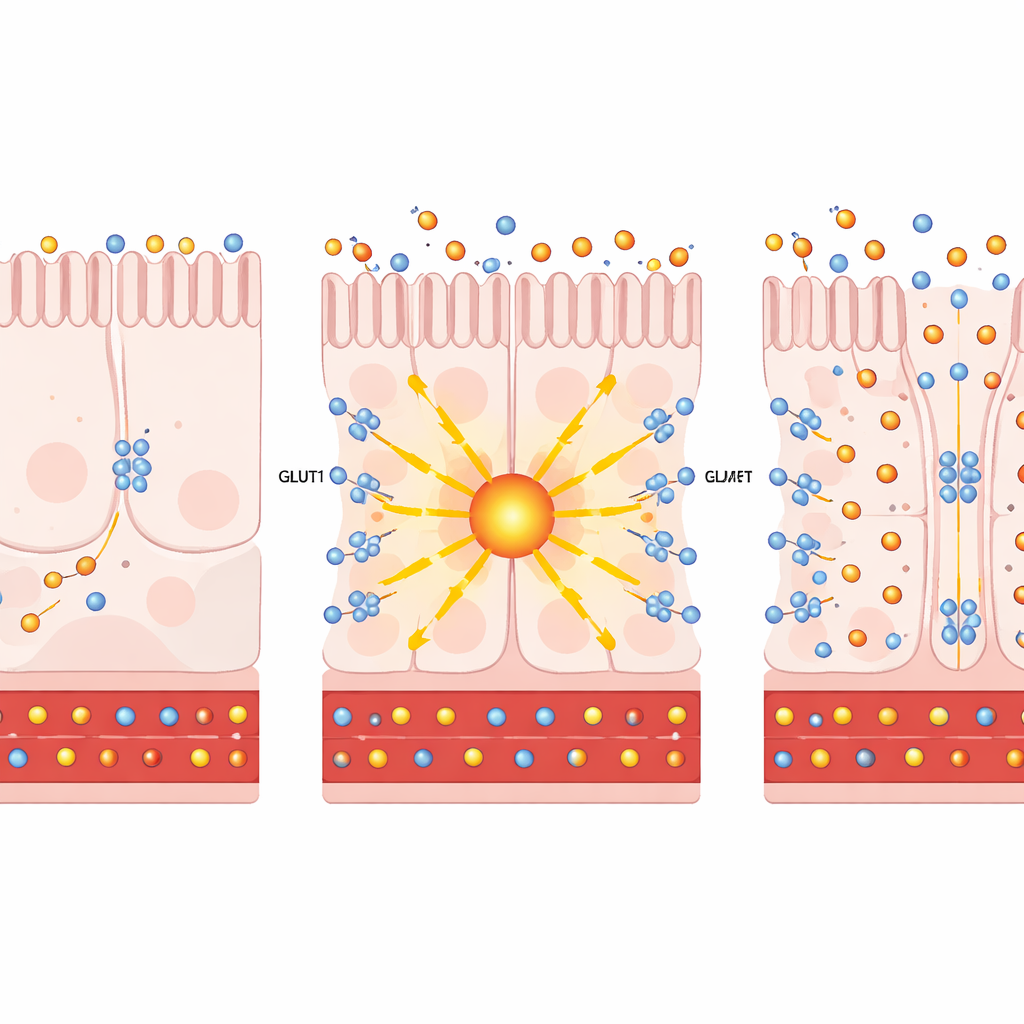
Dalle cellule ai topi: imitare la chirurgia senza il bisturi
Il team ha quindi testato se l'attivazione di questa via in animali vivi potesse migliorare il diabete. In topi obesi e resistenti all'insulina, l'espressione aumentata di PKCζ specificamente nell'intestino ha ridotto la velocità di aumento di peso, abbassato la glicemia a digiuno e migliorato la tolleranza al glucosio. Traccianti di zuccheri radioattivi hanno mostrato un maggiore assorbimento di glucosio da parte dell'intestino distale e il suo lavaggio nel lume intestinale. Un quadro simile è emerso nei modelli murini diabetici trattati con prostratina: hanno guadagnato meno peso, gestito meglio i carichi di zucchero e deviato più glucosio nel tratto intestinale, il tutto senza variazioni nei livelli di insulina, nell'assunzione di cibo o nell'integrità della barriera intestinale. Nei tagli di tessuto, GLUT1 è comparso sia sul lato rivolto al sangue sia su quello verso il lume, posizionandosi perfettamente per prelevare zucchero dalla circolazione e spingerlo nell'intestino.
Cosa potrebbe significare per la cura futura del diabete
Per un non specialista, il messaggio chiave è che l'intestino può essere trasformato in una via di fuga controllata per l'eccesso di zucchero nel sangue. Attivando un enzima specifico all'interno delle cellule intestinali — le PKC atipiche — i ricercatori sono riusciti a indurre le cellule a trasferire più trasportatori GLUT1 sulla loro superficie e a comportarsi come uno scarico reversibile, sottraendo glucosio dal sangue e riversandone una parte nel lume intestinale. Nei topi, questo smaltimento guidato dall'intestino ha migliorato la glicemia e limitato l'aumento di peso senza sovrastimolare l'insulina, modificare l'appetito o danneggiare l'intestino. Sebbene prostratina e composti affini non siano ancora approvati come farmaci per il diabete, questo lavoro indica la via aPKC–GLUT1 come un promettente bersaglio per future terapie che potrebbero riprodurre in parte i benefici metabolici del bypass gastrico senza ricorrere all'intervento chirurgico.
Citazione: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Parole chiave: escrezione intestinale del glucosio, diabete di tipo 2, trasportatore GLUT1, proteina chinasi C atipica, prostratina