Clear Sky Science · it
Segnale autocrino TGFβ1 attivato da MerTK regola la risposta microgliale alla neurodegenerazione
Come la squadra di pulizia del cervello modella la malattia
Quando i neuroni nel cervello e nel nervo ottico muoiono, lasciano dietro di sé una scia di detriti. Cellule immunitarie specializzate chiamate microglia fungono da squadra di pulizia del cervello, inglobando questi rifiuti. Ma le microglia fanno più che riordinare: il modo in cui reagiscono può proteggere i circuiti nervosi o peggiorare malattie come l’Alzheimer. Questo studio scopre un circuito di auto-comunicazione nascosto all’interno delle microglia che viene attivato dai detriti delle fibre nervose morenti e aiuta a determinare quanto intensamente queste cellule rispondono al danno.
Un innesco nascosto nelle fibre nervose morenti
Per sondare questo processo, i ricercatori hanno usato un modello murino in cui il nervo ottico viene schiacciato, causando la degenerazione delle lunghe proiezioni dei neuroni oculari senza uccidere i corpi cellulari. Questo isola chiaramente le conseguenze della degradazione degli assoni. Sulla superficie di queste fibre in degenerazione, una molecola grassa si capovolge verso l’esterno, fungendo da segnale “mangiami” per le microglia vicine. Questi segnali vengono percepiti da un recettore sulle microglia chiamato MerTK, uno di una piccola famiglia di proteine che riconoscono i detriti. Eliminando selettivamente MerTK nelle microglia, il gruppo ha dimostrato che senza questo recettore le microglia non attivano la loro risposta tipica al danno: si dividono meno, si muovono meno e attivano meno geni collegati al controllo del danno e all’infiammazione.
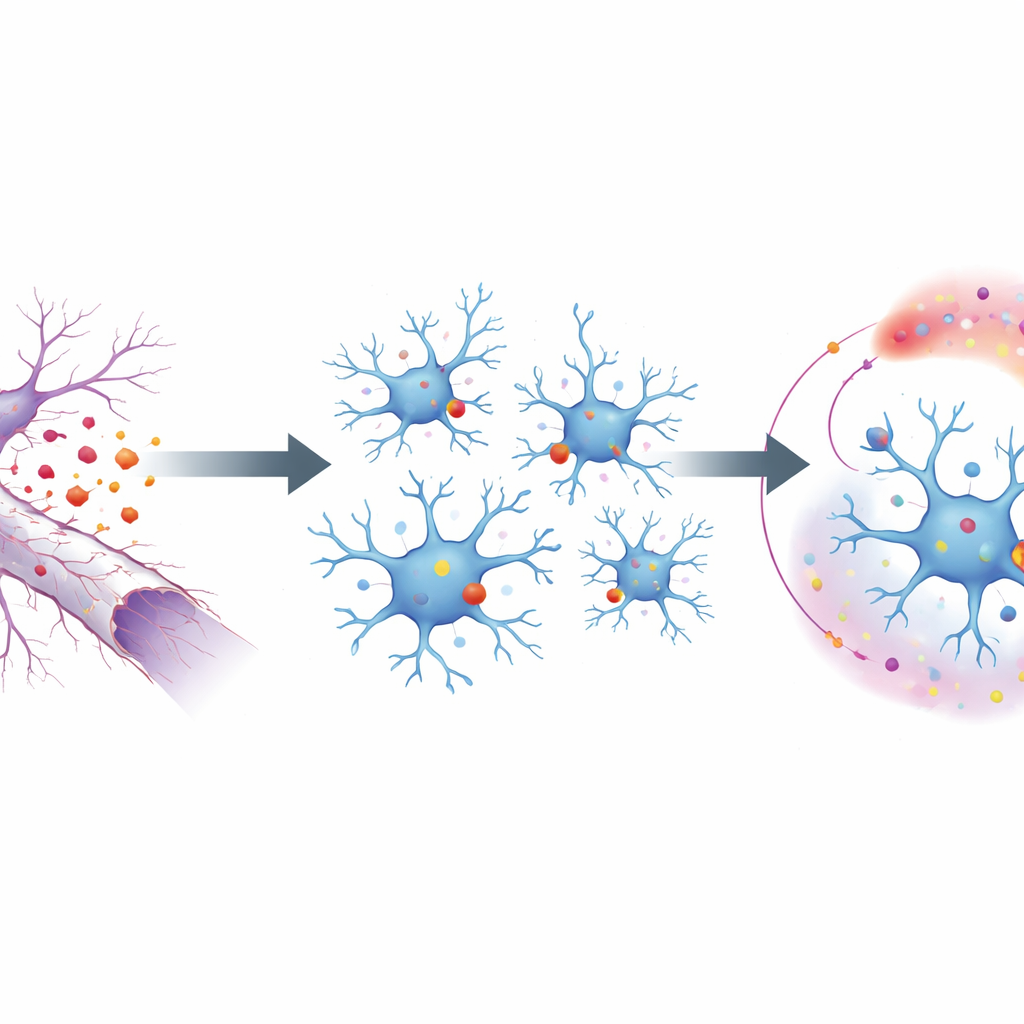
Dal segnale di superficie alla riprogrammazione genetica
Analizzando le microglia dall’interno, gli scienziati hanno tracciato come il segnale di MerTK sulla superficie venga convertito in cambiamenti nell’attività genica. Hanno scoperto che MerTK attiva un reattore molecolare chiamato fosfolipasi C, che a sua volta potenzia due proteine di controllo maestro nel nucleo, PU.1 e IRF8. Questi fattori agiscono come capi cantiere sulla linea di montaggio microgliale, attivando molti geni necessari per uno stato attivato. Utilizzando mappe di legame al DNA, il team ha scoperto che PU.1 e IRF8 si legano direttamente a un sito specifico nel gene che codifica per TGFβ1, una potente proteina di segnalazione. Quando questo sito di legame è stato mutato in modo che i capi non potessero più ancorarsi, le microglia nei nervi lesionati non sono più riuscite ad aumentare la produzione di TGFβ1, pur mantenendo altre funzioni di base intatte.
Un circuito di retroazione nelle microglia
La domanda successiva era cosa faccia effettivamente TGFβ1 in questo contesto. Lo studio mostra che le microglia producono TGFβ1 e poi rispondono a esso esse stesse, formando un circuito autocrino, o di retroazione su sé stesse. Quando TGFβ1 o i suoi recettori sono stati rimossi geneticamente solo dalle microglia, la lesione ha comunque causato la degenerazione degli assoni, ma le microglia non hanno più mostrato il loro programma completo di attivazione. Si sono proliferate meno ed hanno espresso meno geni di risposta al danno e infiammatori, anche se molti marcatori identitari omeostatici sono rimasti soppressi da altri segnali. Una molecola chiave a valle della segnalazione TGFβ, chiamata SMAD2 fosforilata, è comparsa specificamente nei nuclei microgliali dopo la lesione ed è in gran parte scomparsa quando TGFβ1 o i suoi recettori sono stati eliminati, confermando che il circuito di retroazione era interrotto.
Dal nervo ottico del topo ai cervelli dei malati di Alzheimer
Per verificare se questa via abbia rilevanza oltre un modello di lesione artificiale, gli autori hanno esaminato un modello murino ampiamente usato della malattia di Alzheimer. In questi animali, le microglia raggruppate attorno alle placche amiloidi mostravano alti livelli di PU.1, IRF8, TGFβ1 e segnalazione TGFβ attivata, riecheggiando i risultati sul nervo ottico. Il team si è poi rivolto a dati umani da sequenziamento di RNA a singolo nucleo di tessuto cerebrale di pazienti con Alzheimer. Lì, le microglia si sono distinte come le principali cellule che esprimono gli omologhi umani di MerTK, PU.1, IRF8 e TGFB1. In sezioni cerebrali postmortem dei pazienti, le microglia mostravano anche forti segni di segnalazione TGFβ attiva, in contrasto con i tessuti dei donatori di controllo. Insieme, queste osservazioni suggeriscono che lo stesso circuito di auto-comunicazione opera nella malattia umana.
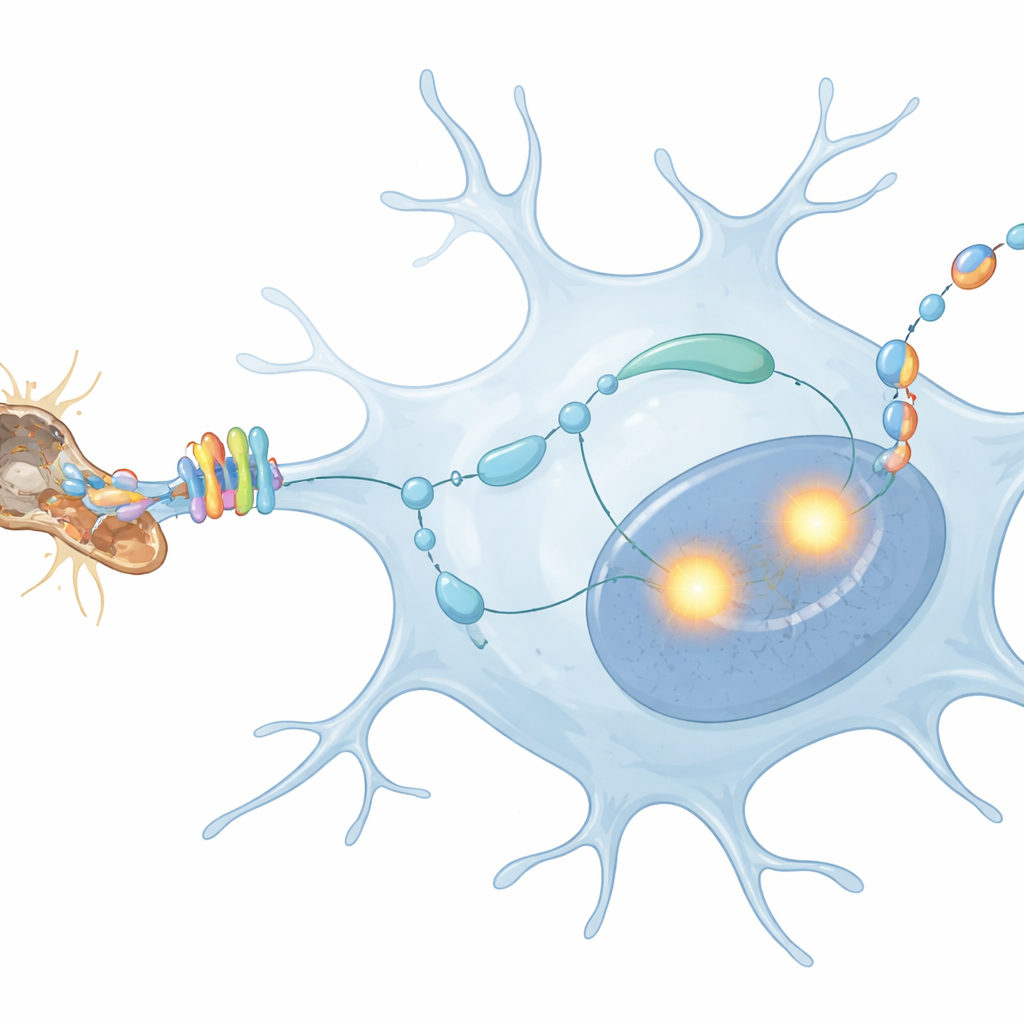
Perché questo dialogo interno è importante per la salute cerebrale
Questo lavoro rivela una catena di eventi nella quale i detriti delle fibre nervose in degenerazione attivano MerTK sulle microglia, che a sua volta aumenta PU.1 e IRF8, i quali inducono le microglia a produrre TGFβ1 che ricade su se stesse. Questo dialogo interno affina e sostiene la loro risposta alla neurodegenerazione. Per un lettore non specialista, il messaggio chiave è che le cellule addette alla pulizia del cervello non sono meri raccoglitori passivi; ascoltano attivamente i propri segnali e questo circuito di retroazione può influenzare se le loro azioni proteggono i neuroni o favoriscono la progressione di malattie come l’Alzheimer. Comprendere e, possibilmente, modulare questo circuito potrebbe aprire nuove strade per moderare l’infiammazione dannosa preservando la pulizia benefica fornita dalle microglia.
Citazione: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Parole chiave: microglia, neurodegenerazione, morbo di Alzheimer, infiammazione cerebrale, segnalazione TGF-beta