Clear Sky Science · it
Determinante molecolare della dipendenza da basso voltaggio dell’inattivazione umana di Nav1.7 rivelata da un inibitore selettivo di Nav1.7 basato sull’efficacia
Abbassare il volume dei segnali del dolore
Perché alcune persone avvertono un dolore lancinante a un tocco leggero, mentre altre quasi non sentono nulla? Gran parte della risposta risiede in minuscoli portali proteici nelle nostre cellule nervose che controllano i segnali elettrici. Questo studio svela come una sottile peculiarità strutturale in uno di questi portali, chiamato Nav1.7, lo renda particolarmente importante per innescare il dolore — e come un composto naturale, l’Uvarigranol D, possa spegnerlo selettivamente. Il lavoro indica una nuova strategia per progettare antidolorifici che calmano i nervi del dolore iperattivi senza rallentare il cuore o offuscare il cervello. 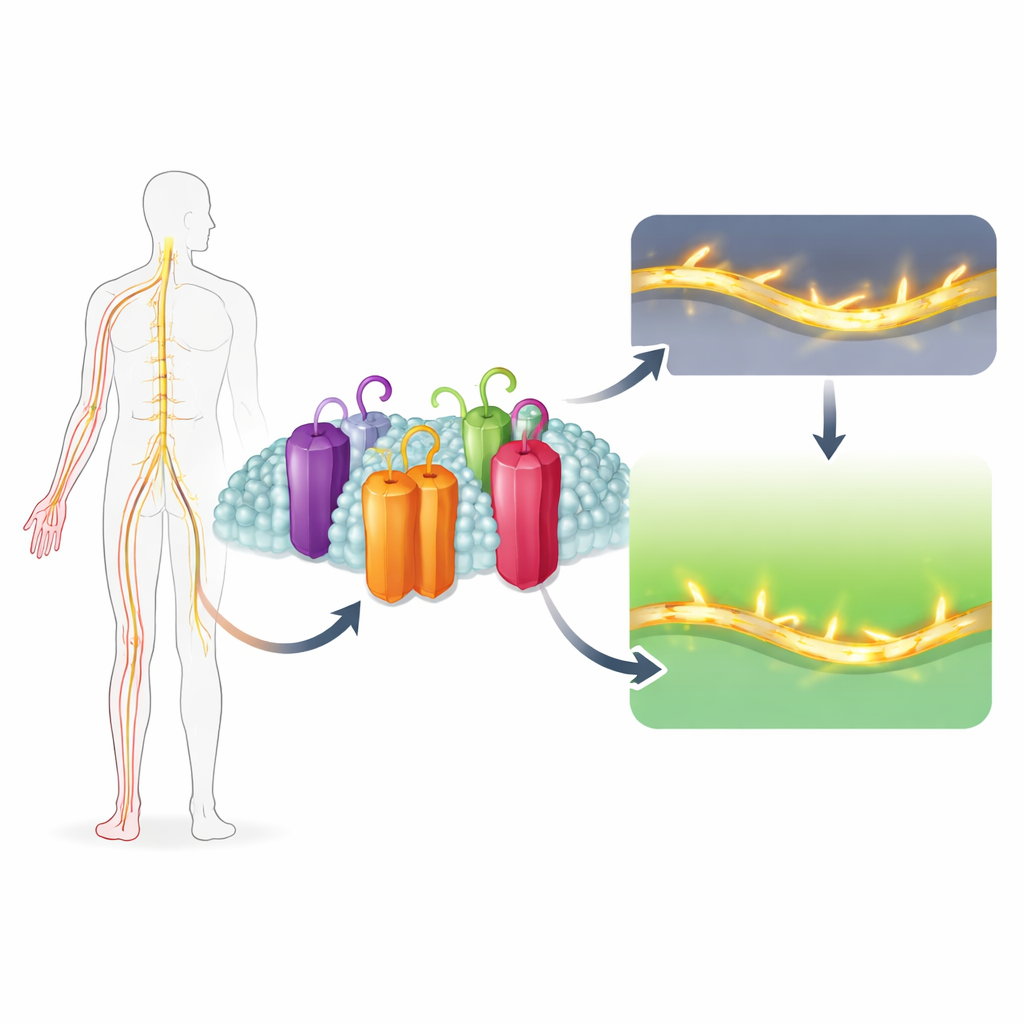
Un guardiano speciale per il dolore
I nostri nervi generano impulsi elettrici usando canali del sodio, pori microscopici che si aprono brevemente per far entrare ioni sodio carichi positivamente. Nell’uomo esistono nove versioni principali di questi canali, ciascuna ottimizzata per tessuti diversi come cervello, muscolo, cuore o fibre sensoriali del dolore. Nav1.7 è la versione presente nelle fibre periferiche del dolore. È particolare perché può attivarsi e inattivarsi a voltaggi più bassi rispetto ai suoi parenti, permettendole di rispondere anche a piccole variazioni di potenziale. Ciò rende Nav1.7 un potente amplificatore di segnali deboli che scatenano dolore. Studi genetici mostrano che l’iperattivazione di Nav1.7 provoca gravi sindromi dolorose ereditarie, mentre l’assenza totale di Nav1.7 rende le persone incapaci di provare dolore.
Alla ricerca di un bloccante selettivo per il dolore
Gli sviluppatori di farmaci da tempo sperano di colpire Nav1.7 per trattare il dolore cronico, ma questa proteina somiglia molto ad altri canali del sodio vitali per il battito cardiaco e la funzione cerebrale. La maggior parte dei farmaci sperimentali si lega a diversi tipi di canali, causando effetti collaterali o fallendo nelle prove cliniche. I ricercatori hanno selezionato oltre 1.500 composti naturali usando un saggio cellulare che rileva cambiamenti nel voltaggio della membrana. Hanno identificato una famiglia di molecole dalla pianta Uvaria grandiflora, concentrandosi su una chiamata Uvarigranol D (UGD). UGD attenuò le correnti di sodio in diversi tipi di canali, ma quasi completamente silenziò Nav1.7 mentre bloccava solo per metà altri canali anche a dosi elevate. Ciò significa che la sua selettività non deriva da un legame più forte, ma da un effetto molto più pronunciato una volta legato. 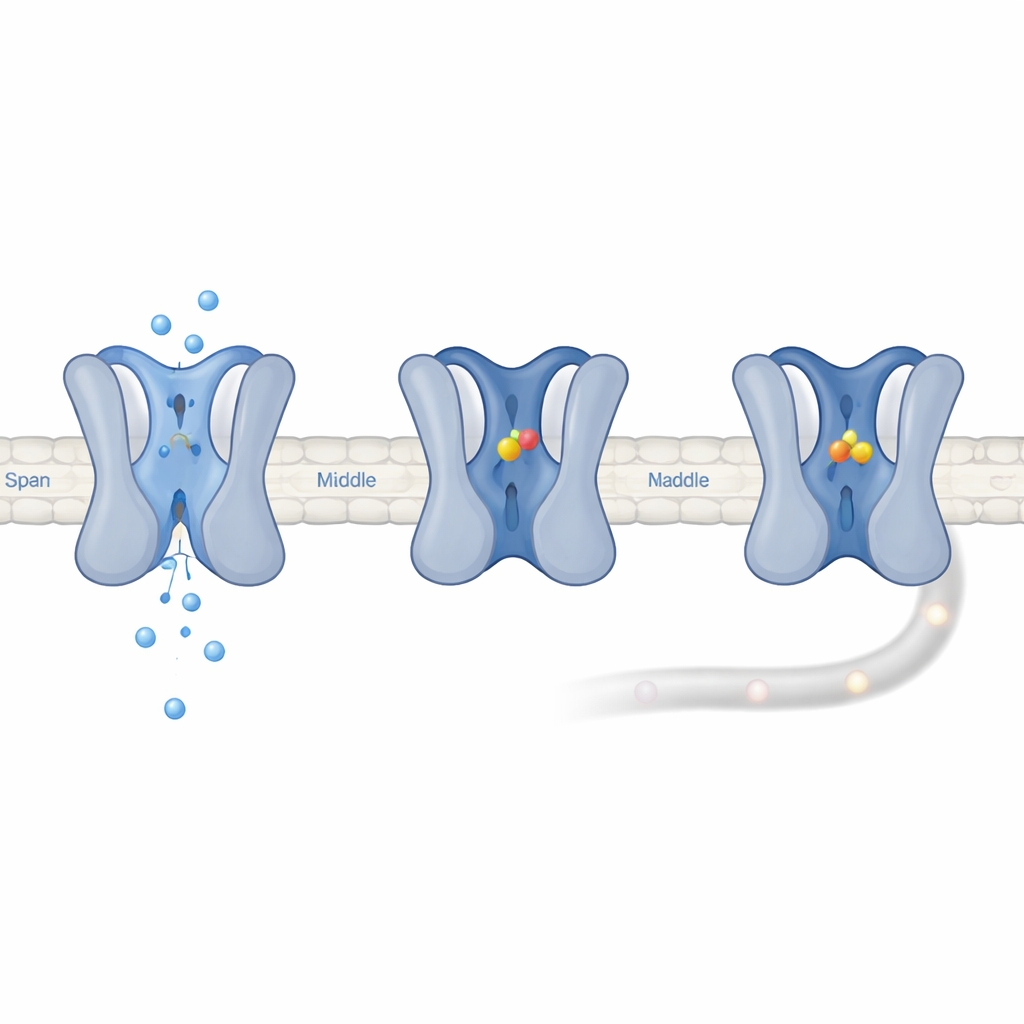
Un singolo cambiamento delle dimensioni atomiche rende Nav1.7 unica
Per capire perché UGD è così efficace su Nav1.7, il team ha costruito canali chimerici che scambiavano porzioni tra Nav1.7 e un canale cerebrale strettamente correlato, Nav1.2. Questo ha individuato una piccola regione vicino alla bocca esterna del poro, tra due segmenti strutturali chiamati S5 e S6 nel dominio III, come determinante chiave della piena capacità bloccante di UGD. Il confronto delle sequenze amminoacidiche ha rivelato che solo Nav1.7 porta una treonina alla posizione 1398, mentre tutti gli altri canali del sodio umani portano lì una metionina più ingombrante. Quando i ricercatori sostituirono la treonina di Nav1.7 con la metionina, UGD non riuscì più a chiudere completamente il canale; invertire la sostituzione in Nav1.2, mettendo una treonina al posto della metionina, rese quel canale simile a Nav1.7. Questa singola sostituzione modificò anche i voltaggi a cui i canali si attivano e si inattivano: la treonina rese il canale più incline ad aprirsi e inattivarsi a voltaggi più negativi e a farlo più rapidamente, proprietà che favoriscono la presenza di Nav1.7 in uno stato non a riposo anche vicino al voltaggio di riposo normale dei neuroni del dolore.
Bloccare il canale in una modalità inattivata
Le registrazioni elettriche hanno mostrato che UGD non si lega a Nav1.7 quando è chiuso o brevemente aperto. Preferisce invece canali che sono entrati in uno stato di “inattivazione lenta” di lunga durata, in cui il poro è chiuso e la ripresa richiede centinaia di millisecondi o più. Quando UGD era presente, i canali impiegavano circa dieci volte più a lungo per uscire da questo stato, il che significa che UGD lo stabilizza. Simulazioni al computer suggerirono che UGD si infila in una tasca formata dove un’ansa del dominio III incontra un’elica del dominio IV, stabilendo contatti chiave con cinque amminoacidi. Mutare uno qualsiasi di questi residui indebolì l’effetto di UGD, confermando l’importanza della tasca. Poiché la struttura ricca di treonina di Nav1.7 la porta a entrare in stati inattivati a voltaggi più bassi, una maggiore frazione dei suoi canali si trova proprio nello stato che UGD preferisce legare, spiegando perché Nav1.7 è funzionalmente molto più soppressa rispetto alle sue controparti nonostante affinità di legame simili.
Dai pori ionici all’alleviamento del dolore
In definitiva, ciò che conta è come questi eventi molecolari influenzano le cellule reali. Nei neuroni sensoriali del dolore del ganglio della radice dorsale di ratto, UGD ridusse notevolmente il numero di potenziali d’azione — i rapidi picchi di voltaggio che trasmettono informazioni sul dolore — e alla fine li bloccò del tutto a concentrazioni micromolari basse e submicromolari. Al contrario, cellule di tipo cardiaco umano derivate da cellule staminali, che usano principalmente un diverso canale del sodio (Nav1.5) e riposano a un voltaggio leggermente più negativo, risultarono circa 60 volte meno sensibili. Ciò suggerisce che un bloccante “efficacia-selettivo” come UGD può attenuare molto di più le vie del dolore rispetto al tessuto cardiaco o altri tessuti eccitabili semplicemente a causa della frequente presenza di Nav1.7 nel suo stato inattivato favorito dal farmaco.
Cosa significa per i futuri trattamenti del dolore
Lo studio rivela che un piccolo dettaglio strutturale — una singola treonina — sta alla base del comportamento a basso voltaggio di Nav1.7 e della sua capacità di generare “correnti soglia”, i segnali minimi che determinano se un neurone del dolore scaricherà. Legandosi e stabilizzando la forma inattivata di questo canale, UGD sfrutta quella tendenza intrinseca e sopprime Nav1.7 molto più fortemente rispetto ad altri canali del sodio. Per il lettore non specialista, la conclusione è che gli autori hanno mappato un punto debole preciso nel guardiano del dolore del corpo e mostrato come premerlo senza disturbare pesantemente i canali del cuore o del cervello. Questa intuizione apre la strada alla progettazione di nuovi antidolorifici che placano i nervi del dolore iperattivi mirando al comportamento in voltaggio e allo stato del canale, piuttosto che limitarsi a cercare un legame più stretto con Nav1.7.
Citazione: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
Parole chiave: canale del sodio Nav1.7, dolore cronico, Uvarigranol D, inibizione dipendente dallo stato, canali del sodio voltaggio-dipendenti