Clear Sky Science · it
Il meccanismo di pompaggio del Na+ guidato da redox nella NADH-quinone ossidoreduttasi di Vibrio cholerae si basa su cambiamenti conformazionali dinamici
Come l’impianto di energia del colera è diventato un bersaglio farmacologico
Il batterio che causa il colera, Vibrio cholerae, sopravvive e si moltiplica grazie a una minuscola centrale molecolare nella sua membrana cellulare. Questo studio rivela, con dettagli senza precedenti, come uno dei suoi motori chiave—un enzima chiamato Na⁺-NQR—modifichi la propria forma mentre funziona per pompare ioni sodio fuori dalla cellula. Capire questa macchina molecolare non solo soddisfa la curiosità di base su come la vita converte i nutrienti in energia utilizzabile, ma indica anche nuove strade per progettare antibiotici che disattivino batteri nocivi senza colpire le cellule umane.
Un motore alimentato a sodio nei batteri
Molti batteri marini e patogeni si affidano a Na⁺-NQR come primo passo nella catena respiratoria, la serie di reazioni che estrae energia dai nutrienti. Na⁺-NQR è inserito nella membrana interna e prende elettroni da una molecola carburante chiamata NADH, trasferendoli lungo una catena di molecole “ausiliarie” colorate (chiamate cofattori) fino alla chinone, un’altra piccola molecola incorporata nella membrana. Man mano che gli elettroni scorrono, l’enzima usa quell’energia per spingere ioni sodio (Na⁺) dall’interno verso l’esterno della cellula, creando un gradiente di sodio. Questo gradiente è come una batteria caricata: alimenta il motore flagellare batterico per il nuoto, aiuta la sintesi di ATP (la moneta energetica della cellula) e guida l’assorbimento di nutrienti e l’efflusso di farmaci. Poiché Na⁺-NQR esiste solo nei batteri ed è molto diverso dall’enzima correlato nei nostri mitocondri, rappresenta un bersaglio attraente per antibiotici altamente selettivi.
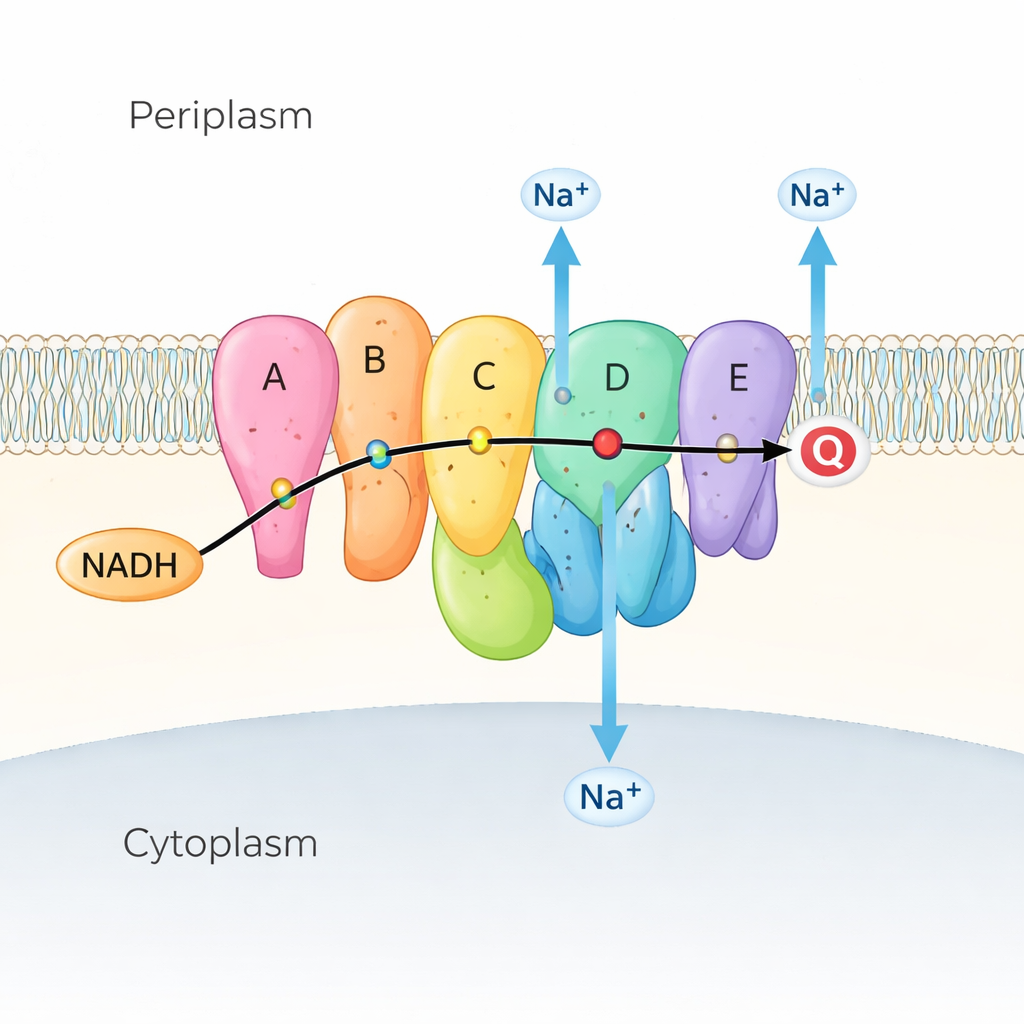
Osservare la macchina in movimento
I precedenti istantanee ottenute con diffrazione a raggi X e microscopia crioelettronica mostravano dove si trovano le subunità e i cofattori di Na⁺-NQR, ma rivelavano anche un enigma: alcuni salti elettronici critici erano troppo distanti perché gli elettroni potessero muoversi efficacemente a meno che la proteina non cambiasse conformazione. Gli autori hanno affrontato questo problema catturando Na⁺-NQR in molte condizioni leggermente diverse. Hanno usato mutanti che rimuovono cofattori specifici, farmaci che bloccano la reazione in stadi particolari e soluzioni con e senza sodio. Con crio-EM ad alta risoluzione e analisi avanzata delle immagini, sono riusciti a separare e ricostruire molteplici conformazioni dello stesso enzima, trasformando di fatto istantanee statiche in un filmato del suo ciclo di funzionamento.
Un braccio flessibile e una pinza che si sposta
Una scoperta chiave riguarda una subunità citoplasmatica flessibile, NqrF, che ospita due cofattori portatori di elettroni. Il gruppo ha identificato tre posizioni per il suo dominio “simile alla ferredossina”—soprannominate gli stati “alto”, “medio” e “basso”. Nel raro ma cruciale stato “basso”, questo piccolo dominio oscillA in una tasca formata da due subunità di membrana, NqrD e NqrE, avvicinando il suo cluster ferro-zolfo quanto basta per trasferire un elettrone in avanti. Nel frattempo, una subunità periplasmatica chiamata NqrC si comporta come una pinza mobile. In una conformazione (“stabile”) si accosta a un’altra subunità di membrana, NqrB, posizionandosi per trasferire elettroni verso l’accettore finale, la chinone. In una seconda conformazione (“spostata”), NqrC si muove verso NqrD/E, portando il suo cofattore flavinico più vicino per accettare un elettrone dal loro centro ferro-zolfo. Questi movimenti mostrano che NqrF e NqrC agiscono come corrieri dinamici, colmando ampi gap nella catena di cofattori.
Come i cambiamenti di forma pompano il sodio
Il cuore della pompa del sodio risiede nelle subunità accoppiate NqrD e NqrE, che formano un fascio centrale di eliche attraversanti la membrana. Sulla base delle strutture e di simulazioni di dinamica molecolare a livello atomico, gli autori mostrano che quando il cluster ferro-zolfo in NqrD/E viene ridotto (acquista un elettrone), si crea un sito carico negativamente che attrae un iono Na⁺ e alcune molecole d’acqua dal lato citoplasmatico, formando una tasca di legame transitoria. Residui idrofobici sopra e sotto questa tasca si comportano come porte interne ed esterne, controllando l’accesso allo ione. Quando NqrD/E passano da una forma “aperta verso l’interno” a una “aperta verso l’esterno”, il Na⁺ si sposta verso il lato periplasmatico ed è infine rilasciato mentre il cluster ferro-zolfo viene riossidato. Le simulazioni mostrano che il Na⁺ rimane parzialmente idratato ma non attraversa mai un tunnel continuo pieno d’acqua, suggerendo che l’enzima è ben sigillato contro perdite di protoni indesiderate.
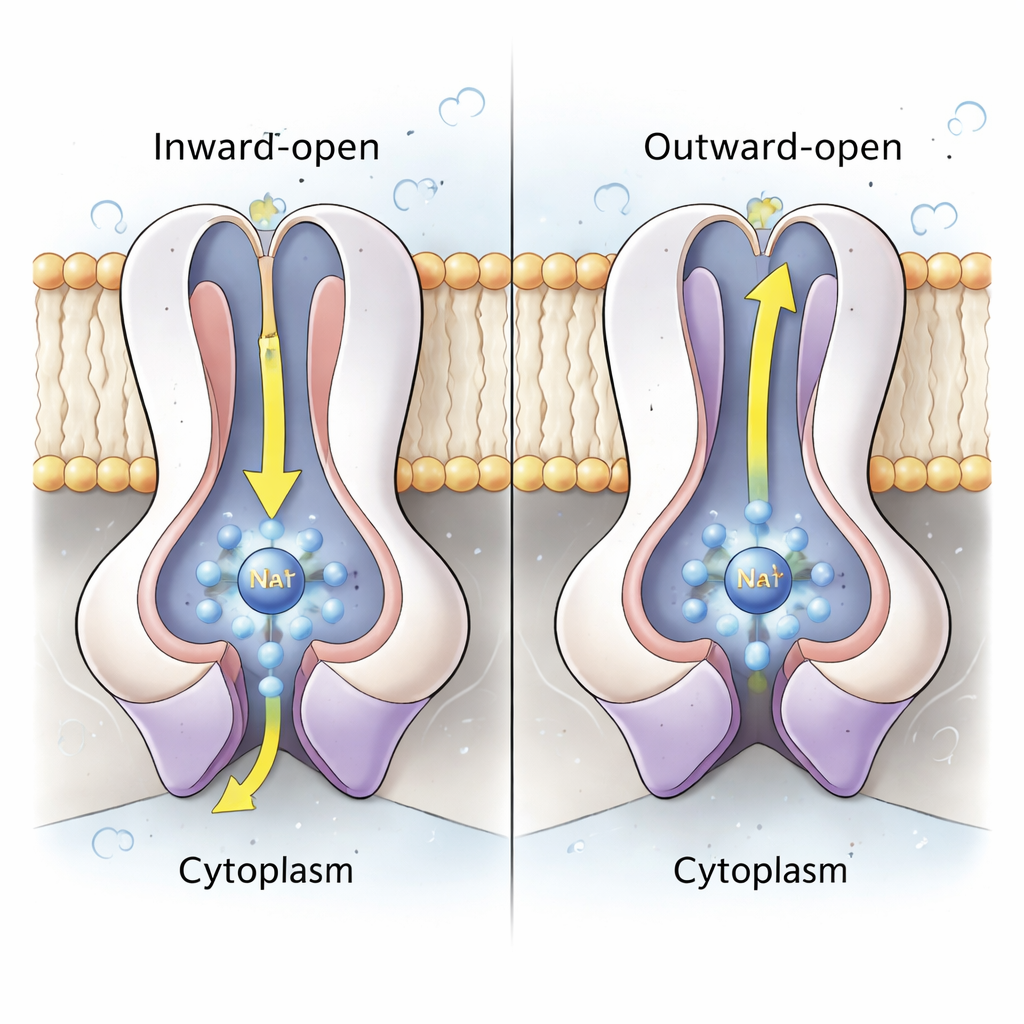
Un ciclo coordinato che fissa la direzione
Combinando tutti gli stati strutturali e le simulazioni, i ricercatori propongono un ciclo in sei passaggi. Prima NADH si lega e dona elettroni a NqrF, che a sua volta trasferisce un elettrone a NqrD/E, scatenando l’assorbimento di Na⁺ dal citoplasma e il caricamento della tasca centrale. La conseguente transizione conformazionale di NqrD/E alla forma aperta verso l’esterno espelle il Na⁺ verso la periplasma e incentiva NqrC a posizionarsi per accettare l’elettrone. I passaggi successivi trasferiscono elettroni verso i cofattori flavinici e riboflavinici finali e infine alla chinone, che deve ricevere due elettroni per diventare chinolo. È importante che gli stessi cambiamenti conformazionali che spostano il Na⁺ allentino e irrigidiscano alternativamente NqrF e NqrC, rendendo probabile il flusso elettronico in avanti solo quando il Na⁺ viene pompato verso l’esterno e scoraggiando scivolamenti all’indietro. Questo accoppiamento aiuta l’enzima a pompare Na⁺ contro un gradiente già esistente, mantenendo la “batteria” batterica carica.
Perché questo è importante per la medicina e la biologia
Per un non specialista, questo lavoro mostra come la vita costruisca macchine finemente coreografate fatte di proteine, dove minuscole variazioni di carica innescano grandi movimenti utili. Per la ricerca sulle malattie infettive, chiarisce che la traslocazione di Na⁺ in Na⁺-NQR avviene principalmente attraverso il nucleo NqrD/E, non attraverso la subunità NqrB precedentemente sospettata. Questa intuizione affina i punti in cui i futuri farmaci dovrebbero legarsi per meglio interrompere il motore che alimenta Vibrio cholerae e altri patogeni, risparmiando gli enzimi umani. Più in generale, lo studio fornisce una mappa strutturale di come le reazioni redox possano essere cablate al pompaggio di ioni—un principio di progetto che la natura riutilizza in molte forme di macchine bioenergetiche.
Citazione: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Parole chiave: pompa del sodio, respirazione batterica, Na+-NQR, cryo-EM, bersagli antibiotici