Clear Sky Science · it
Un sistema sintetico per la piroptosi sensibile all’RNA basato su una nucleasi‑proteasi CRISPR di tipo III‑E
Trasformare esplosioni cellulari letali in strumenti mirati
I nostri organismi a volte si difendono facendo esplodere le cellule infette o danneggiate in una forma di autodistruzione infiammatoria. Questa esplosione non solo elimina cellule pericolose, ma richiama anche il sistema immunitario. Il nuovo studio presenta un circuito genico sintetico, chiamato DAMAGE, in grado di leggere i messaggi di RNA all’interno di una cellula e decidere se quella cellula debba essere distrutta. Collegando un sistema di difesa microbico alla nostra macchina di morte cellulare, i ricercatori mostrano un modo per eliminare selettivamente cellule infette da virus, tumorali o invecchiate, risparmiando le vicine sane. 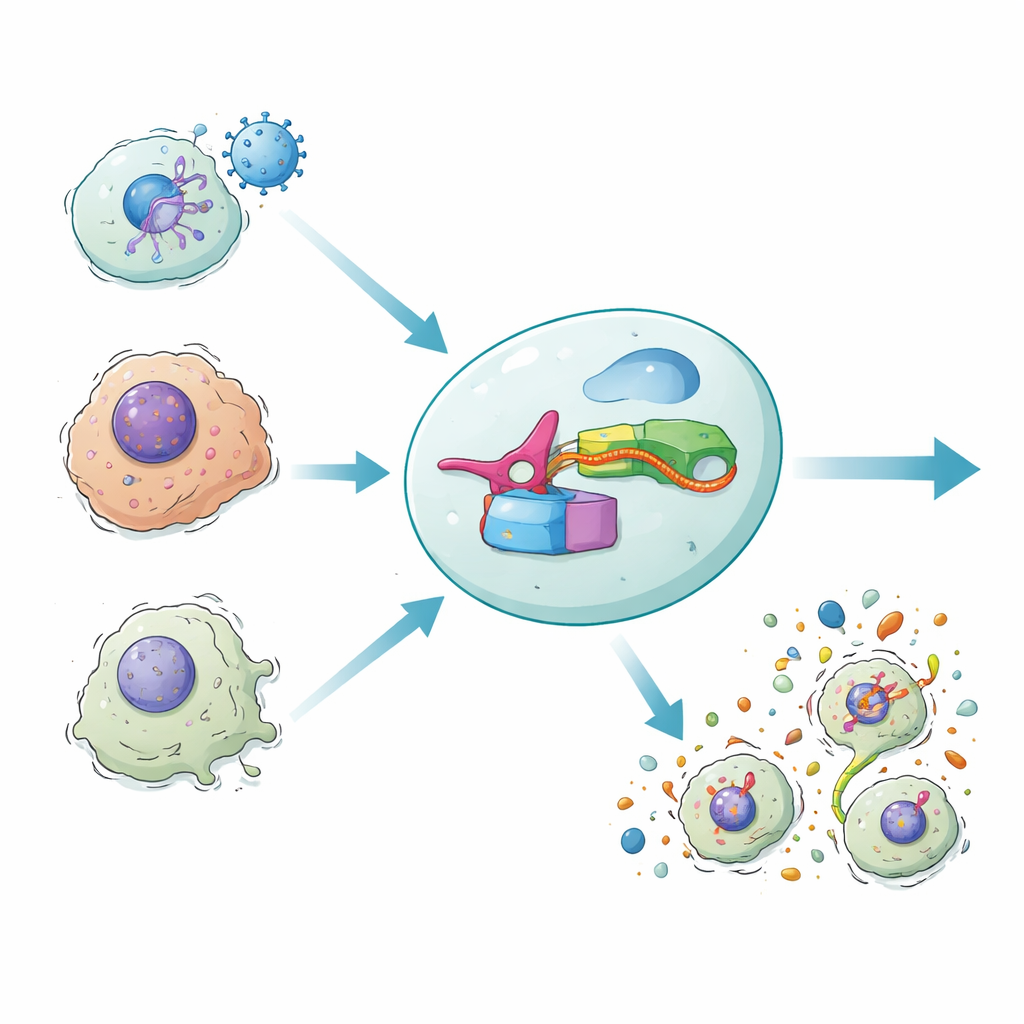
Come le cellule normalmente si fanno esplodere
Nella morte cellulare infiammatoria, una famiglia di proteine note come gasdermine giace nelle cellule come cariche pronte. Ogni gasdermina ha una metà anteriore “omicida” che può perforare le membrane cellulari e una metà posteriore che funge da “cappuccio di sicurezza” per trattenerla. Quando i sensori immunitari rilevano pericolo, gli enzimi tagliano le gasdermine in due, liberando la metà anteriore che si assembla in pori nella membrana esterna. La cellula si gonfia, scoppia e sprigiona segnali di allarme che richiamano le cellule immunitarie. Questa risposta potente aiuta a combattere infezioni e tumori, ma la sua rete di controllo naturale è complessa e difficile da riorganizzare per scopi terapeutici.
Prendere in prestito le difese batteriche per leggere l’RNA
I batteri hanno evoluto moduli di difesa compatti oggi noti grazie alla tecnologia CRISPR. Uno di questi, il sistema di tipo III‑E, utilizza una proteina chiamata Cas7‑11 in grado di legarsi a sequenze di RNA specifiche con l’aiuto di un breve RNA guida. Quando Cas7‑11 trova un RNA bersaglio corrispondente, attiva un enzima compagno, Csx29, che taglia una proteina partner, Csx30. Gli autori hanno capito che Csx30 poteva fungere da “cerniera” personalizzabile tra due parti proteiche. Hanno fuso questa cerniera tra le metà omicida e di sicurezza delle gasdermine umane, creando esecutori artificiali che si separano solo quando il sensore di tipo CRISPR rileva il suo RNA scelto all’interno della cellula.
Un interruttore di morte programmabile per cellule malate
Questo progetto, chiamato DAMAGE (Death Manipulation Gene), è costruito da cinque componenti: il sensore Cas7‑11, il tagliatore Csx29, una fusione gasdermina–Csx30, un RNA guida e l’RNA bersaglio presente nella cellula. Quando compare il giusto messaggio RNA, Cas7‑11 lo lega, attiva Csx29 e Csx29 incide la cerniera Csx30 nella proteina di fusione. La metà omicida della gasdermina viene rilasciata, crea pori nella membrana e la cellula muore in un’esplosione infiammatoria. Cambiando semplicemente l’RNA guida, il team ha reindirizzato DAMAGE verso diversi bersagli cellulari. Hanno mostrato che può riconoscere RNA del virus respiratorio sinciziale, di papillomavirus umano ad alto rischio nelle cellule del cancro cervicale e di varie mutazioni oncogeniche di KRAS che differiscono dall’RNA normale per una singola lettera. In ciascun caso, le cellule che portavano l’RNA sospetto venivano eliminate selettivamente, mentre le cellule di controllo vicine restavano intatte. 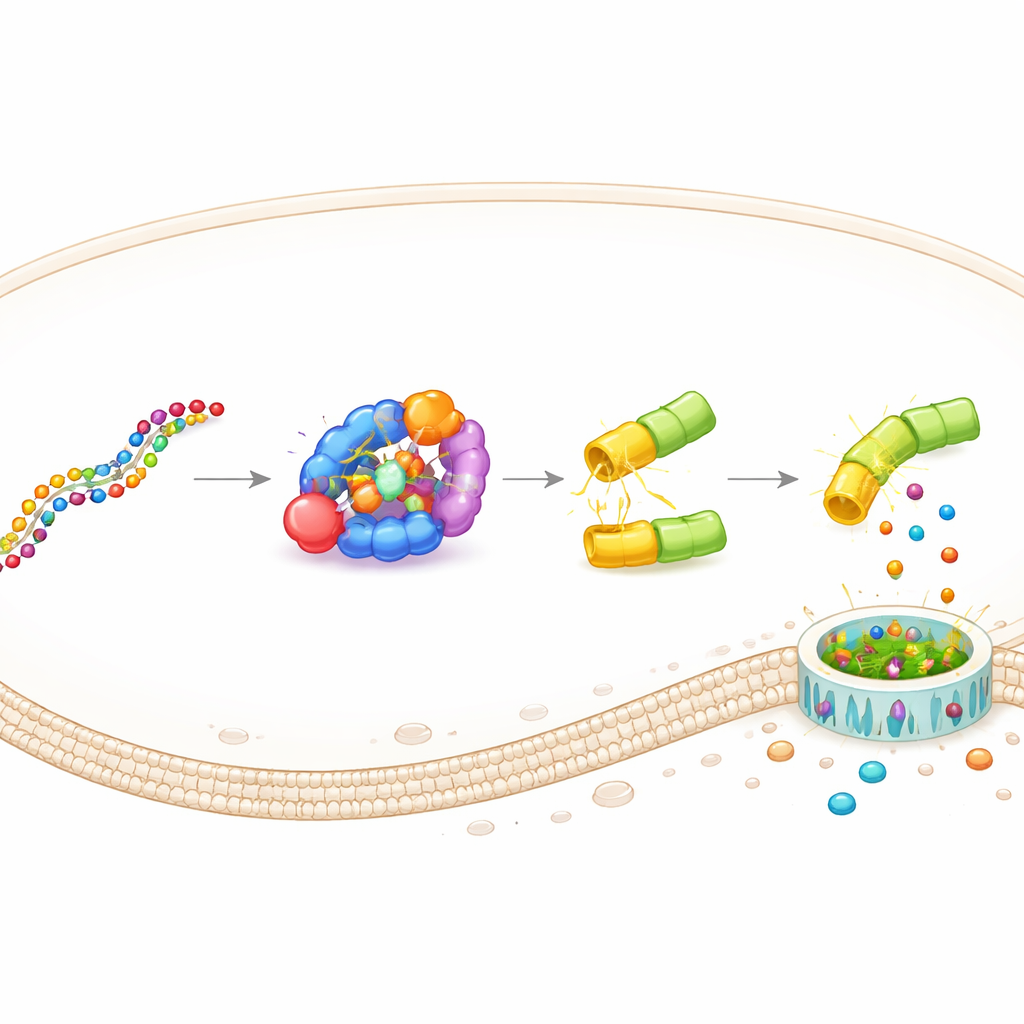
Mirare alle cellule invecchiate
I ricercatori hanno inoltre chiesto se DAMAGE potesse rintracciare le cellule senescenti—cellule invecchiate o sotto stress che smettono di dividersi ma si accumulano nei tessuti contribuendo a fragilità e malattie croniche. Tali cellule aumentano spesso la produzione di due proteine guardiane, p16 e p21. Programmando guide contro gli RNA di p16 e p21, il team ha creato una versione chiamata DAMAGE‑Aging. Questo circuito uccide le cellule con alti livelli di questi messaggi, risparmiando le cellule in cui p16 era stato rimosso geneticamente, confermando che il sistema legge l’abbondanza di RNA in tempo reale e non cambiamenti fissi nel DNA. Trattamenti farmacologici che aumentavano i livelli di p16 o p21 rendevano le cellule più vulnerabili a questa autodistruzione mirata.
Imballare il sistema per future terapie
Per avvicinarsi a un uso pratico, gli autori hanno compresso le numerose parti di DNA di DAMAGE in un costrutto snello, DAMAGE‑Plus, dimostrandone la funzionalità affidabile. Hanno quindi trascritto questo costrutto in mRNA sintetico, lo hanno confezionato in nanoparticelle lipidiche simili a quelle usate nei vaccini anti‑COVID‑19 e lo hanno veicolato in cellule in coltura. La versione mRNA ha assemblato con successo il circuito e ha innescato la morte infiammatoria mirata in cellule che portavano RNA virali o correlati al cancro. Sebbene il sistema complessivo sia ancora ingombrante e testato solo in linee cellulari, questi risultati suggeriscono che in futuro l’uccisione cellulare programmabile guidata da RNA potrebbe essere somministrata tramite formulazioni mRNA iniettabili.
Un nuovo modo di leggere e reagire ai messaggi cellulari
In termini semplici, DAMAGE è un buttafuori molecolare che verifica l’“ID” RNA interno di ogni cellula e scaccia solo quelle che appaiono pericolose—infette da virus, portatrici di mutazioni o senescenti—facendole precipitare in una forma esplosiva di autodistruzione. Il lavoro dimostra che i sensori di RNA batterici possono essere accoppiati alla macchina della morte cellulare umana con alta precisione, distinguendo anche differenze di una singola lettera nei messaggi genetici. Pur restando molto ingegneristico prima che un sistema del genere possa essere usato in sicurezza in animali o persone, delinea una strategia potente: leggere il brusio RNA vivo dentro le cellule e tradurlo direttamente in decisioni di vita o di morte.
Citazione: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Parole chiave: piroptosi, CRISPR, terapia mirata all’RNA, immunoterapia contro il cancro, senescenza cellulare