Clear Sky Science · it
hnRNPM coopera con BCAS2 per modulare lo splicing alternativo durante lo sviluppo oocitario
Perché conta la qualità dell'ovocita
Ogni vita umana inizia con un singolo ovocita, eppure gli scienziati stanno ancora scoprendo come queste cellule straordinariamente grandi si preparino al momento della fecondazione. Molto prima dell'arrivo degli spermatozoi, gli ovociti in crescita accumulano migliaia di messaggi di RNA che guideranno la loro maturazione e i primi giorni dello sviluppo embrionale. Questo studio rivela come una proteina poco nota, lavorando insieme a un partner, modifichi con cura quei messaggi negli ovociti di topo — e cosa succede quando questo sistema di modifica fallisce.
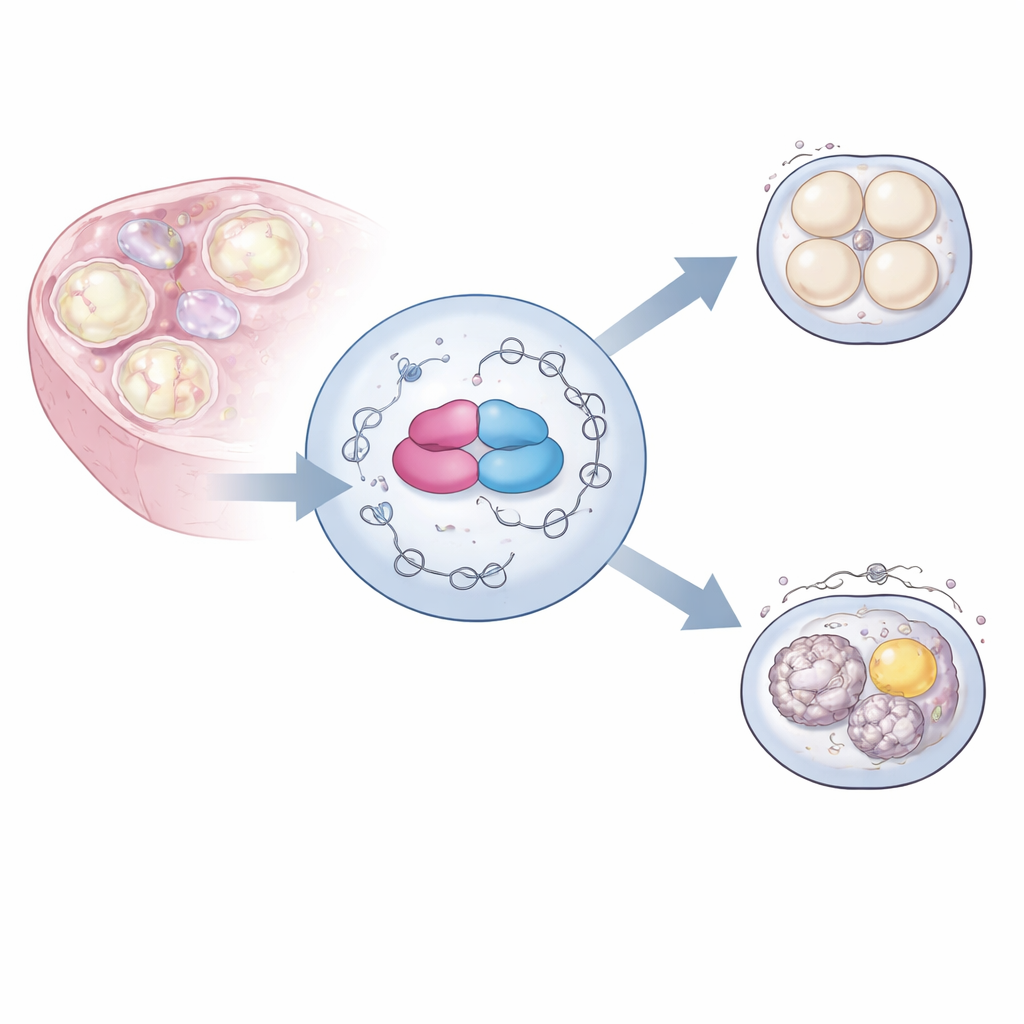
Guardiani dei messaggi genetici
Gli ovociti crescono nell'ovaio per settimane mentre il loro DNA rimane in gran parte silente. Durante questo periodo accumulano un vasto archivio di messaggi RNA materni copiati dal genoma in precedenza. Questi messaggi devono essere tagliati e cuciti in modi diversi, un processo chiamato splicing alternativo, per produrre la giusta combinazione di varianti proteiche nei momenti appropriati. Gli autori si sono concentrati su una proteina chiamata hnRNPM, parte di una grande famiglia che lega l'RNA, e sul suo partner BCAS2, entrambi abbondanti nel sistema riproduttivo femminile. Lavori precedenti suggerivano che queste proteine legano molti RNA negli ovociti, ma il loro ruolo preciso nel plasmare la fertilità restava poco chiaro.
Cosa va storto senza questo «editor»
Per indagare la funzione di hnRNPM, il gruppo ha usato l'ingegneria genetica per rimuovere il gene Hnrnpm specificamente dai precursori degli ovociti nei topi. Le ovaie di queste femmine apparivano normali e producevano un numero simile di ovociti rispetto ai controlli. Tuttavia, quando questi ovociti venivano fecondati in laboratorio, quasi mai sviluppavano oltre le prime divisioni, rendendo le femmine completamente sterili. Un'ispezione più attenta degli ovociti immaturi ha rivelato ammassi scuri nel citoplasma normalmente trasparente. La microscopia elettronica ha mostrato che una sottile impalcatura interna chiamata impalcatura citoplasmatica era per lo più assente, e organelli chiave come i mitocondri e le gocce lipidiche erano anormalmente aggregati anziché distribuiti uniformemente. Questi cambiamenti indicavano un problema profondo nell'organizzazione interna dell'ovocita.
Macchinario della divisione cellulare compromesso
Gli stessi ovociti mutanti faticavano anche a completare la meiosi, la divisione cellulare speciale che dimezza il numero di cromosomi. Quando i ricercatori hanno maturato gli ovociti in coltura, questi riuscivano ad avviare la meiosi ma generalmente si bloccavano prima di terminarla. Al microscopio, le strutture che separano i cromosomi — i fusi — apparivano attorcigliate, multipolari o mal ancorate. Una proteina chiamata pericentrina, che aiuta a organizzare i poli del fuso, compariva in ritardo e nei posti sbagliati. Nel loro complesso, questi difetti impedivano agli ovociti di allineare e separare i cromosomi in modo affidabile, una probabile causa del fallimento completo dello sviluppo dopo la fecondazione.
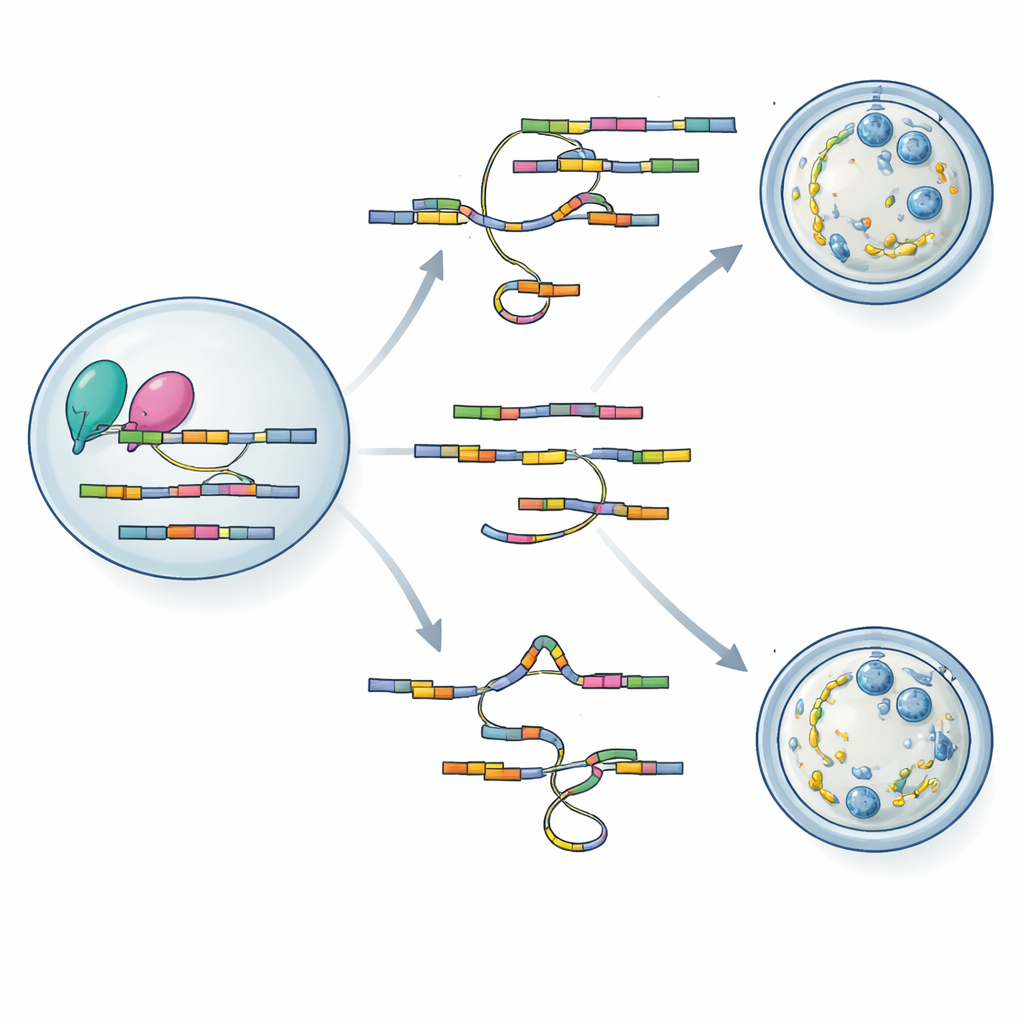
Leggere e riscrivere le istruzioni dell'RNA
Per capire come la perdita di hnRNPM porti a difetti così diffusi, il gruppo si è rivolto a due potenti strumenti di sequenziamento adattati a campioni minimi di ovociti. Usando SCAN-seq, che legge molecole di RNA a lunghezza intera da singoli oociti, hanno scoperto più di mille cambiamenti di splicing negli ovociti mutanti, inclusa molte varianti di RNA precedentemente sconosciute. I geni coinvolti nella costruzione dell'impalcatura citoplasmatica, nel controllo del comportamento del fuso e nella regolazione del ciclo meiotico risultavano particolarmente colpiti. Un secondo metodo, LACE-seq, ha mappato esattamente dove hnRNPM si lega sugli RNA, rivelando una preferenza per tratti ricchi di GU all'interno degli esoni. Sovrapponendo i due set di dati, gli autori hanno dimostrato che hnRNPM si trova direttamente su molti dei messaggi il cui splicing cambia quando la proteina manca, collegando la sua attività di legame alla correttezza dello splicing.
Un modello di lavoro di squadra per il controllo degli ovociti
Studi sulle interazioni proteiche hanno mostrato che hnRNPM si associa fisicamente a BCAS2 e ai componenti centrali del macchinario di splicing. I due partner si legano a molti degli stessi bersagli RNA e spesso li alterano nello stesso modo quando una delle due proteine è disturbata. In modo intrigante, la perdita di hnRNPM riduceva i livelli di proteina BCAS2 e indeboliva la capacità di BCAS2 di legarsi ai bersagli RNA condivisi, suggerendo che hnRNPM non solo modifica i messaggi ma aiuta anche a stabilizzare il suo partner su quei messaggi. Gli autori propongono un modello in cui hnRNPM e BCAS2 formano un complesso cooperativo che modella RNA materni chiave durante la crescita dell'oocita, assicurando la corretta assemblaggio dell'impalcatura citoplasmatica e divisioni meiotiche affidabili.
Cosa significa per la fertilità
In termini semplici, questo lavoro mostra che una squadra molecolare di editing — hnRNPM e BCAS2 — agisce dietro le quinte per preparare gli ovociti alla vita dopo la fecondazione. Quando questa squadra manca, l'impalcatura interna dell'ovocita collassa, il suo macchinario di ordinamento dei cromosomi non funziona e, sebbene l'ovocita venga prodotto in numero normale, non può sostenere lo sviluppo embrionale. Poiché hnRNPM è molto simile nei topi e negli esseri umani, questi risultati indicano un sistema di controllo della qualità conservato che potrebbe essere alla base di alcune forme di infertilità femminile inspiegata e offrire nuovi punti di accesso per diagnosi o terapie.
Citazione: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Parole chiave: sviluppo degli oociti, splicing alternativo, infertilità femminile, proteine leganti l'RNA, impalcatura citoplasmatica