Clear Sky Science · it
Ensemble a risoluzione atomica di proteine intrinsecamente disordinate con AlphaFold
Perché le proteine mutaforma sono importanti
Le nostre cellule sono piene di proteine che non si stabilizzano mai in una forma singola e rigida. Queste proteine “intrinsecamente disordinate” si comportano più come spaghetti molli che come macchine ripiegate con precisione, eppure sono centrali in processi che vanno dalla segnalazione cellulare alle malattie neurodegenerative. Poiché si muovono e si flettono continuamente, catturarne l’intera gamma di conformazioni a risoluzione atomica è estremamente difficile e di solito richiede anni di esperimenti e pesanti calcoli. Questo articolo presenta un nuovo modo di sfruttare insieme intelligenza artificiale e fisica per mappare queste molecole irrequiete in modo molto più efficiente.
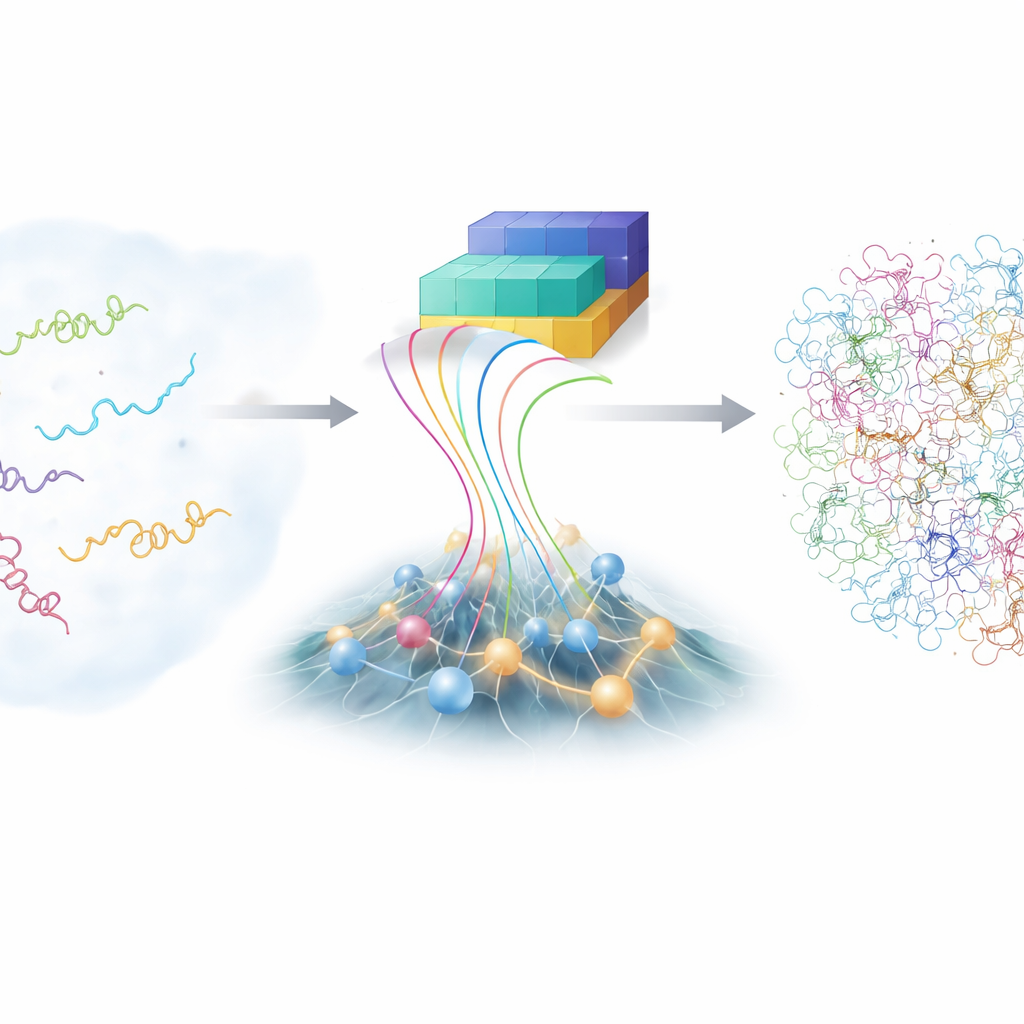
La sfida delle molecole irrequiete
A differenza dei modelli proteici da manuale che mostrano una struttura ordinata, le proteine intrinsecamente disordinate (IDP) vagano in un vasto paesaggio di possibili forme. Questa flessibilità le aiuta a riconoscere molti partner diversi, ma le rende anche notoriamente difficili da studiare. Le tecniche tradizionali di laboratorio, come la risonanza magnetica nucleare avanzata e la diffrazione/radioscattering a raggi X, possono fornire informazioni medie su molte conformazioni ma non su ciascuna forma individuale. Le simulazioni al dettaglio atomico possono, in principio, seguire ogni atomo mentre un IDP si contorce, tuttavia sono estremamente costose e dipendono da modelli fisici finemente tarati. Di conseguenza, la comunità scientifica dispone solo di una collezione limitata di ensemble IDP accurati e dettagliati da cui imparare.
Combinare ipotesi intelligenti con regole fisiche
Negli ultimi anni, la famiglia AlphaFold di strumenti di deep learning ha sbalordito la biologia prevedendo strutture proteiche a partire dalle sequenze di amminoacidi. Per le proteine disordinate, però, la principale forza di AlphaFold—indovinare una singola forma migliore—è meno utile, perché gli IDP non hanno una sola struttura. Ciò che AlphaFold fornisce, tuttavia, è una ricca informazione su quanto sia probabile che diverse parti della catena siano vicine o lontane tra loro. Gli autori hanno costruito un nuovo framework, chiamato bAIes, che tratta queste informazioni derivate dall’IA come guida morbida e le fonde con un modello fisico veloce che parte intenzionalmente da una visione a “random coil”, in cui la catena esplora tutte le possibili pieghe e torsioni senza favorire alcuna struttura particolare.
Da grovigli casuali ad ensemble realistici
Per prima cosa, i ricercatori hanno costruito un modello fisico efficiente che riproduce il comportamento di una catena proteica completamente non strutturata, basandosi su statistiche estratte da migliaia di strutture proteiche note. Questo modello funge da “prior” — l’aspettativa di base di come si muova un IDP se non sappiamo altro. Poi, bAIes legge le previsioni di AlphaFold su quali coppie di residui tendono ad avvicinarsi. Anziché costringere la proteina in un unico schema, converte quegli indizi in leggeri vincoli di distanza con incertezza incorporata, permettendo alla catena di soddisfare i suggerimenti dell’IA solo quando sono coerenti con il quadro fisico più ampio.
Verifica con esperimenti reali
Per verificare se questo approccio funziona, il gruppo ha applicato bAIes a un set di 21 proteine che vanno da catene quasi completamente casuali a sistemi più complessi con eliche transitorie e domini multipli. Per ciascuna hanno confrontato gli ensemble generati al computer con una vasta gamma di misure sperimentali che sondano sia dettagli locali sia dimensioni e forme globali. Per proteine molto flosci come il peptide Aβ40 legato all’Alzheimer, il semplice modello a random coil era già vicino alla realtà, e bAIes ha preservato questo buon accordo. Per proteine parzialmente strutturate, bAIes ha migliorato la corrispondenza con gli esperimenti catturando correttamente dove compaiono e scompaiono brevi segmenti elicali e patch compatte. Crucialmente, il metodo è rimasto robusto anche quando AlphaFold era eccessivamente fiducioso e prediceva per errore ripiegamenti stabili dove gli esperimenti in soluzione mostrano disordine, perché bAIes consente esplicitamente errori nell’input dell’IA.
Superare o eguagliare i metodi esistenti
Gli autori hanno poi confrontato bAIes con simulazioni all-atom pesanti eseguite su supercomputer specializzati, con modelli coarse-grained avanzati che semplificano le proteine in sfere e con nuovi generatori di deep learning addestrati su dati di simulazione. In molteplici test, bAIes ha sistematicamente eguagliato o superato questi approcci nel riprodurre i dati sperimentali, risultando molto meno dispendioso in termini computazionali rispetto alle simulazioni su larga scala. Ha funzionato anche al di là dei semplici IDP, gestendo proteine con diversi domini rigidi collegati da connettori flessibili e recuperandone la forma complessiva in soluzione. Quando i ricercatori hanno ulteriormente rifinito gli ensemble bAIes con dati sperimentali, l’accordo è migliorato ancora, dimostrando che il metodo può servire come punto di partenza potente per la modellizzazione integrativa.
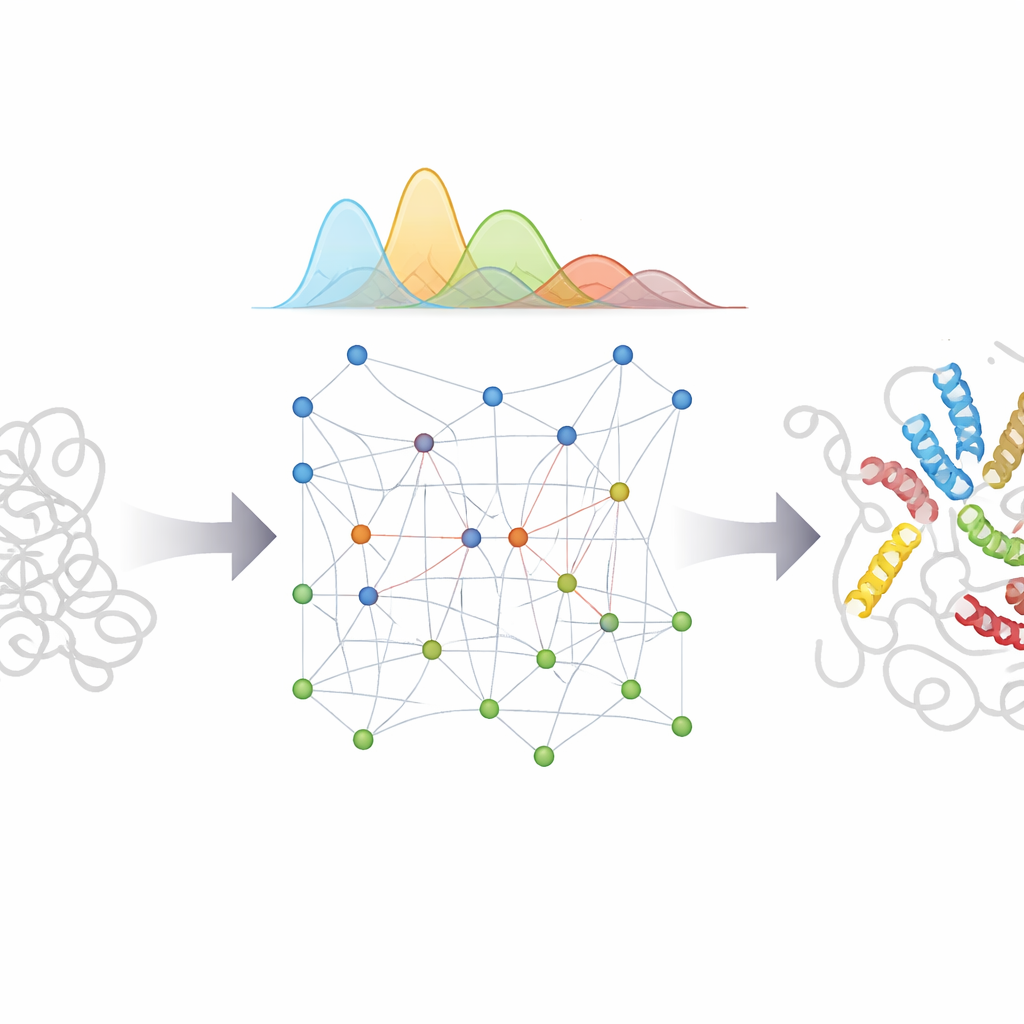
Cosa significa per la biologia e la medicina
Sposando il potere del riconoscimento di pattern di AlphaFold con un modello fisico accuratamente progettato e un trattamento bayesiano dell’incertezza, bAIes offre una via pratica verso “film” dettagliati di proteine disordinate anziché singoli istantanee. Questi ensemble a risoluzione atomica possono aiutare gli scienziati a capire come regioni flessibili riconoscano partner, come inizino il misfolding e l’aggregazione in malattie come il Parkinson e l’Alzheimer, e come piccole molecole possano legarsi a bersagli sfuggenti e mutevoli. Poiché il metodo è efficiente e integrato in software open source, può essere ampiamente adottato per generare ensemble realistici per molte proteine disordinate, guidando esperimenti e supportando futuri sistemi di IA che mirano a prevedere non una sola struttura, ma l’intera gamma di forme che le molecole più flessibili della vita possono assumere.
Citazione: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Parole chiave: proteine intrinsecamente disordinate, AlphaFold, modellizzazione bayesiana, ensemble proteici, biologia strutturale