Clear Sky Science · it
Impatto delle forze del solvente e della simmetria spezzata sull'assemblaggio di proteine progettate a un'interfaccia liquido-solido
Perché questo piccolo mondo su una superficie è importante
Dalle celle solari ai sensori medici, molte tecnologie future dipenderanno dalla capacità di costruire strutture precise dove le molecole biologiche incontrano materiali solidi. Questo studio indaga come «aste» proteiche progettate ad hoc si dispongono su superfici minerali in acqua salina. La lezione sorprendente è che l'acqua proprio sullo strato di superficie, e piccole asimmetrie nel cristallo sottostante, possono cambiare radicalmente l'allineamento di queste proteine—talvolta generando pattern che la teoria classica sostiene non dovrebbero esistere.
Progettare proteine per adattarsi a un cristallo
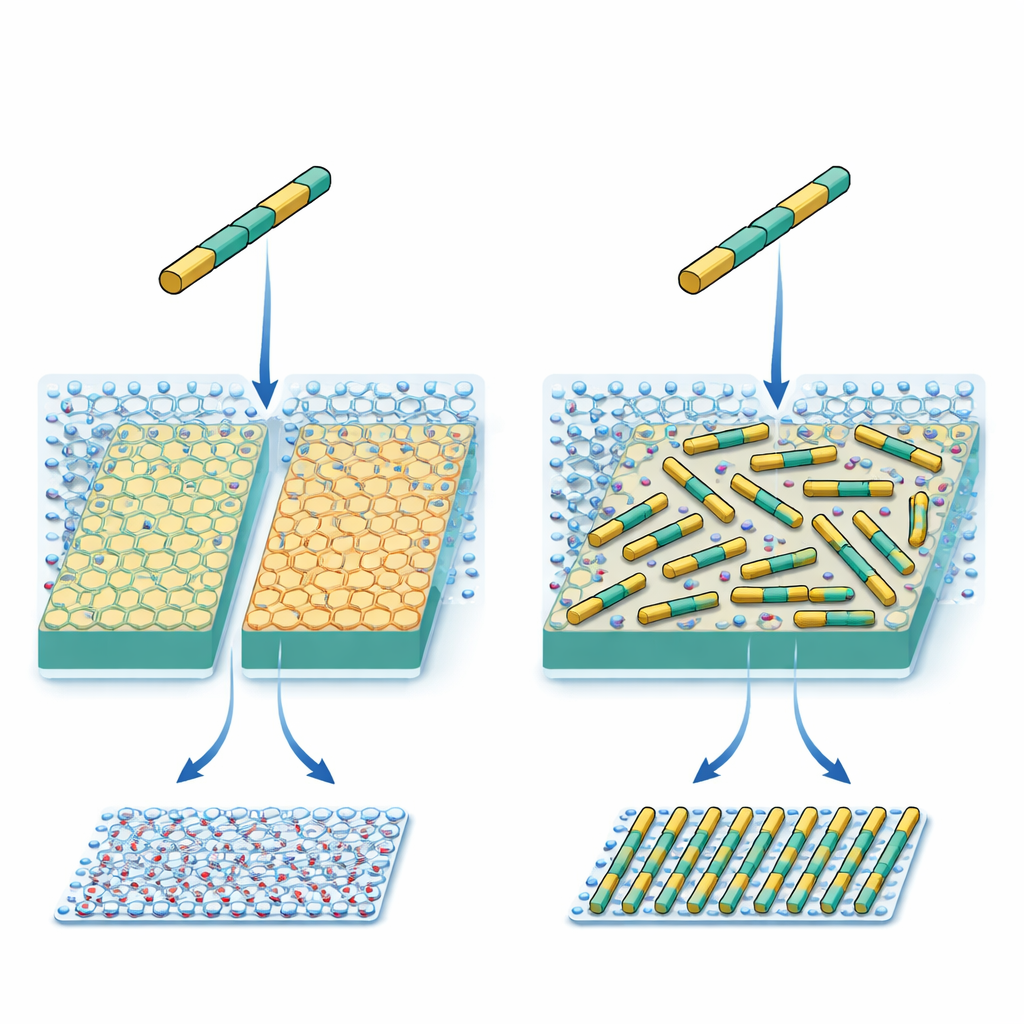
I ricercatori lavorano con una proteina artificiale a forma di asta corta e rigida. La sua chimica superficiale e la spaziatura dei gruppi carichi sono state progettate con cura per corrispondere al reticolo di ioni potassio su un minerale comune chiamato mica. In linea di principio, questo dovrebbe far sì che ogni asta proteica preferisca tre direzioni equivalenti sulla superficie del cristallo, come allinearsi lungo tre raggi di una ruota. Lavori precedenti hanno mostrato che, anche con una progettazione così accurata, le proteine formavano diversi pattern inaspettati invece della singola disposizione desiderata dagli ingegneri. Quell'incoerenza suggeriva che una forza importante mancava nelle regole di progettazione correnti.
Due superfici quasi identiche, due risultati molto diversi
Per seguire cosa stava accadendo, il team ha usato la microscopia a forza atomica ad alta velocità, che può osservare singole aste proteiche muoversi e assemblarsi su una superficie in tempo reale. Hanno confrontato due forme di mica strettamente correlate. Entrambe hanno lo stesso reticolo di potassio esposto, ma le loro strutture atomiche interne differiscono leggermente, il che a sua volta cambia come l'acqua si organizza a strati appena sopra la superficie. A livelli di sale moderati, le aste formavano su entrambe le superfici un tappeto denso ma localmente disordinato, con solo piccole aree di allineamento. Quando la concentrazione di sale è stata però portata molto alta, il comportamento si è diviso: su un tipo di mica le aste sono rimaste disordinate su tre direzioni, mentre sull'altro hanno formato spontaneamente lunghe file parallele e regolarmente spaziate che attraversavano tutta la superficie.
Strati d'acqua e simmetria spezzata
La modellizzazione al computer dei minerali e dell'acqua circostante ha aiutato a spiegare questa doppia personalità. Nella forma di mica più simmetrica, il primo e il secondo strato di molecole d'acqua preservano un motivo regolare esagonale. Nella forma meno simmetrica, atomi interni e gruppi sepolti all'interno del cristallo rompono quella simmetria a tre vie, e questo schema rotto si trasmette negli strati d'acqua vicini, che sviluppano regioni a strisce. Le proteine non toccano il cristallo nudo da sole; interagiscono anche con quest'acqua strutturata. Di conseguenza, un'orientazione delle aste diventa leggermente più favorevole delle altre due, anche se la corrispondenza progettata proteina–cristallo suggerirebbe che tutte e tre dovrebbero essere uguali.
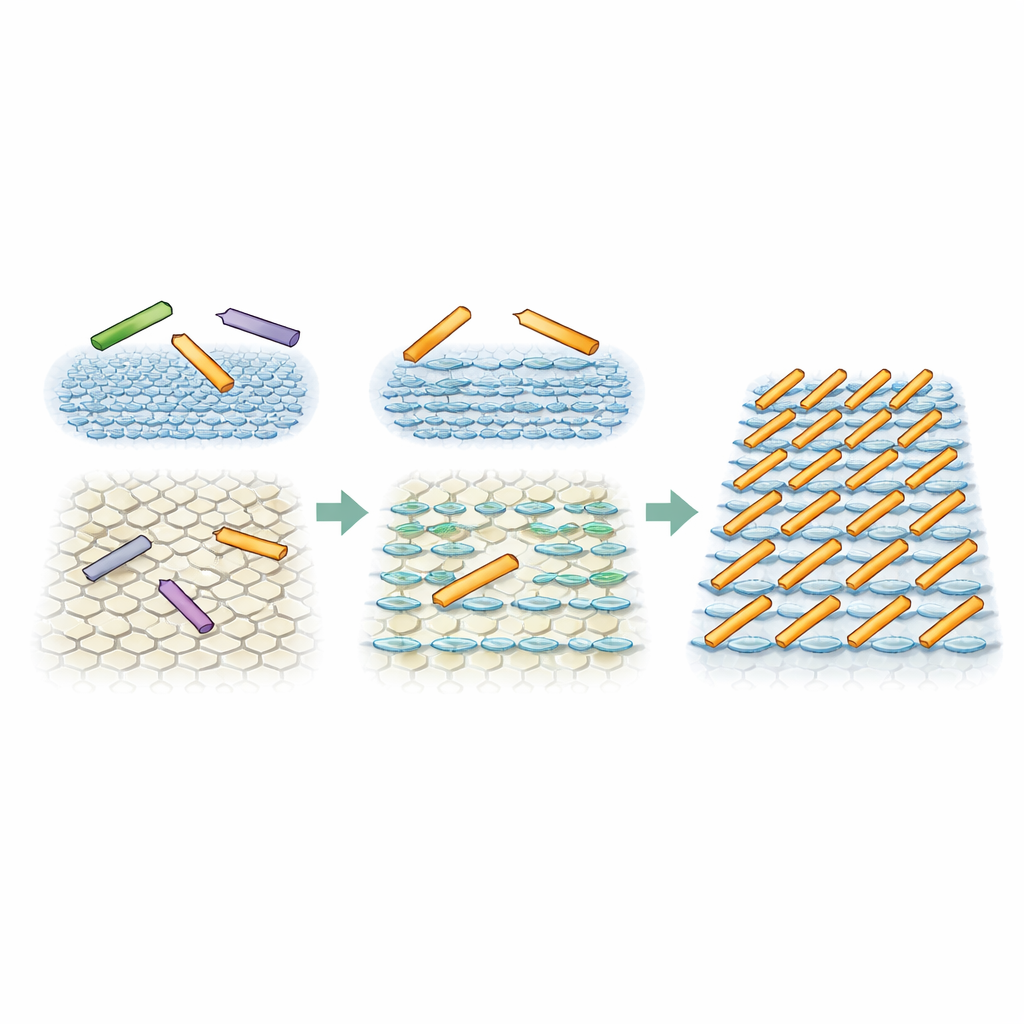
Le simulazioni rivelano una fase inaspettata
Per verificare se un bias direzionale sottile dall'ambiente della superficie potesse davvero spiegare i pattern osservati, i ricercatori hanno eseguito simulazioni Monte Carlo di semplici rettangoli rigidi che rappresentano le aste proteiche. In un set di simulazioni, tutte e tre le orientazioni erano ugualmente probabili, imitando la superficie completamente simmetrica. In quel caso, le aste restavano in uno stato ad alta densità ma disordinato, con solo allineamenti temporanei o limitati, proprio come osservato su un tipo di mica. In un secondo set, una direzione è stata resa solo modestamente più favorevole—circa il doppio di probabilità rispetto alle altre due—a rappresentare l'influenza degli strati d'acqua a strisce. In queste condizioni, e quando le aste potevano muoversi a sufficienza, il sistema evolveva naturalmente verso uno stato con file parallele regolarmente spaziate. Si tratta di una cosiddetta fase smectica, che la teoria di lunga data dice non dovrebbe apparire per aste non interagenti in due dimensioni, eppure la piccola spinta direzionale dall'interfaccia l'ha resa stabile.
Riconsiderare come progettiamo materiali bio‑ispirati
In termini semplici, questo lavoro mostra che una chimica proteina–superficie finemente sintonizzata non è sufficiente per prevedere come proteine progettate si disporranno su materiali reali. L'acqua che si trova tra la proteina e il solido, e il modo in cui il cristallo rompe sottilmente la simmetria, possono indirizzare l'assemblaggio verso pattern che i modelli dei manuali non prevederebbero mai. Combinando microscopia ad alta velocità, apprendimento automatico per quantificare l'ordine e simulazioni basate sulla fisica, lo studio delinea un modo per incorporare questi effetti nascosti di solvente e simmetria negli strumenti futuri di progettazione delle proteine. Per chiunque speri di ingegnerizzare materiali ibridi bio‑inorganici affidabili, il messaggio è chiaro: bisogna progettare non solo per la proteina e la superficie, ma anche per lo strato d'acqua strutturato che li connette.
Citazione: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Parole chiave: auto-assemblaggio delle proteine, interfacce liquido-solido, struttura dell'acqua interfacciale, ordinamento smectico, materiali bioispirati