Clear Sky Science · it
Un meccanismo adattatore multivalente guida l’importazione nucleare dei proteasomi
Come le cellule mantengono pulita la loro sala di controllo
All’interno di ogni cellula, il nucleo funge da centro di comando, pieno di DNA e delle proteine che regolano quali geni vengono attivati o spenti. Per mantenere questa sala di controllo in efficienza, le cellule si affidano a potenti “trituratori” molecolari chiamati proteasomi che degradano le proteine usurate o malfunzionanti. Questo articolo rivela come le cellule gestiscono il compito sorprendentemente complesso di trasportare questi ingombranti proteasomi attraverso i stretti passaggi verso il nucleo nel momento giusto.
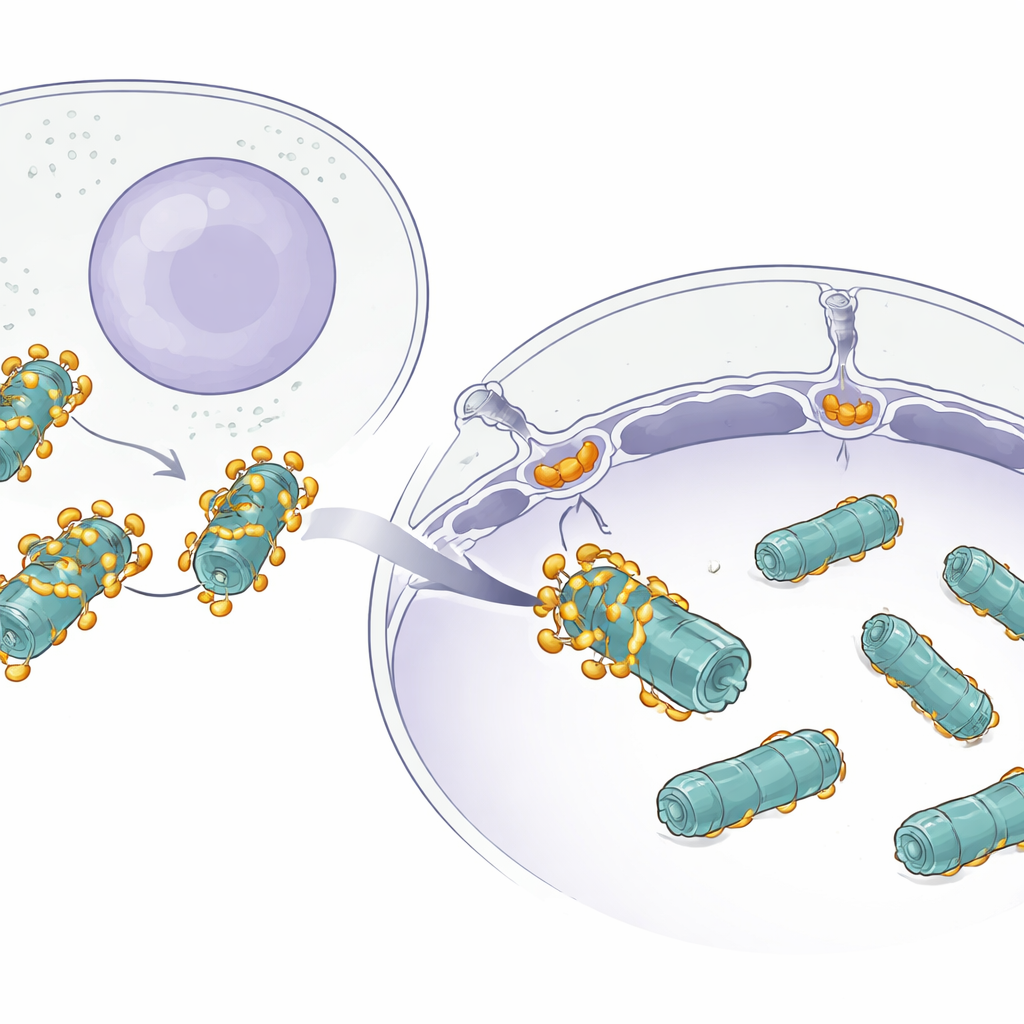
La sfida di muovere grandi macchine
Molte proteine si spostano silenziosamente tra il citoplasma e il nucleo attraverso gigantesche porte nell’involucro nucleare note come pori nucleari. Le piccole proteine possono attraversare facilmente, ma macchine grandi come i proteasomi sono diverse: si tratta di complessi massicci a forma di barile costruiti da molte subunità. Sebbene gli scienziati sapessero già che i piccoli carichi usano proteine ausiliarie chiamate importine per entrare nel nucleo, non era chiaro come qualcosa di grande quanto un proteasoma si infilasse attraverso questi passaggi in modo efficiente senza incastrarsi o perdersi.
Un aiuto che cambia forma prende corpo
Il gruppo si è concentrato su una piccola proteina flessibile chiamata AKIRIN2, che lavori precedenti avevano mostrato essere indispensabile perché i proteasomi possano entrare nel nucleo. Le cellule che si dividono senza AKIRIN2 non riescono a portare i proteasomi nel nucleo e muoiono rapidamente perché le proteine nucleari danneggiate si accumulano. Usando una combinazione di metodi – inclusa una vasta scansione mutazionale che ha alterato quasi ogni amminoacido di AKIRIN2, la crio-microscopia elettronica ad alta risoluzione per visualizzare il complesso in 3D e accurati test biochimici – i ricercatori hanno mappato quali parti di AKIRIN2 sono importanti e cosa fanno. Hanno scoperto un segmento a “ala” precedentemente non apprezzato e una regione a elica che consente ad AKIRIN2 di formare dimeri (coppie), entrambe fondamentali per aggrapparsi ai proteasomi e ad altri partner.
Costruire una maniglia di trasporto a più mani
Le immagini strutturali hanno rivelato che più copie di AKIRIN2 si raggruppano su un lato del proteasoma come tante mani che afferrano lo stesso oggetto. Ogni coppia di AKIRIN2 si lega a punti specifici sulla superficie esterna del proteasoma coinvolgendo contemporaneamente diverse importine. Un’importina, IPO9, si attacca ad AKIRIN2 in modo insolito, avvolgendola e cambiando conformazione mentre il complesso si assemblea. Altre importine, che agiscono a loro volta in coppia, riconoscono brevi segnali di ingresso nucleare portati da AKIRIN2. Poiché diverse molecole di AKIRIN2 si trovano sullo stesso proteasoma, esse espongono collettivamente molti di questi segnali allo stesso tempo. Questa “maniglia” multivalente permette a un gruppo di importine di agganciarsi simultaneamente, fornendo al grande proteasoma la forza di trazione necessaria per attraversare il poro nucleare.
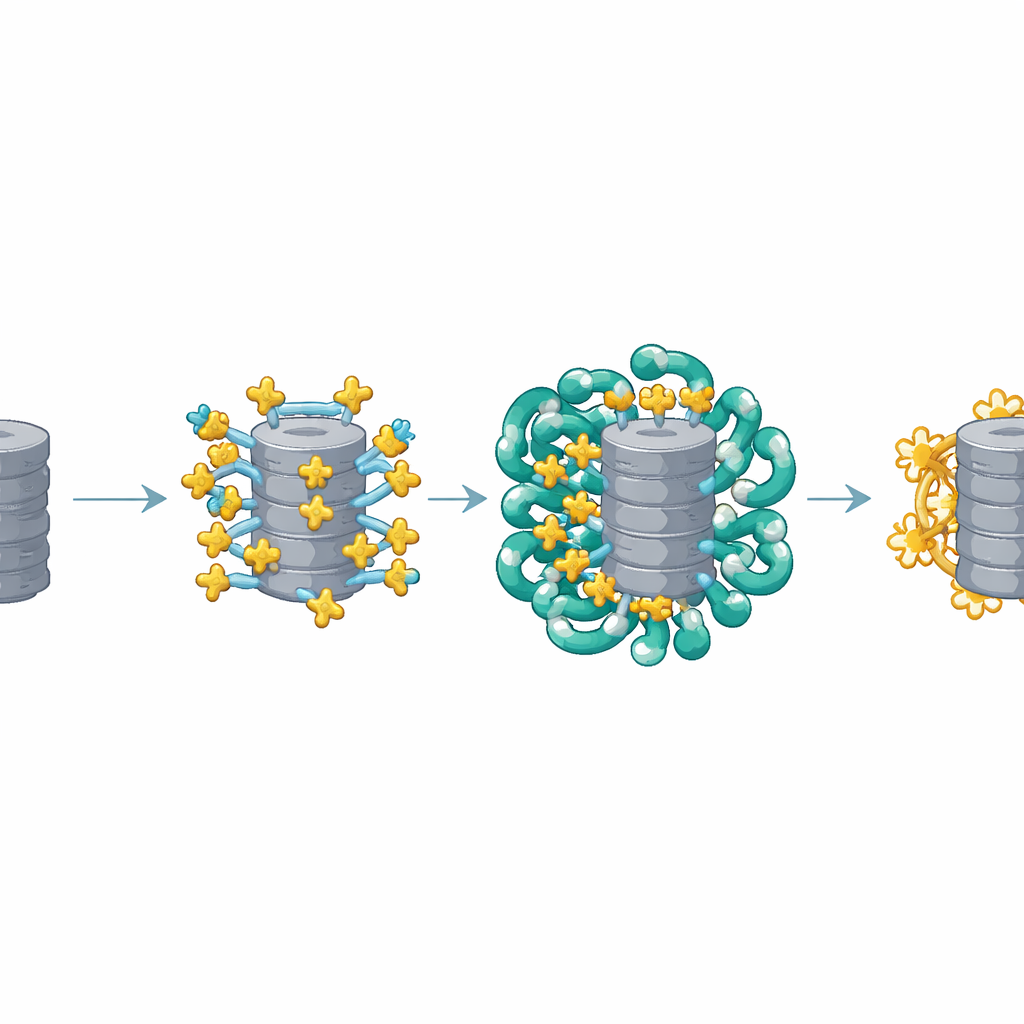
Un ciclo intelligente di assemblaggio e rilascio
Esperimenti di ricostituzione in un sistema semplificato in provetta hanno mostrato che i proteasomi entrano efficientemente nei nuclei solo quando sia AKIRIN2 sia le importine sono presenti insieme. Più AKIRIN2 c’è, più forte e veloce è l’importazione. Una volta all’interno del nucleo, la macchina di trasporto deve essere rimossa affinché i proteasomi possano lavorare. Qui la cellula usa un rilascio in due fasi. Una piccola proteina switch chiamata Ran, nella sua forma legata a GTP, stacca la maggior parte delle importine dal loro carico. AKIRIN2 e qualche IPO9 resistono più a lungo, ma il nucleo ha un piano di riserva: i proteasomi nucleari degradano direttamente AKIRIN2 stessa, senza il solito marchio con l’ubiquitina. Misurazioni nel corso del ciclo cellulare mostrano che AKIRIN2 raggiunge il picco durante la divisione cellulare, quando si formano nuovi nuclei, per poi diminuire in G1 precoce, coerente con questa pulizia mirata.
Perché questo è importante oltre una singola proteina
Nel loro insieme, questi risultati mostrano che AKIRIN2 funge da impalcatura flessibile che raggruppa molte importine su un singolo proteasoma, trasformando un problema di trasporto difficoltoso in uno sforzo coordinato di gruppo. Concentrando i segnali di ingresso nucleare su un adattatore anziché sul proteasoma stesso, le cellule possono controllare quando e con quale intensità le grandi macchine entrano nel nucleo senza riprogettarle. Strategie basate su adattatori simili sembrano essere usate per altri grandi complessi proteici, e persino i virus sfruttano trucchi correlati per invadere il nucleo. Comprendere questa logica generale del trasporto approfondisce la nostra visione di come le cellule mantengono l’equilibrio proteico nel loro compartimento più sensibile e potrebbe alla fine indicare nuovi modi d’intervenire quando la degradazione proteica o la funzione nucleare si alterano.
Citazione: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Parole chiave: trasporto nucleare, proteasoma, AKIRIN2, importina, degradazione proteica