Clear Sky Science · it
Chimica dell’elettrolita con domini a legami idrogeno adattivi per batterie al litio metallico ad alta tensione
Perché questa nuova ricetta per batterie è importante per te
Le batterie al litio metallico promettono dispositivi delle dimensioni di uno smartphone che durano giorni e auto elettriche che percorrono distanze maggiori con una singola carica. Tuttavia queste batterie tendono a degradarsi prematuramente o a guastarsi in modo pericoloso quando vengono caricate a tensioni elevate. Questo studio introduce un nuovo modo di “cucinare” il liquido all’interno di tali batterie in modo che gli ioni di litio si muovano rapidamente e in sicurezza, consentendo di coniugare elevata energia e lunga durata. Lo fa rimodellando il modo in cui le molecole si aggregano e interagiscono nel liquido, usando legami idrogeno progettati con cura.
Riconsiderare il cuore liquido della batteria
In qualsiasi batteria ricaricabile, l’elettrolita liquido è l’autostrada lungo la quale gli ioni di litio viaggiano tra l’elettrodo negativo e quello positivo. Nei progetti ad alta energia odierni, spingere la tensione oltre circa 4,5 volt rende questa autostrada affollata e instabile. Si formano aggregati di ioni e molecole del solvente che diventano grandi e rallentati, ostacolando il movimento ionico, mentre il liquido stesso si decompone alle superfici degli elettrodi. Gli autori pongono una domanda semplice ma potente: invece di limitarsi a cambiare la concentrazione di sale o ad aggiungere additivi casuali, è possibile scolpire deliberatamente minuscoli quartieri molecolari che guidino gli ioni in modo più efficiente e proteggano gli elettrodi?

Costruire minuscoli quartieri legati da legami idrogeno
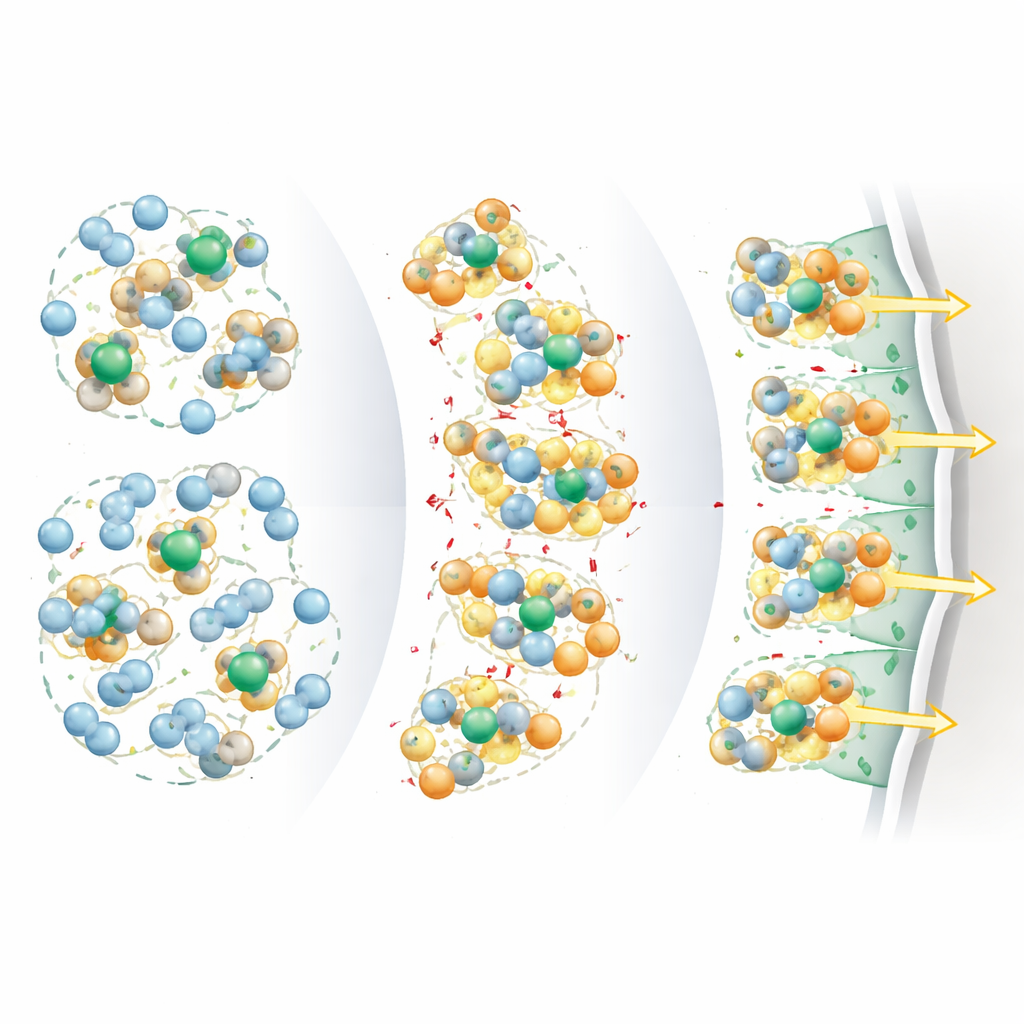
Il gruppo si è rivolto a una piccola molecola organica chiamata 2-ciano-N-metilacetamide (ANM), selezionata tramite ampi calcoli computazionali della sua struttura elettronica. ANM può donare legami idrogeno in due modi: un tipo più familiare, in cui un atomo di idrogeno leggermente positivo interagisce con un atomo di ossigeno, e un tipo “non classico”, in cui un atomo di azoto coinvolge un idrogeno legato al carbonio. Quando miscelata in un elettrolita carbonato comune con un sale di litio, ANM forma domini compatti a scala nanometrica legati da legami idrogeno attorno alle molecole del solvente. Questi domini indeboliscono sottilmente l’adesione degli ioni di litio al solvente circostante, invitando anioni carichi negativamente nel guscio più interno attorno al litio e riducendo la dimensione complessiva degli agglomerati ionici.
Creare corsie veloci per gli ioni di litio
Questi cluster riorganizzati offrono due vantaggi principali. Primo, i gusci di solvatazione più compatti e ricchi di anioni e i cluster complessivi più piccoli creano percorsi più diretti e meno tortuosi per il movimento degli ioni di litio attraverso il liquido, aumentando la conduttività nonostante la soluzione risulti più viscosa. Le misure mostrano una frazione significativamente maggiore di corrente trasportata dagli ioni di litio e barriere energetiche inferiori per il passaggio degli ioni attraverso i film protettivi sugli elettrodi. Secondo, poiché ANM ancora e orienta le molecole di solvente vicine, ne riduce la tendenza a degradarsi a tensioni molto elevate. Al contrario, sono gli anioni a decomporsi per primi alle superfici degli elettrodi, formando interfasi sottili ricche di componenti inorganici che conducono gli ioni ma sono isolanti elettricamente—esattamente ciò che serve per sopprimere reazioni secondarie dannose e la crescita dendritica del litio.
Proteggere entrambi i lati della batteria
Sul lato del litio metallico, l’elettrolita a base di ANM favorisce una deposizione uniforme del litio, formando un film superficiale robusto e in gran parte inorganico ricco di composti quali fluoruro di litio e nitruro di litio. Questo rivestimento supporta un rapido trasporto ionico resistendo ulteriori attacchi chimici, portando a cicli più regolari e a meno strutture filamentose di litio che potrebbero cortocircuitare la cella. Sul lato del catodo ad alta tensione, specialmente con materiali ricchi di nichel e particolarmente sollecitati, la stessa chimica dell’elettrolita rallenta la degradazione delle molecole del solvente e riduce la perdita di metalli di transizione dalla rete cristallina. Studi avanzati con raggi X e microscopia mostrano che i catodi ciclicizzati in questo elettrolita mantengono una struttura più ordinata, film superficiali più sottili e uniformi e meno crepe, anche quando spinti a 4,7–4,8 volt.
Dal concetto di laboratorio alle prestazioni pratiche
Questi cambiamenti a livello molecolare si traducono in guadagni notevoli a livello di dispositivo. Celle a moneta che utilizzano l’elettrolita contenente ANM e un catodo ricco di nichel ad alto carico mantengono quasi quattro quinti della loro capacità dopo 400 cicli a 4,7 volt, con un’efficienza di carica-scarica molto elevata. L’approccio scala inoltre a celle a sacchetto più grandi con spessori di elettrodo realistici, quantità ridotte di elettrolita e litio metallico sottile. In queste condizioni severe, simili ad applicazioni reali, le celle raggiungono energie specifiche superiori a 400 wattora per chilogrammo e mantengono la maggior parte della capacità attraverso decine di cicli ad alta tensione, superando di gran lunga le celle che usano una miscela di elettrolita convenzionale.
Cosa significa questo per le batterie future
Trattando il legame idrogeno come uno strumento di progettazione invece che come un effetto collaterale, questo lavoro propone un nuovo principio per la creazione dei liquidi per batterie: usare domini adattivi legati da legami idrogeno per ridurre gli agglomerati ionici, favorire gusci ricchi di anioni e costruire film superficiali protettivi e inorganici su entrambi gli elettrodi. In termini chiari, i ricercatori hanno dimostrato come sottili riorganizzazioni delle “amicizie” molecolari nel liquido possano domare una chimica di batteria molto energetica. Se estesa e perfezionata, questa strategia potrebbe contribuire ad avvicinare all’uso quotidiano batterie al litio metallico ad alta tensione più sicure e durature per elettronica, veicoli elettrici e accumulo di rete.
Citazione: Yang, Z., Zeng, L., Ju, Z. et al. Electrolyte chemistry of adaptive hydrogen bonded domains for high voltage lithium metal batteries. Nat Commun 17, 2379 (2026). https://doi.org/10.1038/s41467-026-69160-2
Parole chiave: batterie al litio metallico, progettazione dell’elettrolita, legame a idrogeno, catodi ad alta tensione, stoccaggio di energia