Clear Sky Science · it
Un approccio integrativo di biologia strutturale rivela l’organizzazione dinamica del complesso chaperone quaternario R2SP
Come le cellule costruiscono macchine molecolari complesse
All’interno di ogni cellula, molte proteine non funzionano da sole: devono incastrarsi in macchine elaborate prima di poter svolgere il loro compito. Eseguire correttamente questa fase di assemblaggio è essenziale per una respirazione sana, il movimento e persino la fertilità. Questo articolo esplora uno di questi assistenti all’assemblaggio, una “squadra di costruzione” molecolare chiamata complesso R2SP, e mostra come è organizzata e come opera. Capire R2SP è importante perché quando i suoi componenti falliscono, piccole strutture simili a peli sulla superficie cellulare, chiamate ciglia, non si muovono correttamente, provocando problemi respiratori cronici e altre malattie.
Le squadre di costruzione cellulari R2TP e R2SP
Le cellule si affidano a gruppi di proteine helper, noti come complessi chaperone, per guidare altre proteine verso la corretta conformazione multiparte. Una squadra studiata a lungo, chiamata R2TP, si trova in molti tessuti e aiuta ad assemblare grandi macchine come le fabbriche di RNA e i sensori del danno al DNA. R2SP è una stretta cugina di R2TP: entrambi sono costruiti attorno allo stesso motore ad anello, composto da due proteine partner, RUVBL1 e RUVBL2, che consumano la molecola energetica ATP. Ciò che differisce sono gli adattatori accessori che collegano i clienti a questo motore. R2TP utilizza adattatori chiamati RPAP3 e PIH1D1, mentre R2SP usa SPAG1 e PIH1D2. Queste piccole differenze nei componenti conferiscono ai due complessi elenchi di clienti diversi e collegano in particolare R2SP alla costruzione delle ciglia mobili che spazzano muco e fluidi attraverso i tessuti.
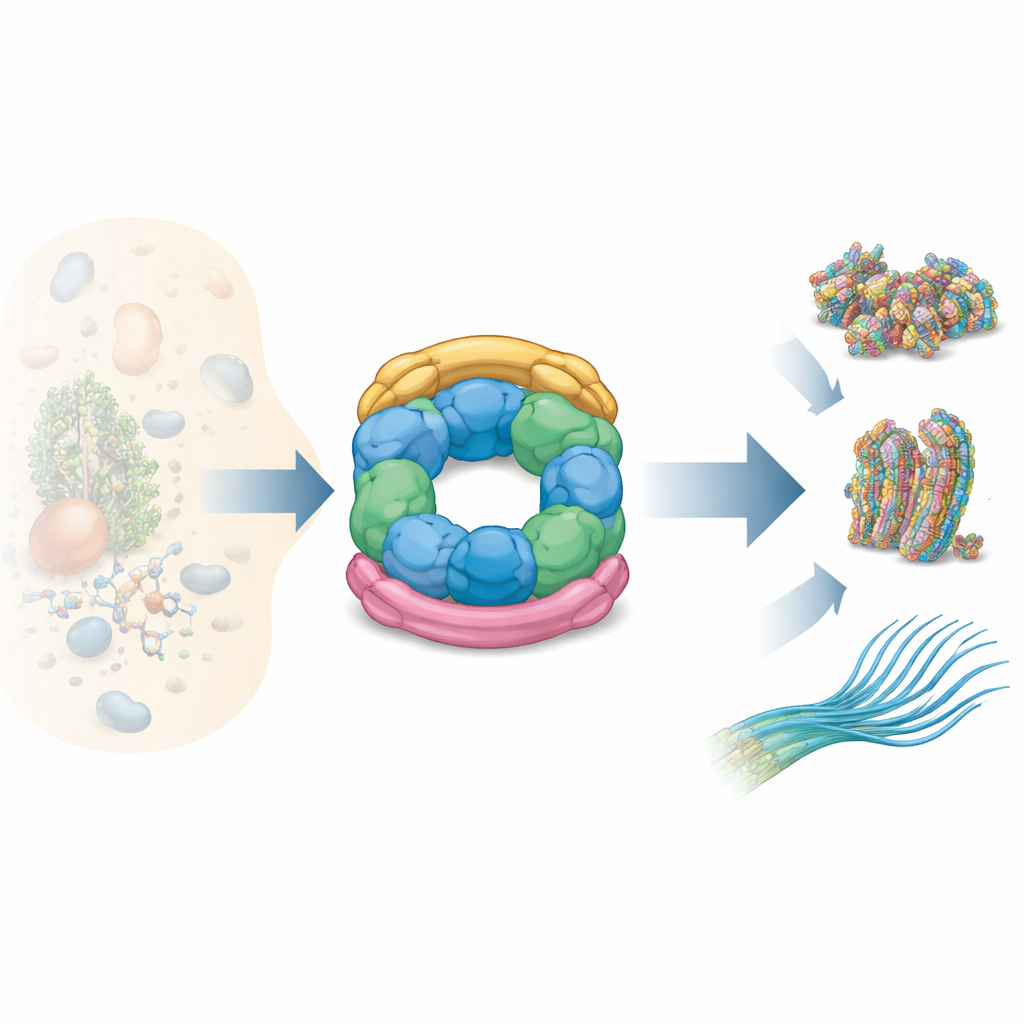
Come si incastrano le parti di R2SP
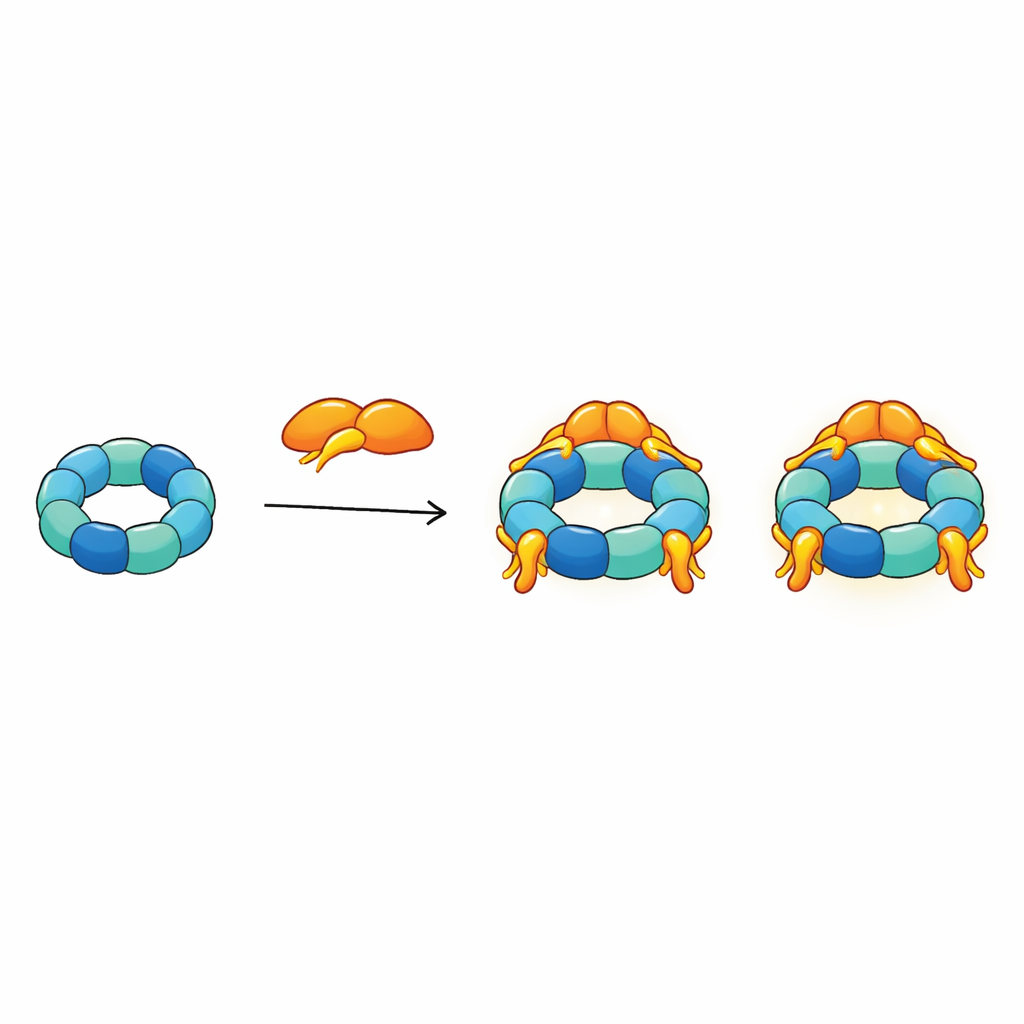
Gli autori hanno combinato diverse tecniche strutturali — risonanza magnetica nucleare, crio‑microscopia elettronica e spettrometria di massa con cross‑linking — con test biochimici per mappare la costruzione di R2SP. Hanno mostrato che l’estremità a coda di SPAG1 afferra l’anello RUVBL1/RUVBL2 in modo simile a come RPAP3 si lega in R2TP, ma con variazioni chiave nella forma e nei punti di contatto. Un secondo adattatore, PIH1D2, si inserisce sotto l’anello e raggiunge anche i domini laterali flessibili del motore. Questi domini laterali agiscono come bracci articolati che aiutano a trasmettere i movimenti dal nucleo consumatore di ATP ai clienti legati. I dati rivelano che SPAG1 e PIH1D2 non si attaccano in modo indipendente: cooperano, formando un’unità accoppiata che serraglia l’anello dall’alto e dal basso, stabilizzando un’architettura tridimensionale caratteristica.
Un anello dinamico che cambia marcia
Oltre alle immagini statiche, il gruppo ha indagato il comportamento dinamico di R2SP. Misurando le interazioni, hanno scoperto che il motore RUVBL1/RUVBL2 può esistere come un singolo anello o come un anello doppio impilato. Quando SPAG1 e PIH1D2 si legano, spostano fortemente questo equilibrio verso la forma a singolo anello e possono decorarlo con fino a tre coppie di adattatori. Allo stesso tempo, gli adattatori aumentano notevolmente l’attività di idrolisi dell’ATP del motore e ne modificano la velocità di associazione e dissociazione di molecole simili all’ATP dai siti attivi. Rispetto al sistema R2TP, SPAG1 e PIH1D2 favoriscono passaggi differenti nel rilascio del nucleotide, suggerendo che R2SP regola il ciclo energetico del motore centrale in modo caratteristico. Questo uso dell’energia finemente controllato si pensa sia ciò che guida l’assemblaggio passo dopo passo dei complessi cliente necessari per le ciglia mobili.
Una piattaforma flessibile per costruire componenti ciliare
Integrando tutte le restrizioni strutturali in un unico modello, gli autori propongono che R2SP funzioni come una piattaforma flessibile con molti bracci. La coda di SPAG1 si ancora saldamente sulla sommità dell’anello, mentre le sue altre regioni e i due domini di PIH1D2 si estendono verso il lato del motore più aperto e a forma di braccio. È su questo lato che le proteine cliente e i chaperoni ausiliari come HSP70 e HSP90 probabilmente si agganciano. Poiché fino a tre unità SPAG1–PIH1D2 possono attaccarsi a un singolo anello e i bracci flessibili sono in continuo movimento, l’intero complesso somiglia a un polpo i cui tentacoli possono afferrare più pezzi cliente contemporaneamente, coordinarli e passarli per essere assemblati in strutture ciliare più ampie.
Cosa significa per la salute e la malattia
Per i non specialisti, il messaggio principale è che R2SP è una versione specializzata di una macchina cellulare generale, riconfigurata mediante lo scambio di soli due adattatori proteici. Questo scambio modifica sia il controllo del motore centrale sia il posizionamento dei clienti, spiegando perché R2SP si concentra sulla costruzione di parti per le ciglia mobili mentre R2TP serve altre “fabbriche” cellulari. Difetti in SPAG1 sono già noti per causare dischinezia ciliare primaria, un disturbo caratterizzato da infezioni croniche e problemi di fertilità. Rivelando la disposizione dettagliata e i principi operativi di R2SP, questo studio pone le basi per comprendere come mutazioni specifiche interrompono l’assemblaggio delle ciglia e potrebbe, in futuro, guidare trattamenti mirati che ripristinino o modulino questa cruciale squadra di costruzione molecolare.
Citazione: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Parole chiave: chaperoni molecolari, assemblaggio di complessi proteici, ciglia mobili, biologia strutturale, RUVBL1 RUVBL2