Clear Sky Science · it
Base strutturale della traduzione mitocondriale efficiente mediata da TACO1
Mantenere fluide le centrali energetiche della cellula
I mitocondri sono spesso definiti le centrali energetiche delle nostre cellule perché producono la molecola energetica ATP. Per farlo devono sintetizzare un piccolo ma essenziale insieme di proteine usando le proprie macchine proteiche specializzate, chiamate mitoribosomi. Questo studio svela come una proteina ausiliaria poco nota, TACO1, regoli finemente queste macchine in modo che possano funzionare senza intoppi, soprattutto quando incontrano tratti di catena proteica particolarmente “inguacchiati” che tendono a bloccare il meccanismo.
Centrali energetiche con hardware proprio
A differenza della maggior parte della sintesi proteica, che avviene nel citoplasma acquoso della cellula, la produzione di proteine mitocondriali si svolge sui mitoribosomi ancorati alla membrana interna del mitocondrio—la stessa membrana che ospita molti enzimi coinvolti nella produzione di energia. Utilizzando la criomicroscopia elettronica all’avanguardia su mitocondri umani intatti, gli autori hanno ottenuto istantanee quasi atomiche di questi mitoribosomi nel loro contesto naturale. Hanno osservato che tutti i mitoribosomi catturati erano attaccati alla membrana interna e orientati in modo che le catene proteiche neoformate possano alimentare direttamente un insertasi di membrana, una sorta di fessura molecolare che inserisce le nuove proteine nella membrana dove sono necessarie per la produzione di energia. 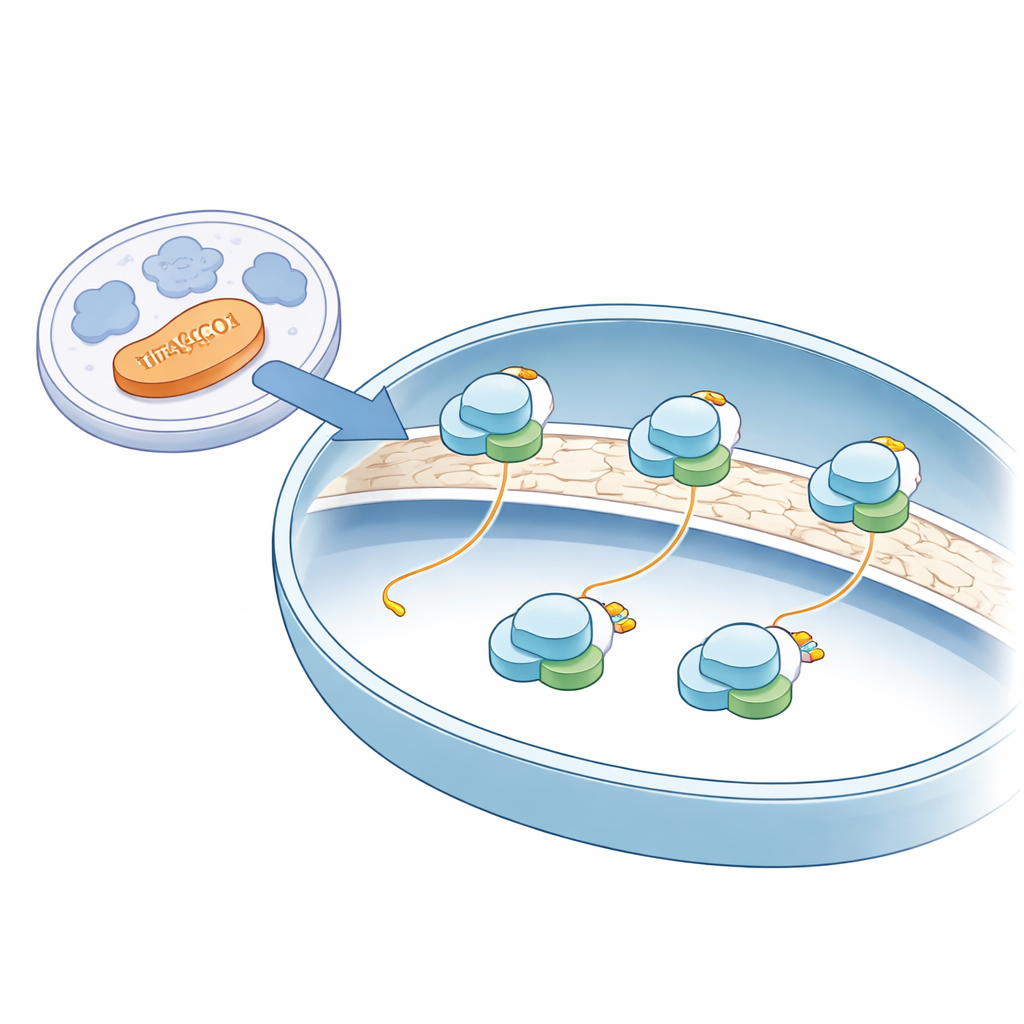
Un aiutante nascosto prende forma
Tra i componenti ribosomali, i filamenti di RNA e le catene proteiche in crescita, i ricercatori hanno notato una macchia di densità extra che non era mai stata vista nelle preparazioni precedenti, più artificiali. Raffinando con cura le loro mappe e confrontando le forme con strutture proteiche predette, hanno identificato questo componente misterioso come TACO1, una proteina già collegata a malattie mitocondriali umane ma il cui ruolo fisico era rimasto oscuro. Le immagini hanno rivelato che TACO1 si adagia accanto alla parte del ribosoma dove arriva il tRNA carico del prossimo amminoacido (sito A), stabilendo contatti sia con l’RNA ribosomiale sia con diverse proteine ribosomiali. Questo posizionamento permette a TACO1 di funzionare quasi come una staffa, sostenendo il tRNA in arrivo mentre il ribosoma forma un nuovo legame per allungare la catena proteica.
Prevenire gli ingorghi sulla linea di assemblaggio delle proteine
La sintesi proteica procede in ciclo: un fattore di elongazione (mtEF‑Tu) consegna un tRNA carico, il ribosoma lo verifica e lo utilizza, e il fattore se ne va così che il passo successivo possa avere luogo. Gli autori hanno scoperto che TACO1 si lega grosso modo nella stessa regione usata da mtEF‑Tu, e che i due fattori non possono occupare il ribosoma contemporaneamente. Nelle cellule normali, molti mitoribosomi apparivano in uno stato in cui il nuovo tRNA è completamente al suo posto e l’allungamento procede. Quando il gruppo ha esaminato mitocondri di cellule prive di TACO1, ha invece osservato un accumulo di ribosomi bloccati in uno stato precedente in cui mtEF‑Tu è ancora attaccato e il nuovo tRNA non si è stabilizzato del tutto. Esperimenti biochimici hanno confermato che, senza TACO1, mtEF‑Tu persiste più a lungo sui ribosomi attivamente in traduzione e le subunità maggiore e minore tendono a separarsi più facilmente—segni di traduzione bloccata o fallita. 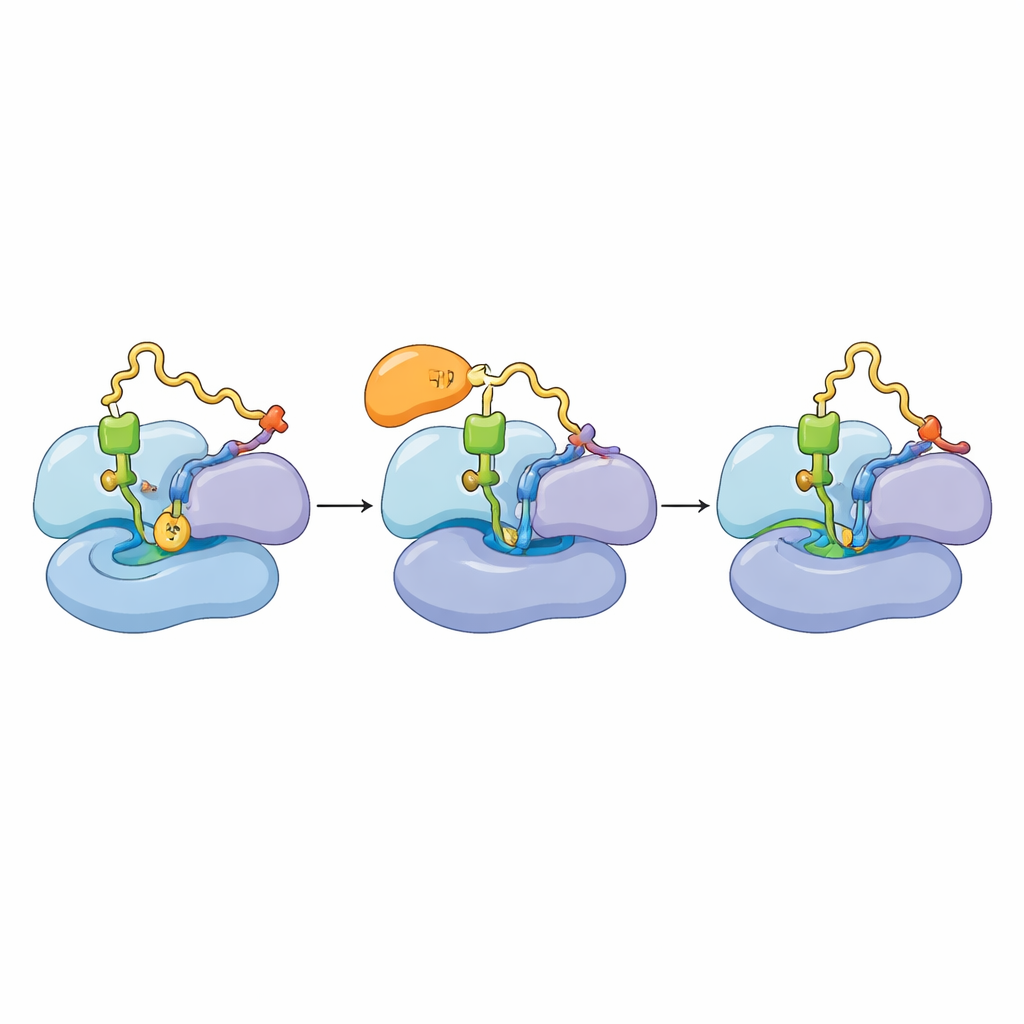
Perché certi tratti proteici sono così problematici
Uno dei compiti più importanti di TACO1 sembra essere l’aiuto al ribosoma nel superare sequenze di prolina, amminoacido che rallenta naturalmente la formazione di legami a causa della sua struttura ad anello rigida. Lavori precedenti avevano mostrato che TACO1 è cruciale per la produzione della subunità 1 della citocromo c ossidasi, un componente centrale della catena di produzione energetica che contiene un raro motivo di tripla prolina, e che la sua perdita provoca il collasso di questo complesso energetico e una malattia cerebrale umana nota come sindrome di Leigh. Nei batteri e nel sistema citoplasmatico principale della cellula, fattori ausiliari diversi svolgono una funzione anti‑blocco simile, ma i mitocondri sono privi di quei fattori convenzionali. Questo nuovo lavoro strutturale mostra che TACO1 si è evoluto come soluzione specifica per i mitocondri: spingendo via mtEF‑Tu, stabilizzando il tRNA in arrivo e sostenendo la formazione del legame, aiuta il mitoribosoma a superare questi tratti di sequenza difficili invece di fermarsi.
Una strategia antica con implicazioni per la salute moderna
Oltre alle cellule umane, proteine correlate a TACO1 si trovano in molti batteri e altri organismi, e alcune di queste versioni batteriche sono state ora dimostrate alleviare anch’esse i blocchi ribosomiali. Questa conservazione suggerisce che l’uso di un fattore simile a TACO1 per salvare ribosomi lenti o bloccati sia una strategia antica per mantenere efficiente la sintesi proteica. Per l’uomo, il lavoro fornisce una spiegazione concreta e visiva del perché le mutazioni in TACO1 possano danneggiare così gravemente la produzione di energia e il sistema nervoso, e suggerisce che manipolare TACO1 o i suoi parenti potrebbe un giorno offrire modi per modulare la traduzione mitocondriale—sia per trattare le malattie mitocondriali sia per colpire batteri dannosi che dipendono da sistemi simili di sollievo dal blocco.
Citazione: Wang, S., Brischigliaro, M., Zhang, Y. et al. Structural basis of TACO1-mediated efficient mitochondrial translation. Nat Commun 17, 2521 (2026). https://doi.org/10.1038/s41467-026-69156-y
Parole chiave: traduzione mitocondriale, TACO1, mitoribosoma, blocco del ribosoma, sindrome di Leigh