Clear Sky Science · it
Meccanismo molecolare dell’importazione di fosfato dal trasportatore batterico PstSCAB
Perché i nutrienti minuscoli contano
Ogni cellula vivente, dai neuroni umani ai batteri del suolo, dipende dal fosforo. Questo elemento aiuta a immagazzinare energia, costruire il DNA e mantenere l’integrità delle membrane cellulari. Tuttavia, nell’ambiente il fosfato utilizzabile — la forma di fosforo che le cellule possono effettivamente importare — è spesso scarso. Molti batteri patogeni si affidano a una macchina molecolare ultra-efficiente, chiamata trasportatore PstSCAB, per recuperare il fosfato quando è poco disponibile. Capire esattamente come funziona questa macchina non è solo una questione di scienza di base; potrebbe aprire la strada a nuovi modi per disarmare le infezioni privando i batteri di questo nutriente essenziale.
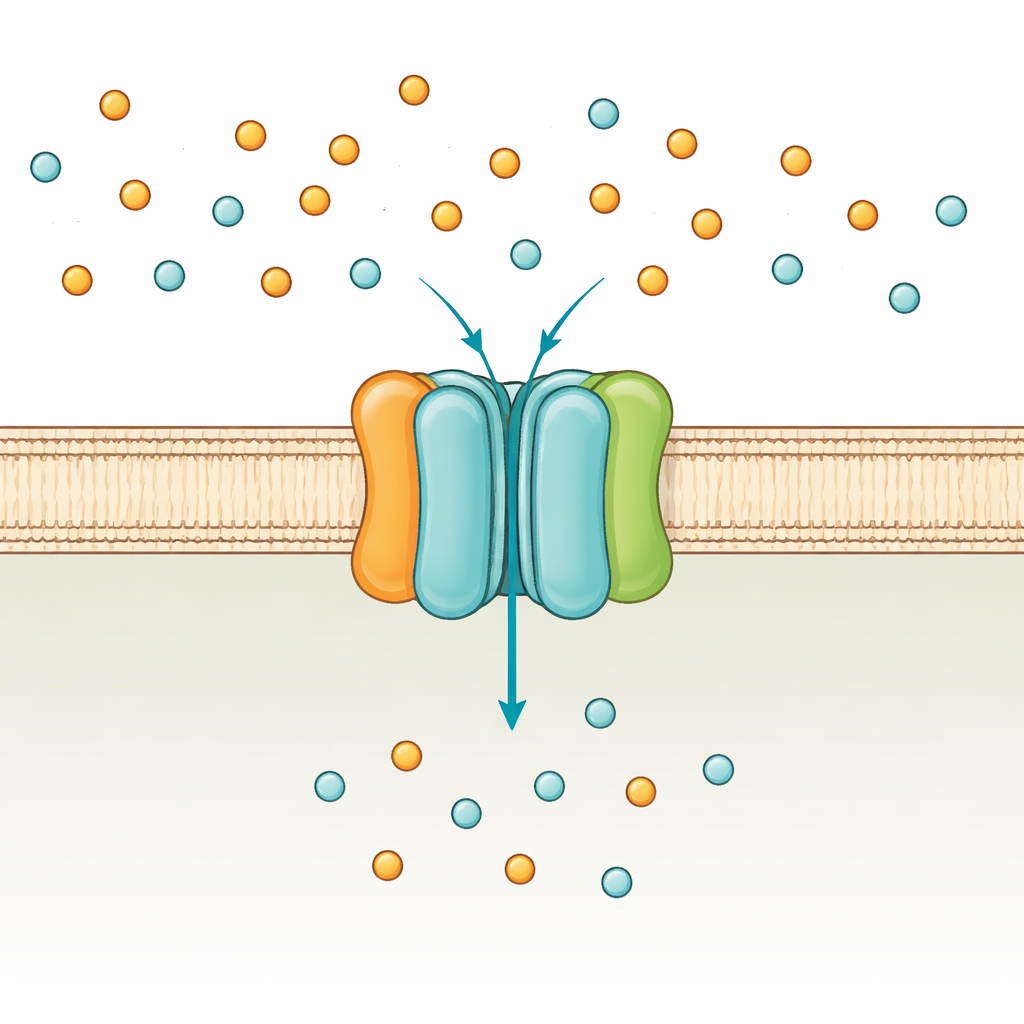
Il guardiano del fosfato della cellula
Batteri come Escherichia coli usano due vie principali per assorbire il fosfato: un sistema a bassa affinità che funziona quando il fosfato è abbondante e il sistema ad alta affinità PstSCAB che si attiva in condizioni di carenza. PstSCAB è inserito nella membrana cellulare ed è alimentato dall’ATP, la moneta energetica universale della cellula. È composto da cinque parti: due subunità transmembrana (PstA e PstC) che formano il passaggio, una proteina solubile “catturatrice” all’esterno della membrana (PstS) che afferra il fosfato e una coppia di subunità interne (PstB) che idrolizzano ATP per guidare il trasporto. Poiché questo sistema aiuta anche a controllare molti geni legati alla virulenza batterica, mutazioni in PstSCAB possono indebolire patogeni responsabili di infezioni del tratto urinario, sepsi negli animali da allevamento e tubercolosi.
Cogliere la macchina in azione
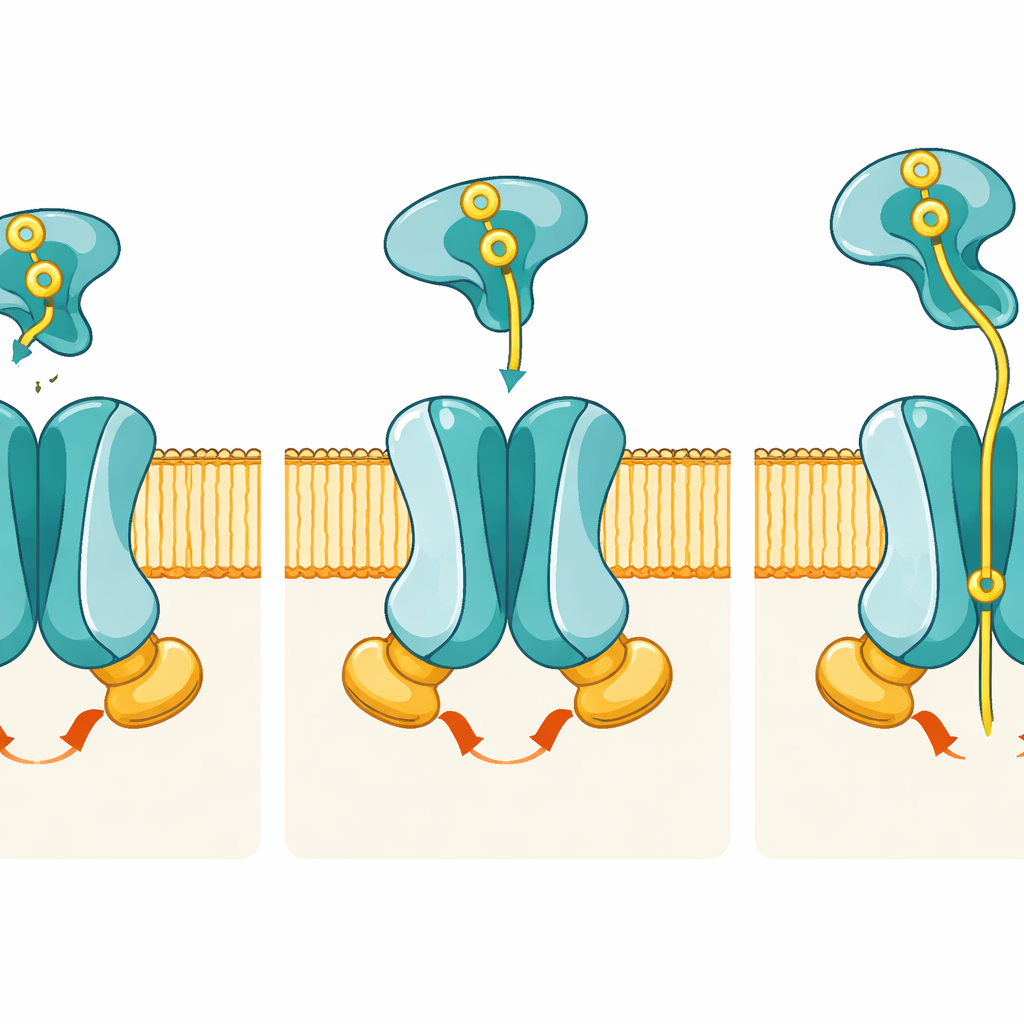
Fino ad ora, gli scienziati avevano solo viste parziali di PstSCAB, per lo più della sola proteina catturatrice PstS. In questo studio, i ricercatori hanno usato la crio-microscopia elettronica ad alta risoluzione per visualizzare l’intero trasportatore in diverse tappe chiave del suo ciclo di funzionamento. Hanno ricostituito le proteine batteriche in “nanodischi” di membrana artificiali e le hanno congelate così rapidamente che le molecole sono rimaste intrappolate a mezz’azione. Modificando con cura le proteine e aggiungendo o sottraendo ATP, hanno ottenuto strutture di tre stati principali: una forma di riposo rivolta verso l’interno senza la proteina catturatrice attaccata, uno stato pre-translocazione in cui la PstS carica di fosfato si aggancia al complesso di membrana, e un intermedio catalitico legato ad ATP in cui il fosfato è trattenuto all’interno del trasportatore.
Come i cambiamenti di forma spostano il fosfato
Le immagini rivelano come cambiamenti conformazionali coordinati trasferiscano il fosfato dall’esterno all’interno della cellula. Nello stato di riposo, il passaggio formato da PstA e PstC è aperto solo verso l’interno della cellula; il lato esterno è sigillato da un insieme di residui che fungono da “porta”, perciò il fosfato non può ancora entrare dall’esterno. Quando la PstS carica di fosfato si aggancia nello stato pre-translocazione, si adagia tra anse flessibili di PstA e PstC ma, sorprendentemente, le subunità di membrana cambiano forma molto poco. Lo spostamento reale avviene quando la PstS inizia ad aprire le sue due lobi per rilasciare il fosfato e, in concerto, le due subunità PstB si avvicinano per legare l’ATP. Questo legame ad ATP clampa PstB in un dimero e tira le eliche connettenti in PstA e PstC, capovolgendo l’intero poro in una conformazione rivolta verso l’esterno che espone una tasca specifica di legame per il fosfato verso l’ambiente esterno.
Una tasca su misura per il fosfato
Nella struttura rivolta verso l’esterno e legata ad ATP, gli autori individuano una densità nella regione centrale della membrana che corrisponde a uno ione fosfato. Questo ione è cullato da amminoacidi carichi positivamente — in particolare due arginine, una da PstA e una da PstC — che agiscono come dita molecolari che afferrano il fosfato carico negativamente. Le simulazioni al computer mostrano che il fosfato rimane stabilmente legato in questa tasca per microsecondi, e esperimenti genetici ne confermano l’importanza: quando questi residui chiave sono mutati, il trasportatore continua ad idrolizzare ATP ma importa fosfato molto male. Questa separazione tra “dove si spende energia” e “dove viene riconosciuto il carico” evidenzia quanto sia finemente sintonizzata la macchina per il fosfato.
Dalle istantanee strutturali alla promessa medica
Nel loro insieme, le strutture e i test biochimici di supporto delineano un ciclo completo: PstS cattura il fosfato all’esterno, si aggancia al trasportatore rivolto verso l’interno, quindi — accoppiato al legame e alla scissione dell’ATP da parte di PstB — induce un capovolgimento che trasferisce il fosfato nella tasca della membrana e infine all’interno della cellula. Dopo l’idrolisi dell’ATP, la macchina si rilassa tornando allo stato di riposo, pronta per un nuovo ciclo. Per un osservatore non specialistico, il messaggio chiave è che ora disponiamo di un progetto a livello atomico di come molti batteri sopravvivono in ambienti a basso contenuto di fosfato e regolano la loro virulenza. Questa mappa dettagliata può guidare la progettazione di farmaci, anticorpi o peptidi che bloccano il trasportatore o la sua proteina catturatrice, trasformando potenzialmente una porta essenziale per i nutrienti in un vulnerabile bersaglio terapeutico.
Citazione: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Parole chiave: trasporto del fosfato, assimilazione di nutrienti nei batteri, trasportatore ABC, PstSCAB, bersagli antibatterici