Clear Sky Science · it
Alchenilazione e alchinilazione selettive in fase finale su N‑Me di farmaci e amine terziarie non attivate mediante catalisi fotoredox
Perché ha senso modificare farmaci già esistenti
Molti dei farmaci odierni funzionano bene ma lasciano margini di miglioramento in termini di sicurezza, effetti collaterali o precisione del bersaglio biologico. I chimici sono sempre più interessati a «ritoccare» delicatamente farmaci esistenti in fasi avanzate dello sviluppo, piuttosto che inventare da zero nuove molecole. Questo studio mostra come fasci di luce visibile possano essere usati per agganciare nuovi gruppi a un comune blocco costruttivo dei farmaci, generando candidati antidepressivi migliorati e aprendo una via più rapida a terapie raffinate.
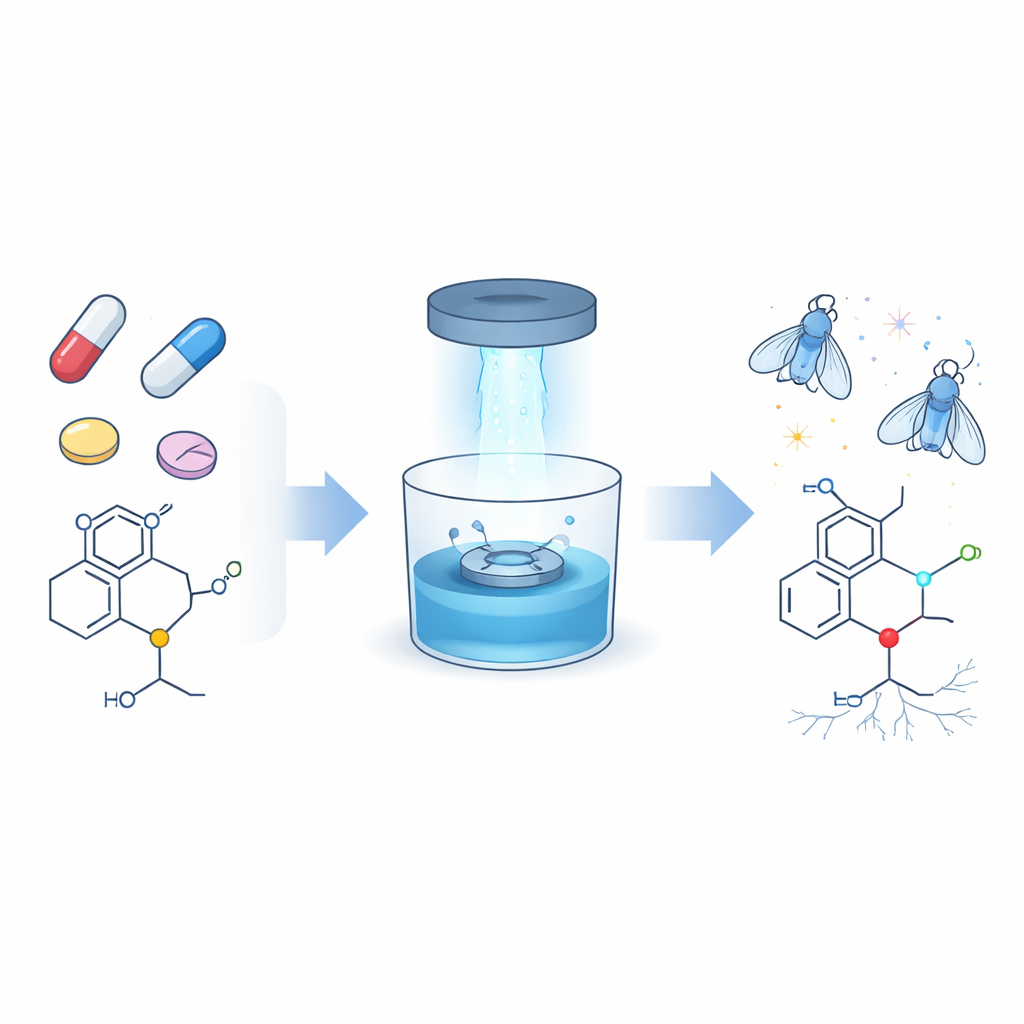
Aggiornare una caratteristica comune in molti farmaci
Una quota sorprendentemente ampia dei farmaci moderni—più di due su cinque—contiene frammenti ricchi di azoto chiamati amine, la maggior parte dei quali è del sottotipo noto come amine terziarie. Compaiono in antibiotici, farmaci antitumorali, antiallergici, analgesici e antidepressivi. Finora i chimici hanno faticato a modificare in modo selettivo una sola piccola parte di questi gruppi, l’unità N‑metile, quando è circondata da diversi legami carbonio–idrogeno quasi identici. Gli autori si sono proposti di sviluppare un metodo delicato e affidabile per attaccare nuovi “manici”, nello specifico doppi legami carbonio–carbonio (alcheni) e tripli legami (alchini), in posizione N‑metile senza alterare il resto della molecola del farmaco.
Usare la luce per riscrivere un legame alla volta
Il gruppo ha fatto ricorso alla catalisi fotoredox, una tecnologia che usa luce visibile e un catalizzatore fotosensibile per spostare singoli elettroni e innescare reazioni in condizioni blande. Nel loro sistema, la luce blu eccita un catalizzatore organico che temporaneamente sottrae un elettrone all’amina terziaria. Questo step genera un radicale di breve durata in posizione N‑metile che può unirsi a molecole partner scelte, portatrici di gruppi vinilici o alchinilici. Mettendo a punto le condizioni di reazione—scelta del solvente, base e additivi—i ricercatori hanno ottenuto rese elevate e controllo eccellente, in modo che il nuovo gruppo si leghi quasi esclusivamente alla posizione N‑metile, anche quando sono presenti più siti simili. Hanno dimostrato il metodo su un ampio pannello di amine semplici e poi su farmaci reali, tra cui antistaminici, cardiaci, antiinfettivi e diversi antidepressivi.
Dal ritocco chimico a una migliore azione antidepressiva
Per verificare se questi ritocchi strutturali potessero avere rilevanza medica, gli autori si sono concentrati sull’imipramina, un antidepressivo triciclico usato da lungo tempo. Hanno progettato e modellato oltre venti varianti di imipramina in cui l’estensione vinilica o alchinilica porta anelli aromatici in grado di inserirsi in una tasca idrofoba del trasportatore umano della serotonina, una proteina che regola i livelli del mediatore dell’umore serotonina. Il docking computazionale ha suggerito che molte di queste molecole modificate potrebbero legarsi altrettanto bene o meglio del farmaco parentale. I candidati più promettenti sono stati quindi sintetizzati con il nuovo metodo guidato dalla luce e testati in sistemi biologici: un modello di depressione nella Drosophila basato sull’isolamento sociale e, per i due composti migliori, in cellule nervose murine che trasportano attivamente la serotonina.
Come mosche e cellule hanno rivelato farmaci più efficaci
Nelle mosche maschio isolate, il comportamento simile alla depressione si manifesta con un’aggressività aumentata. Somministrare imipramina riduce questa aggressività, rispecchiando la sua azione antidepressiva nell’uomo. È notevole che diverse delle derivazioni di imipramina ottenute con il nuovo metodo abbiano ridotto l’aggressività altrettanto bene, e quattro candidati abbiano funzionato anche meglio dell’imipramina stessa. In cellule ippocampali murine coltivate, due composti leader hanno inibito il riassorbimento della serotonina più fortemente dell’imipramina, come confermato sia da misure chimiche dirette della serotonina sia da un colorante fluorescente che si illumina quando viene captato dalle cellule. Questi test indicano che sottili modifiche in fase finale alla posizione N‑metile possono realmente aumentare la potenza antidepressiva, e non solo modificare la molecola sulla carta.
Perché la reazione è così selettiva
Una domanda scientifica chiave era perché la reazione modifichi l’unità N‑metile in modo così netto quando altre posizioni vicine appaiono altrettanto reattive. Attraverso esperimenti di controllo, misure di spin elettronico e calcoli computazionali dettagliati, gli autori hanno mostrato che il punto decisionale cruciale non è quando il radicale si forma, ma quando quel radicale si addiziona al partner vinilico o alchinilico. Il percorso che porta dal radicale N‑metile al prodotto finale è sia energeticamente più favorevole sia molto più veloce rispetto a vie concorrenti, orientando di fatto la reazione verso un unico esito. Questa intuizione aiuta a spiegare l’elevata selettività e potrebbe guidare strategie analoghe su altre molecole complesse.
Cosa significa questo lavoro per i futuri farmaci
Nel complesso, lo studio introduce un modo pratico per aggiornare chirurgicamente farmaci esistenti che contengono amine terziarie, aggiungendo maniglie chimiche compatte in grado di modulare le loro interazioni con bersagli biologici o di collegarli ad altri componenti. Dimostrando che tali modifiche in fase finale possono trasformare un antidepressivo ben consolidato in varianti ancora più efficaci in modelli animali e cellulari semplici, il lavoro indica un potente incontro tra chimica sintetica moderna, calcolo e biologia. Man mano che l’approccio verrà esteso ad altri farmaci, potrebbe accelerare il perfezionamento di candidati farmacologici e contribuire a rinnovare terapie più datate con migliori prestazioni e sicurezza.
Citazione: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Parole chiave: catalisi fotoredox, funzionalizzazione in fase finale, amine terziarie, progettazione di farmaci antidepressivi, trasportatore della serotonina