Clear Sky Science · it
Un fosfaalumene(3) isolabile capace di attivare piccole molecole tramite modalità di reattività uniche
Rompere legami ostinati con un nuovo strumento chimico
I chimici cercano costantemente modi per convincere molecole refrattarie a reagire. Molte sostanze comuni, dall’idrogeno gassoso all’anidride carbonica, sono sorprendentemente stabili, il che le rende difficili da trasformare in prodotti utili. Questo articolo descrive una molecola di nuova concezione, formata da alluminio e fosforo, in grado di catturare questi partner riluttanti e di aprire i loro legami. Capire e controllare questo tipo di attivazione del legame potrebbe un giorno aiutare a trasformare gas di scarto in materie prime o offrire percorsi più miti e parchi di metallo per produrre prodotti chimici fini e materiali.
Un legame progettato tra alluminio e fosforo
Al centro dello studio c’è un tipo raro di connessione tra due elementi del main group: alluminio e fosforo. I ricercatori hanno costruito una molecola, denominata “3” nell’articolo, nella quale questi due atomi condividono un legame doppio ben definito. Per impedire che questa coppia reattiva si disgreghi, l’hanno avvolta in un ingombrante impalcatura organica che la protegge da reazioni accidentali. Con due diverse vie sintetiche hanno ottenuto il complesso in forma isolabile e sono riusciti a crescere cristalli singoli adatti alla diffrazione a raggi X, confermando che il fosforo è legato all’alluminio con un collegamento corto, simile a un doppio legame, mentre ogni atomo è sostenuto da leganti contenenti azoto. Calcoli teorici hanno mostrato che gli elettroni sono condivisi in modo diseguale tra alluminio e fosforo, rendendo il legame polarizzato e predisposto all’attacco da parte di altre molecole.
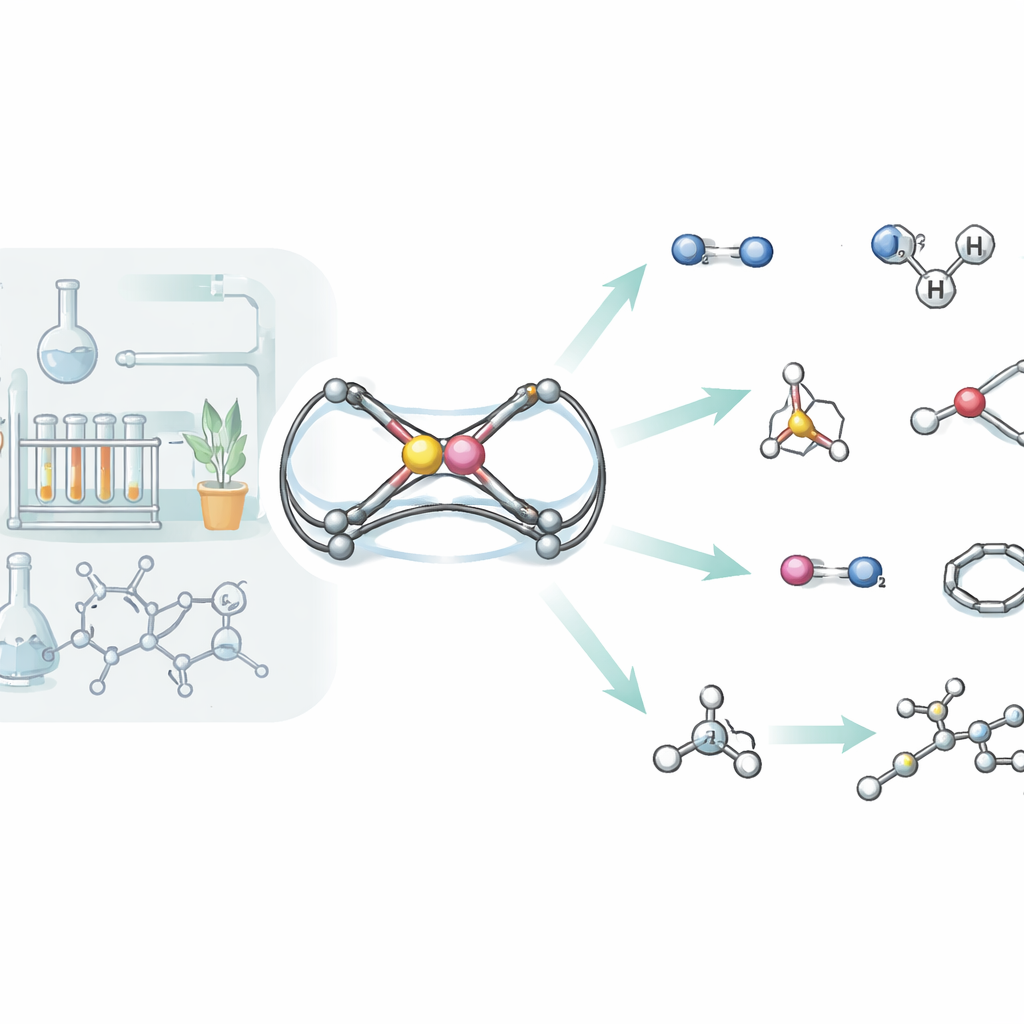
Come la nuova molecola tratta l’idrogeno gassoso
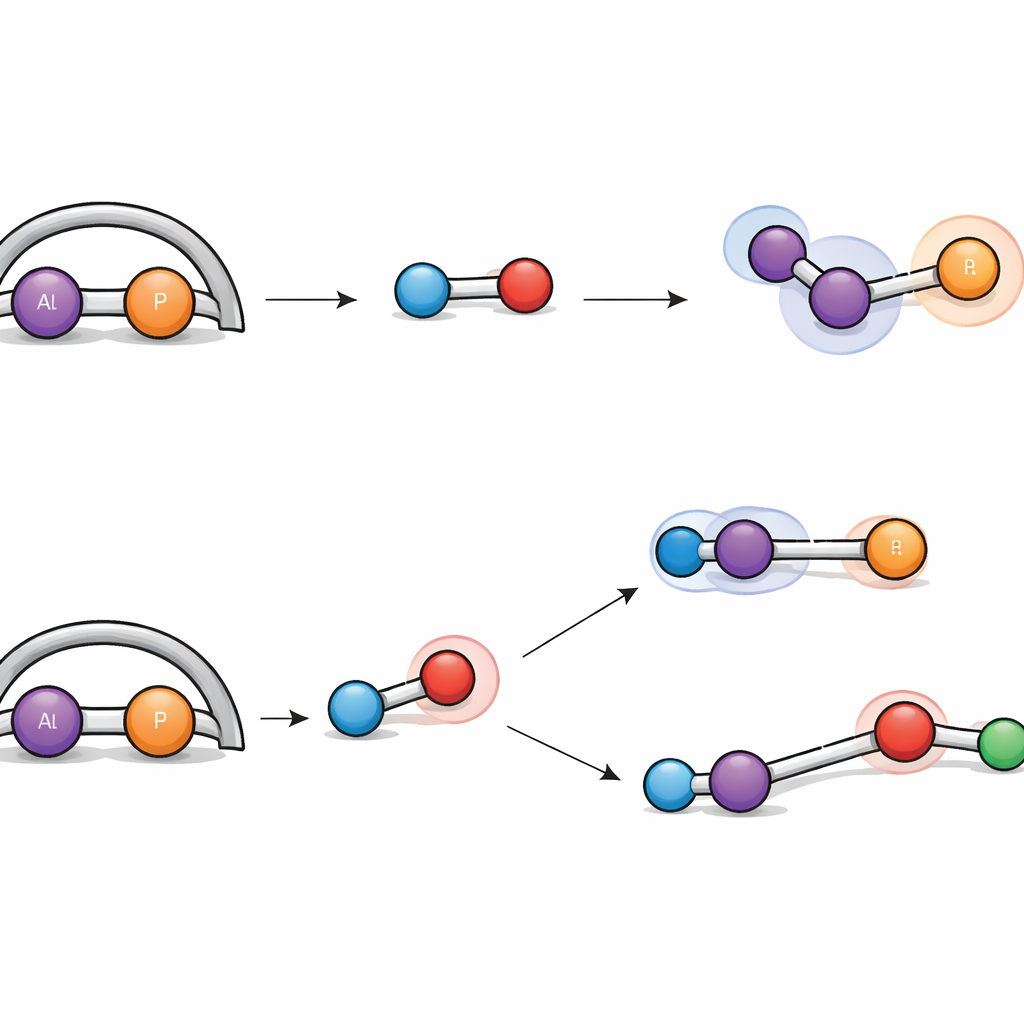
L’idrogeno gassoso è notoriamente difficile da scindere senza ricorrere a metalli preziosi, eppure l’unità alluminio‑fosforo riesce a farlo. Quando esposta a idrogeno in condizioni blande, il complesso reagisce in due modi distinti. In una via, il legame H–H si addiziona semplicemente attraverso il doppio legame alluminio–fosforo, trasformandolo in due legami semplici e legando un atomo di idrogeno a ciascun atomo. Nell’altra, la molecola di idrogeno viene scissa in modo cooperativo dall’alluminio e da un atomo di azoto vicino, un comportamento che ricorda le cosiddette “coppie di Lewis frustrate”, che attivano l’idrogeno senza i tradizionali catalizzatori metallici. Simulazioni dettagliate al calcolatore hanno tracciato entrambe le vie, mostrando che le barriere energetiche sono simili, il che spiega perché si formano entrambi i prodotti in parallelo.
Smontare una galleria di piccole molecole
L’idrogeno è solo l’inizio. Il gruppo ha testato sistematicamente come il loro impalcatura alluminio‑fosforo reagisce con un’ampia gamma di piccole molecole, inclusi fosforo bianco, isocianuri, anidride carbonica, protossido di azoto, azide trimetilsililica, dimeri di selenio, silani, ammine, stirene e alchini semplici. In molte di queste reazioni il legame Al=P originale viene completamente distrutto, con i due atomi che finiscono in strutture più grandi a forma di gabbia o anello che incorporano frammenti della molecola entrante. Per esempio, il fosforo bianco (P4) viene rotto e riorganizzato in una gabbia alluminio‑fosforo, mentre l’anidride carbonica si inserisce due volte formando un anello a sei membri che lega alluminio e fosforo tramite due nuovi ponti carbonio‑ossigeno. Con silani e ammine, la molecola si comporta invece più come un doppio legame classico: l’unità Si–H o N–H entrante si addiziona ordinatamente attraverso Al=P, dimostrando ancora il carattere “π” di questo insolito legame.
Perché l’impalcatura circostante conta
Una delle lezioni chiave del lavoro è che l’ingombrante impalcatura ricca di azoto attorno all’unità Al=P non è solo sostegno; indirizza come e dove avvengono le reazioni. Confrontando i propri risultati con sistemi alluminio‑fosforo precedenti e più effimeri, gli autori mostrano che piccole modifiche nei leganti di supporto ribaltano l’equilibrio tra diverse vie, come la semplice addizione attraverso il doppio legame rispetto a scissioni di legame più complesse e formazione di anelli. Analisi sofisticate della distribuzione elettronica hanno rivelato una forte polarizzazione del legame Al=P e messo in luce come gli atomi di azoto adiacenti possano cooperare con l’alluminio, soprattutto nell’attivazione dell’idrogeno. L’ingombro sterico — l’affollamento fisico di grandi gruppi — indirizza inoltre le molecole entranti verso un sito reattivo piuttosto che un altro.
Quali implicazioni per la chimica futura
Per un non specialista l’elenco di reagenti in questo studio può sembrare distante, ma il messaggio di fondo è chiaro: sintonizzando con cura sia il legame sia la forma intorno agli elementi del main group, i chimici possono costruire strumenti agili che rivaleggiano o completano i catalizzatori metallici tradizionali. Questo complesso isolabile alluminio‑fosforo non solo sopravvive in una fiala ma affronta anche una vasta gamma di piccole molecole ostinate in condizioni miti, spaccando l’idrogeno, riorganizzando il fosforo bianco e catturando l’anidride carbonica. Il lavoro mostra che cambiamenti sottili nella “maniglia” di una molecola possono indirizzare profondamente la sua reattività, offrendo un progetto per concepire futuri catalizzatori che aiutino a convertire molecole semplici e stabili in prodotti più preziosi con precisione ed efficienza.
Citazione: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Parole chiave: attivazione di piccole molecole, chimica dei main group, legame doppio alluminio-fosforo, coppia di Lewis frustrata, meccanismi di attivazione del legame