Clear Sky Science · it
Meccanismo di inibizione delle β−1,3-glucano-sintasi fungine da parte di farmaci antifungini triterpenoidi
Perché fermare le infezioni fungine è importante
Le infezioni fungine uccidono silenziosamente più di un milione di persone ogni anno e costituiscono una minaccia per colture ed ecosistemi in tutto il mondo. I medici dispongono già di una lista ristretta di farmaci antifungini, e alcuni funghi pericolosi stanno evolvendo per sfuggire a questi trattamenti. Questo studio rivela, a livello molecolare, come una nuova classe di farmaci antifungini si leghi e disattivi un enzima chiave che i funghi usano per costruire la loro parete protettiva. Capire questo processo offre una mappa per progettare terapie migliori in grado di superare i funghi resistenti.
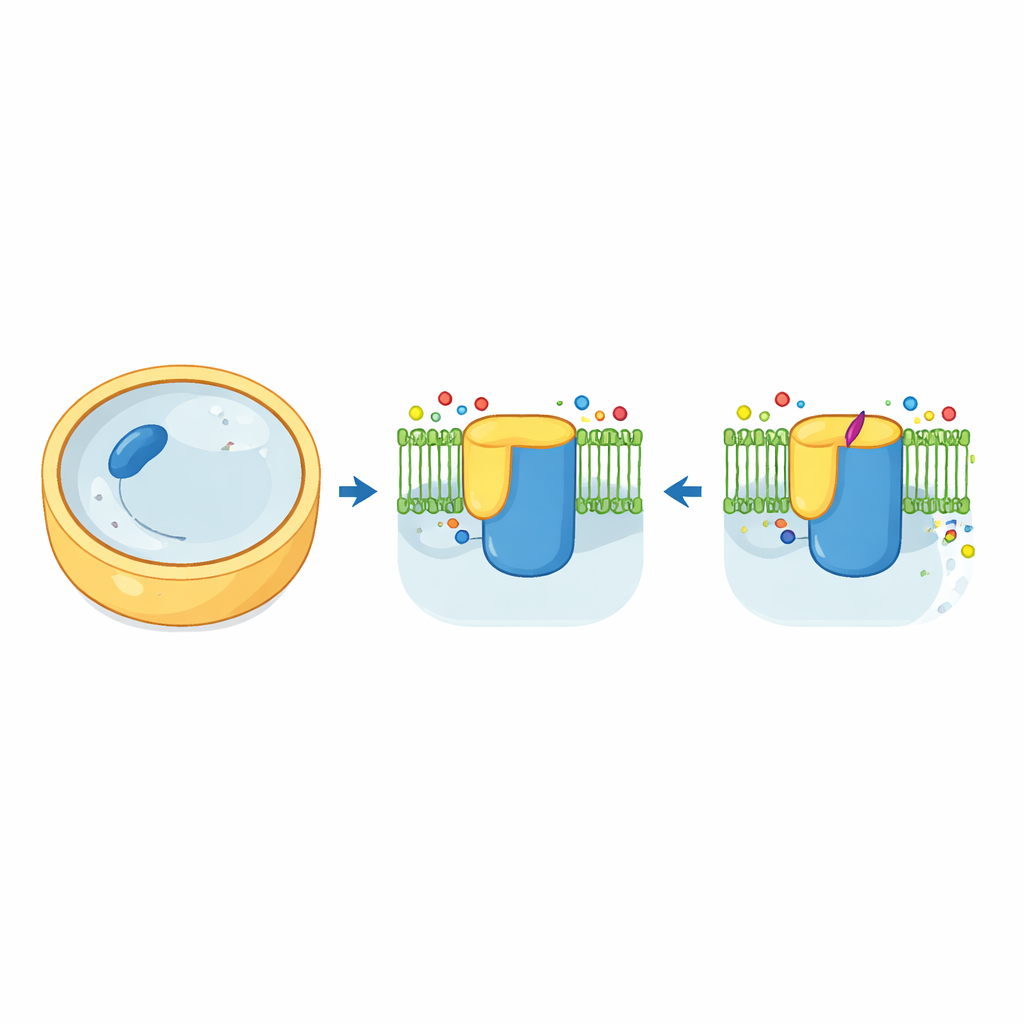
Il “fabbricabrick” della parete cellulare fungina
Le cellule fungine sono avvolte da una parete robusta composta in gran parte da un polimero a base di zucchero chiamato β-1,3-glucano. L’enzima che sintetizza ed esporta questo polimero, noto come β-1,3-glucano-sintasi, funziona come un combinato di fabbricabrick e nastro trasportatore. Nel lievito di birra, questa macchina è costruita da due versioni molto simili, Fks1 e Fks2, entrambe inserite nella membrana cellulare e controllate da una piccola proteina ausiliaria chiamata Rho1. Grazie alla crio-microscopia elettronica, gli autori hanno catturato viste tridimensionali ad alta risoluzione sia di Fks1 sia di Fks2 nella loro forma naturale. Le strutture rivelano un ampio “banco di lavoro” citosolico collegato a una foresta di eliche transmembrana, con una cavità centrale che probabilmente funge da tunnel attraverso il quale la catena di glucano in crescita esce dalla cellula.
Come un farmaco di origine naturale afferra l’enzima
I farmaci triterpenoidi di rilevanza clinica, incluso il medicinale orale ibrexafungerp, derivano da un composto naturale chiamato enfumafungin. Fino ad ora non si sapeva esattamente dove su la glucano-sintasi questi farmaci si legassero. I ricercatori hanno risolto le strutture di entrambe le Fks1 e Fks2 legate all’enfumafungin. Sorprendentemente, il farmaco non si inserisce nel sito attivo dove le unità di zucchero vengono unite. Piuttosto, si annida sulla porzione esterna di una singola elica transmembrana chiamata TM5, posizionandosi nella membrana a circa tre nanometri dal centro catalitico e vicino al probabile canale di uscita del glucano. Aminoacidi chiave in questa regione accolgono il nucleo idrofobico del farmaco e contattano la sua coda acida, mentre il suo appendice zuccherina tocca a malapena la proteina — il che spiega perché i chimici sono riusciti a modificare quella parte senza perdere potenza.
Farmaci che bloccano una macchina in movimento
A prima vista, la forma complessiva dell’enzima con e senza enfumafungin sembra quasi invariata. La differenza cruciale riguarda l’organizzazione dei lipidi circostanti e la flessibilità di certe eliche. Quando il farmaco si lega, una catena laterale aromatica vicina ruota per stringere l’enfumafungin in posizione e, insieme a un altro residuo, stabilizza un lipide ordinato accanto al farmaco. Altri lipidi simili a steroli si dispongono ordinatamente attorno a un set di eliche orizzontali che contribuiscono a definire il percorso di esportazione del glucano. Questi lipidi agiscono come cunei e puntelli, bloccando le eliche e l’ingresso del canale in un particolare assetto “basale”. Test genetici mostrano che alterare molti dei punti di contatto per il farmaco o per questi steroli indebolisce il legame col farmaco o distrugge la funzione enzimatica, e le mutazioni in questi siti corrispondono a mutazioni di resistenza note in patogeni umani e vegetali.
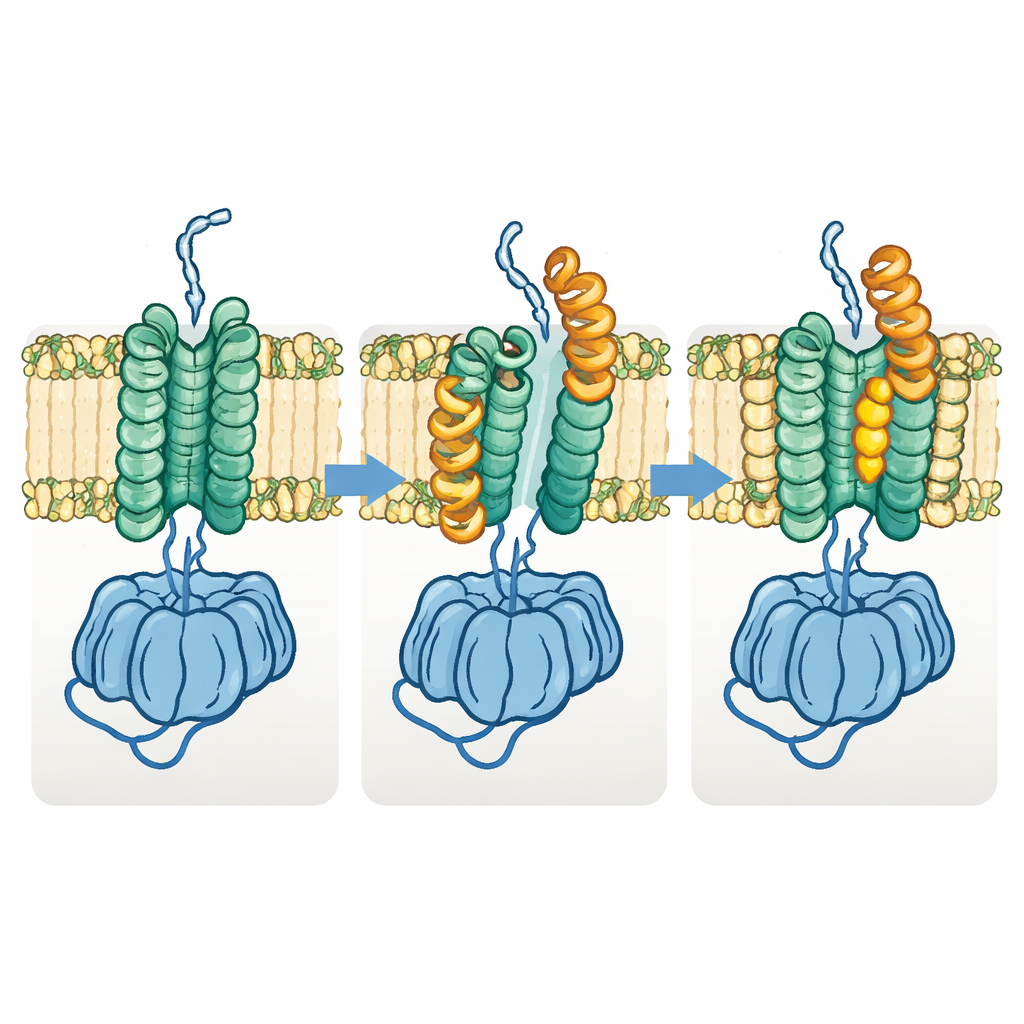
Una trasformazione necessaria per il trasporto del polimero
Il gruppo ha anche scoperto una forma distinta “aperta” di Fks1. In questo stato, metà della regione transmembrana si sposta lateralmente e le eliche orizzontali chiave si aprono verso l’esterno, scardinando lo spazio tra i due fasci di eliche e allargando l’apparente tunnel del glucano. Il confronto di molte strutture suggerisce che l’enzima cicli tra gli stati basale e aperto durante il normale funzionamento: lo stato basale prepara e avvia la formazione del polimero, mentre lo stato aperto permette alla catena in crescita di muoversi lateralmente attraverso la membrana verso l’esterno. Quando gli autori hanno progettato legami disolfuro per bloccare permanentemente l’enzima in uno dei due stati, entrambe le varianti hanno perso in gran parte l’attività, a sostegno dell’idea che questo cambiamento conformazionale sia essenziale per la funzione.
Cosa significa per i futuri farmaci antifungini
Dimostrando che l’enfumafungin e i farmaci correlati non agiscono bloccando la tasca catalitica ma rimodellando l’ambiente lipidico locale e immobilizzando la glucano-sintasi nello stato basale, questo studio rivela una modalità di azione del farmaco non convenzionale. Mostra inoltre che Fks1 e Fks2 condividono strutture e risposte al farmaco quasi identiche, spiegando perché entrambi devono essere considerati nell’affrontare la resistenza. Più in generale, il lavoro evidenzia come piccole molecole possano controllare proteine di membrana considerate “non drogabili” legandosi a superfici poco profonde e reclutando lipidi, offrendo un modello concettuale per la progettazione della prossima generazione di antifungini che restino efficaci anche mentre i funghi evolvono.
Citazione: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Parole chiave: farmaci antifungini, parete cellulare fungina, glucano-sintasi, resistenza ai farmaci, crio-microscopia elettronica