Clear Sky Science · it
Strutture cryo-EM degli intermedi di assemblaggio del portale-collo del batteriofago T4 rivelano un meccanismo di ritenzione del genoma virale
Come un virus mantiene il suo DNA sotto pressione
Il batteriofago T4 è un virus che infetta i batteri E. coli e confeziona il suo DNA così strettamente nella testa che la pressione all’interno può essere da cinque a sette volte superiore rispetto a quella di una bottiglia di champagne. Eppure il DNA non fuoriesce mentre il virus completa la costruzione del resto del suo corpo. Questo studio rivela, a livello molecolare, come il T4 risolva il problema utilizzando un minuscolo doppio cancello che funziona come una camera d’aria per il materiale genetico.
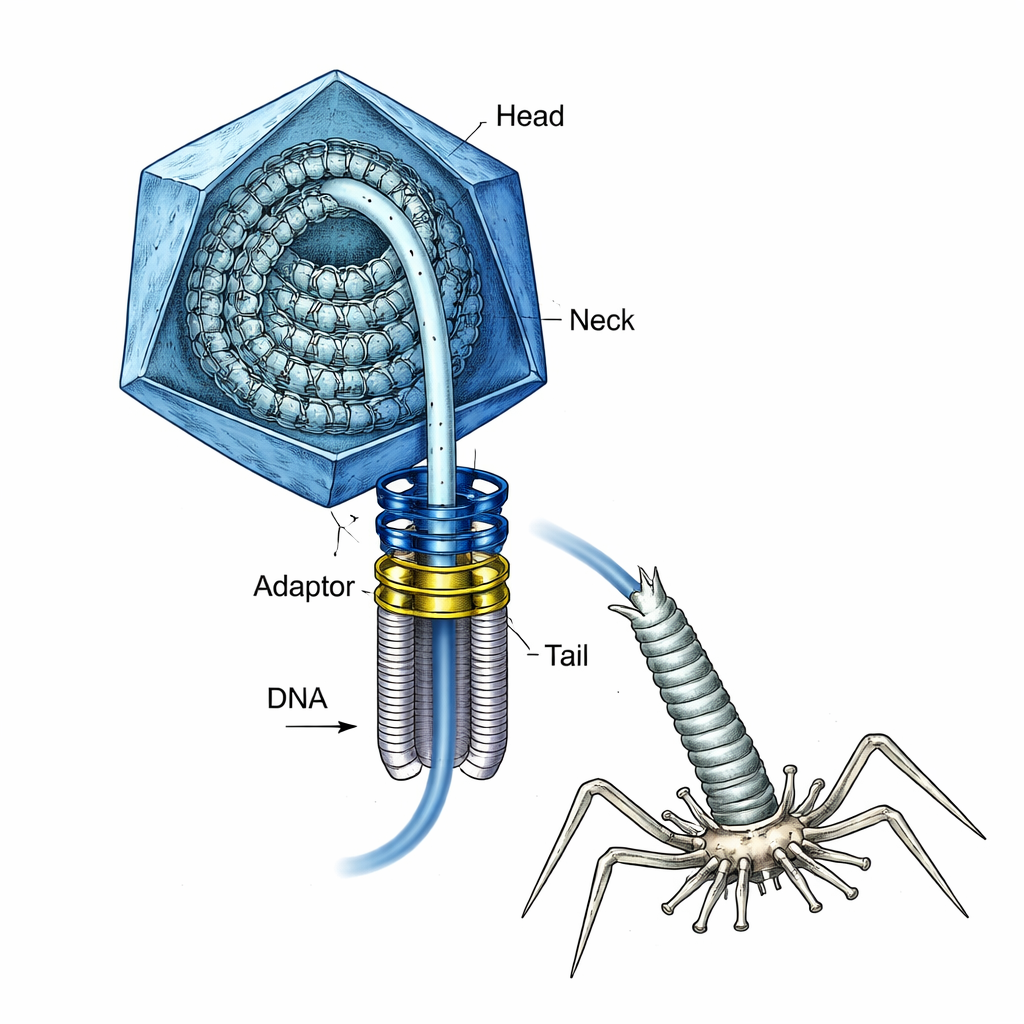
Il virus con una molla carica al suo interno
Il T4 è da tempo un cavallo di battaglia della biologia molecolare ed è anche un modello per costruire future vaccini e vettori per la consegna genica. Durante l’assemblaggio, il virus costruisce prima una conchiglia proteica vuota, o testa, e un “portale” a forma di anello in uno dei vertici. Un potente motore molecolare avvolge quindi il DNA nella testa attraverso questo portale fino a che la testa non è «piena». A quel punto il motore deve staccarsi, devono essere attaccati un collo e una coda e, più tardi, il DNA deve essere iniettato in un batterio—tutto senza permettere che il DNA pressurizzato fuoriesca prematuramente. Non era chiaro in che modo il virus mantenesse questo DNA altamente stressato al sicuro durante queste transizioni.
Ricostruire il collo in laboratorio
I ricercatori hanno ricreato pezzi chiave del T4 in batteri e li hanno mescolati in modo controllato per osservare come si assembla il collo—il connettore tra testa e coda. Due proteine virali, chiamate gp13 e gp14, sono state prodotte separatamente. Da sole flottavano come unità singole, ma insieme si incastravano in anelli impilati che formano un tunnel centrale per il passaggio del DNA. Con sorpresa degli scienziati, una terza proteina continuava a comparire in queste preparazioni: Hfq, una ben nota proteina batterica che di solito aiuta a controllare RNA e attività genica in E. coli. La spettrometria di massa ha confermato che Hfq si legava in modo specifico a gp14, suggerendo che il virus prende in prestito questa proteina dell’ospite come parte del suo collo.
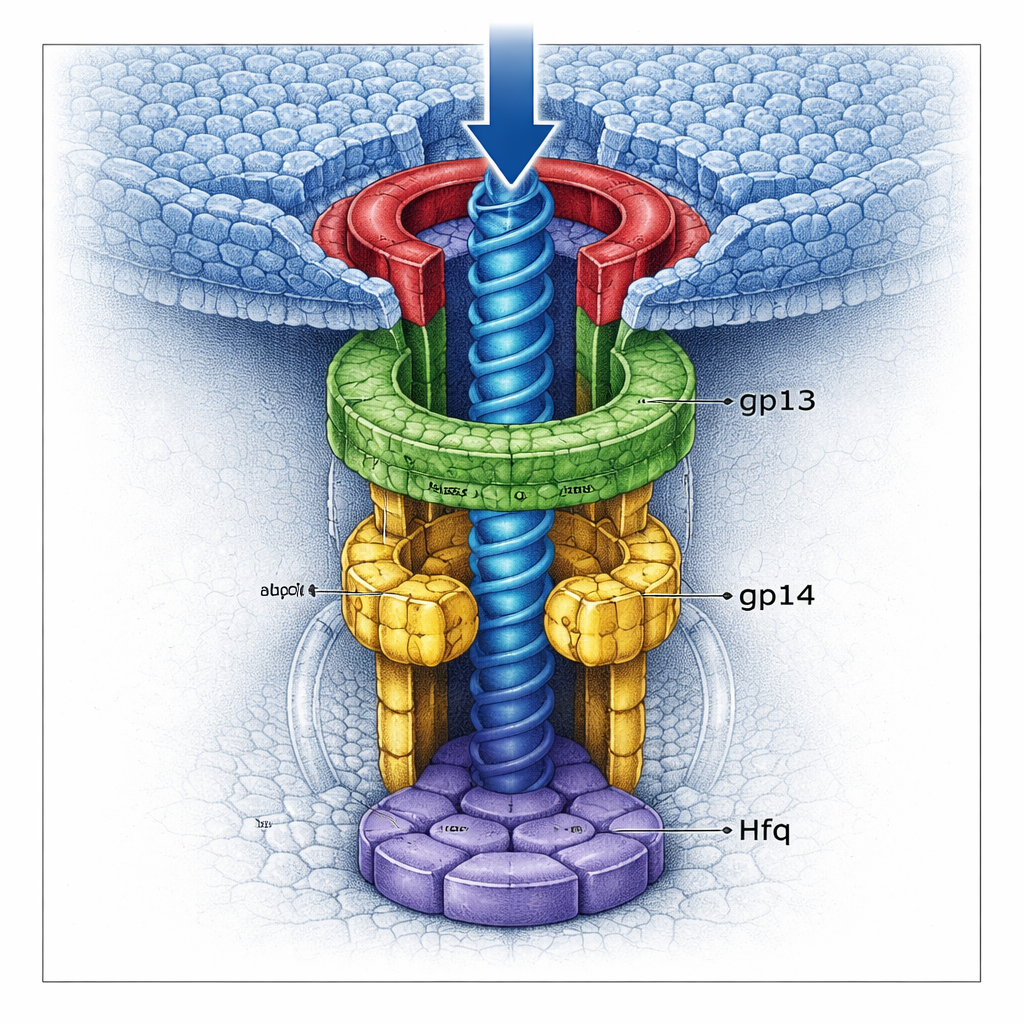
Un doppio cancello che blocca il genoma
Usando la crio-microscopia elettronica ad alta risoluzione, il team ha visualizzato diverse versioni del complesso del collo a dettaglio quasi atomico. Hanno scoperto che gp13 forma un anello ampio che si adatta al portale, mentre gp14 si trova sotto di esso come esamero, creando un canale più stretto. Crucialmente, ogni subunità di gp14 contribuisce con un lungo loop che si protende verso il centro del tunnel. Insieme, sei di questi «anelli arresto» formano un cancello stretto che può catturare l’ultimo segmento di DNA quando tenta di uscire dalla testa. Sotto gp14, la proteina Hfq, dirottata dall’ospite, si assemblа a sua volta in un esamero, tappando il fondo del canale come una seconda porta. Quando Hfq è presente, la struttura gp13–gp14 è più completa e rigida, e i cancelli combinati restringono ulteriormente il tunnel, rendendo molto meno probabile la fuoriuscita di DNA.
Tempi, prevenzione degli errori e un aiutante preso in prestito
Lo studio mostra anche che questo sistema non è solo un tappo statico; è una sequenza di cambiamenti conformazionali attentamente coreografata. Una volta che la testa è piena, la pressione interna spinge il portale in una nuova conformazione che espone siti di legame per gp13. Un collo pre-assemblato gp13–gp14–Hfq si ancora quindi al portale. Gp13 flette, si solleva e si blocca sia sul portale sia sulla conchiglia esterna, intrecciando saldamente il collo nella testa. Durante questa fase, i loop arresto di gp14 e il tappo Hfq tengono il DNA al suo posto. Hfq svolge un secondo ruolo come fattore di controllo qualità: occupando superfici chiave su gp14, impedisce a gp14 di legarsi al portale nella posizione sbagliata, il che provocherebbe un assemblaggio difettoso del collo. Solo quando arriva la coda preassemblata una proteina della punta della coda, gp15, forma un legame ancora più forte con gp14, spostando Hfq e aprendo la via al rilascio controllato del DNA nella coda.
Perché questo importa oltre un singolo virus
In termini semplici, il T4 usa una serratura a due porte per trattenere una potente «molla» di DNA mentre completa la costruzione del resto del virus. La prima porta è costruita dalla sua proteina del collo, gp14, e la seconda porta è presa in prestito dalla proteina Hfq dell’ospite, che il virus utilizza temporaneamente e poi scarta. Questo doppio cancello garantisce che quasi nessun DNA venga perso e che il virus finale sia pienamente infettivo. Poiché molti grandi virus impacchettano i loro genomi sotto pressioni estremamente elevate e condividono un’architettura correlata, questo lavoro suggerisce che sistemi di bloccaggio comparabili, e persino il dirottamento temporaneo di proteine ospiti, possano essere diffusi. Comprendere questi meccanismi potrebbe guidare la progettazione di vettori virali più sicuri per la medicina e indicare nuovi modi per bloccare virus dannosi puntando alle loro «serrature» del genoma.
Citazione: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Parole chiave: batteriofago T4, assemblaggio virale, crio-microscopia elettronica, impacchettamento del genoma, interazione ospite–virus