Clear Sky Science · it
scLong: un modello di base con miliardo di parametri per catturare il contesto genico a lungo raggio nella trascrittomica single-cell
Insegnare ai computer a leggere il linguaggio nascosto delle cellule
Ogni cellula del tuo corpo ospita una città brulicante di geni che si accendono e spengono seguendo schemi complessi. Le moderne tecniche di sequenziamento dell'RNA a singola cellula possono ora ascoltare ogni singola cellula, ma il risultato è un flusso travolgente di numeri. Questo articolo presenta scLong, un enorme modello di intelligenza artificiale progettato per dare senso a questi complessi modelli di attività genica, inclusi i segnali deboli che i metodi più vecchi tendono a ignorare. Il suo obiettivo è aiutare i ricercatori a comprendere come le cellule reagiscono quando certi geni vengono spenti, quando vengono aggiunti farmaci o quando insorgono malattie.
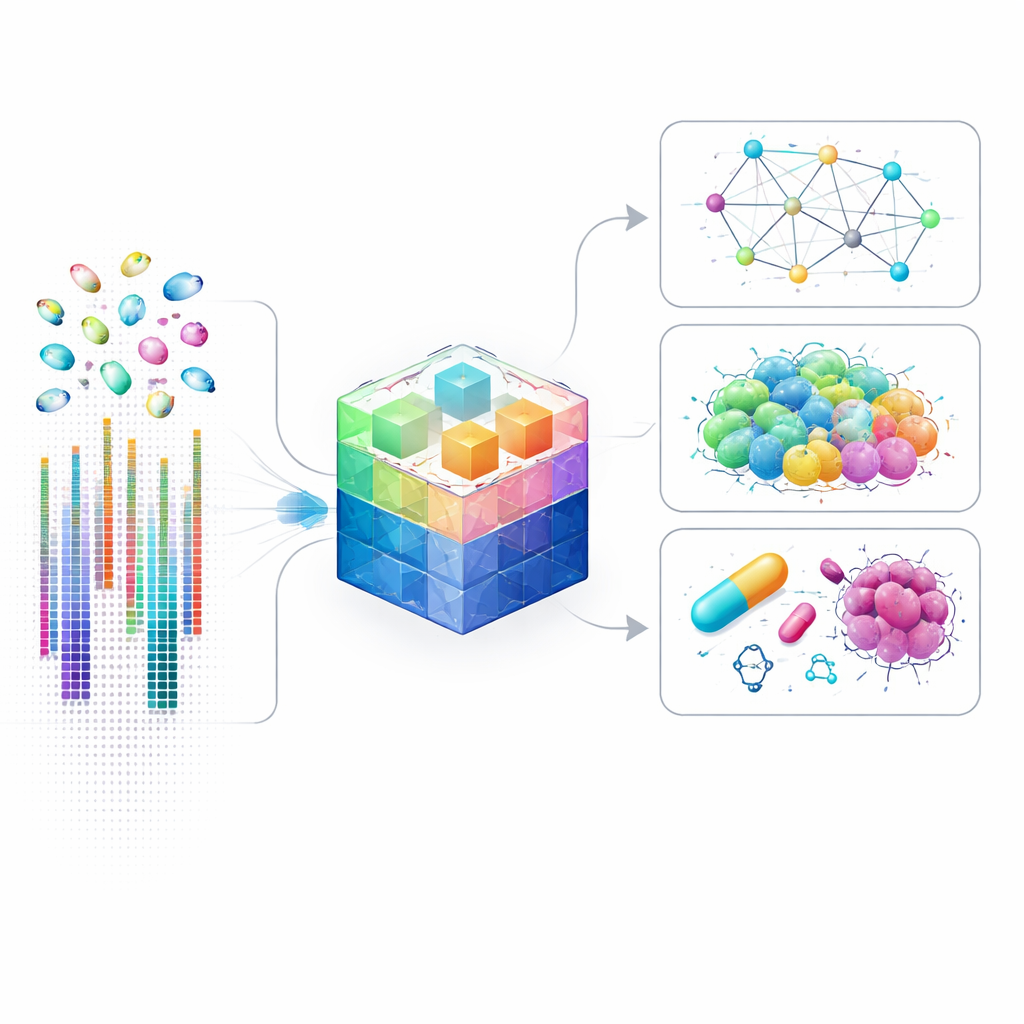
Perché le mappe geniche a livello cellulare sono importanti
Gli studi genetici tradizionali spesso mescolano milioni di cellule, mediando via le cellule rare o anomale. Le tecniche single-cell hanno cambiato questo approccio misurando l'attività genica di ciascuna cellula separatamente, rivelando tipi cellulari nascosti, sottili comunicazioni cellula-cellula e circuiti di controllo dettagliati che decidono il destino di una cellula. Tuttavia, analizzare questo tipo di dati è estremamente difficile: ogni cellula può avere livelli di attività misurati per decine di migliaia di geni, molti dei quali sono appena rilevabili. I modelli di IA esistenti semplificano il problema concentrandosi solo sui geni più rumorosi, il che accelera i calcoli ma perde molti segnali sottili che potrebbero essere cruciali nelle malattie, nello sviluppo o nella risposta ai farmaci.
Un nuovo modello che ascolta ogni gene
scLong affronta questa sfida ampliando la scala invece di ridurla. È un modello di base con miliardo di parametri addestrato su profili di attività genica di circa 48 milioni di cellule umane provenienti da oltre 50 tessuti. Diversamente dagli approcci precedenti che considerano poche migliaia di geni altamente attivi, scLong prende in esame circa 28.000 geni alla volta, inclusi quelli raramente o debolmente espressi. Combina due tipi di informazioni per ciascun gene: quanto è attivo in una determinata cellula e cosa è già noto sulla sua funzione dal Gene Ontology, un ampio catalogo curato da esperti sui ruoli e le relazioni geniche. Una rete specializzata che opera su un grafo di connessioni geniche distilla questa conoscenza a priori in rappresentazioni compatte che il modello può usare insieme ai valori grezzi di espressione.
Come il modello bilancia potenza ed efficienza
Considerare ogni gene in dettaglio è computazionalmente costoso, quindi scLong usa un ingegnoso design a due piste. All'interno di ciascuna cellula, i geni sono ordinati in base all'intensità di espressione. I geni più attivi, che spesso portano il segnale biologico principale, vengono elaborati attraverso un modulo di attenzione più grande e potente. I geni più silenziosi, incluse misurazioni basse o addirittura nulle, sono instradati attraverso un modulo più piccolo e leggero. Successivamente, tutti i geni vengono ricombinati e passati attraverso un altro strato di attenzione che permette a ogni gene di influenzare tutti gli altri. Questo design consente al modello di mantenere rappresentazioni meno costose ma comunque significative per i segnali deboli, riservando maggiore capacità per quelli più forti. Durante il pretraining, il sistema nasconde ripetutamente un sottoinsieme dei valori di attività genica e impara a ricostruirli dal contesto circostante, costringendolo a scoprire i pattern che collegano i geni tra loro.
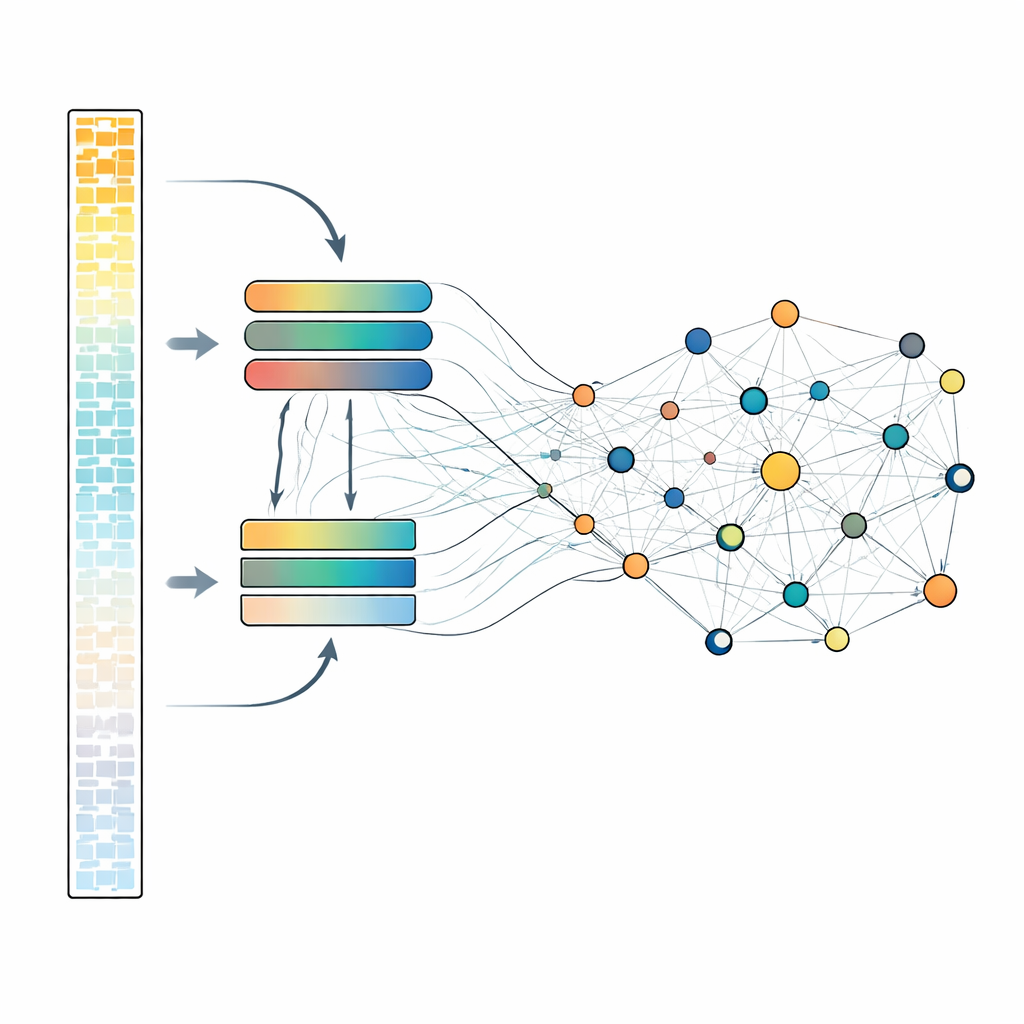
Mettere il modello al lavoro su problemi reali
Una volta addestrato, scLong può essere adattato a una vasta gamma di domande biologiche. Gli autori mostrano che predice come l'attività genica cambierà quando geni specifici vengono spenti o alterati, comprese combinazioni di due geni che possono agire insieme. Predice anche come le cellule rispondono quando esposte a diversi composti chimici, cosa importante per la scoperta di farmaci e i test di sicurezza. Negli studi sul cancro, scLong aiuta a prevedere come linee cellulari tumorali risponderanno a singoli farmaci e a coppie di farmaci che potrebbero funzionare meglio in combinazione, spesso superando sia modelli specializzati sia altri grandi modelli di base. Oltre alla predizione, scLong può inferire reti di relazioni regolatorie tra geni e può aiutare a correggere distorsioni tecniche che emergono quando i dati sono raccolti in laboratori o su macchine diverse.
Cosa significa questo per la medicina e la ricerca future
In termini semplici, scLong offre agli scienziati una mappa ad alta risoluzione e consapevole del contesto dell'attività genica all'interno delle singole cellule, una mappa che non scarta i geni silenziosi o raramente usati. Imparando da milioni di cellule e incorporando conoscenze biologiche esistenti, fornisce previsioni più accurate su come le cellule reagiranno quando i geni vengono perturbati, quando vengono introdotti nuovi farmaci o quando si sviluppano processi patologici. Questo potrebbe accelerare la ricerca di nuove terapie, guidare scelte di trattamento più personalizzate e affinare la nostra comprensione di come reti geniche complesse controllino salute e malattia. Pur essendo un modello grande e computazionalmente esigente, indica una direzione futura in cui potenti sistemi di IA generali fungono da compagni versatili per esplorare il funzionamento nascosto delle nostre cellule.
Citazione: Bai, D., Mo, S., Zhang, R. et al. scLong: a billion-parameter foundation model for capturing long-range gene context in single-cell transcriptomics. Nat Commun 17, 2380 (2026). https://doi.org/10.1038/s41467-026-69102-y
Parole chiave: trascrittomica single-cell, modelli di base, regolazione genica, predizione della risposta ai farmaci, espressione genica