Clear Sky Science · it
Cellule ILC1 CD127+ del tessuto adiposo indotte da peritonite acuta esprimono PD-L1 e riducono l’infiammazione nei topi
Perché il grasso addominale può aiutare a combattere un’infezione mortale
Quando batteri fuoriescono da un intestino lacerato nella cavità addominale, l’organismo può precipitare in una condizione potenzialmente letale chiamata sepsi. Questo studio rivela un alleato inaspettato in quella battaglia: un gruppo speciale di cellule immunitarie nascoste nel grasso addominale che migrano all’inizio dell’infezione e funzionano come un freno integrato contro l’infiammazione incontrollata. Comprendere come operano queste cellule potrebbe ispirare nuovi trattamenti per calmare infezioni pericolose senza spegnere del tutto il sistema immunitario.
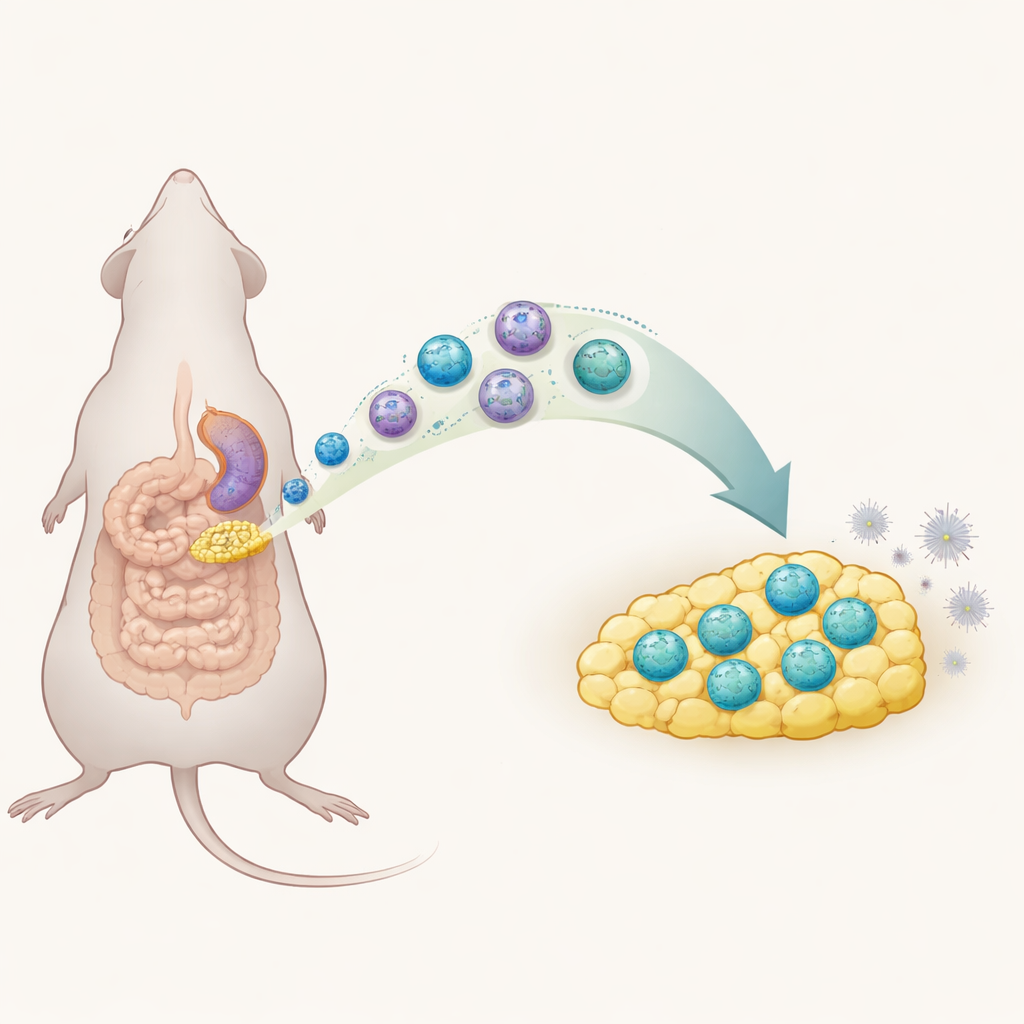
Una perdita pericolosa nell’addome
La peritonite si verifica quando il rivestimento dell’addome si infiamma, più spesso perché batteri fuoriescono da un intestino perforato. Se questa prima ondata di infiammazione non viene controllata, i pazienti possono sviluppare sepsi, che ancora oggi uccide circa una persona su cinque tra gli affetti nonostante le cure moderne. I medici possono trattare l’infezione con interventi chirurgici e antibiotici, ma dispongono di pochi strumenti per orientare la reazione immunitaria del corpo lontano da un pericoloso sovraccarico. Il grasso che ricopre l’intestino, chiamato tessuto adiposo mesenterico, è noto per affluire verso i siti di danno intestinale, suggerendo che svolga un ruolo attivo in questa risposta immunitaria precoce.
Guardiani nascosti nel grasso addominale
Negli ultimi anni i ricercatori hanno scoperto le “cellule linfoidi innate”, sentinelle immunitarie ad azione rapida che vivono in molti tessuti. Un sottotipo, chiamato ILC di gruppo 1, aiuta normalmente ad avviare forti reazioni infiammatorie. In questo studio su topi, i ricercatori hanno usato un modello chirurgico standard di peritonite per indagare il comportamento di queste cellule nel grasso mesenterico. Hanno scoperto che, sei ore dopo la lesione, questo tessuto mostrava segnali infiammatori e una forte ondata di cellule ILC1, mentre altri tipi cellulari correlati cambiavano di poco. Questa tempistica coincideva con il picco della malattia negli animali, suggerendo che le ILC1 fossero strettamente legate alla fase infiammatoria iniziale nell’addome.
Cellule migranti che cambiano natura
Approfondendo, il team ha utilizzato sofisticate analisi a singola cellula per suddividere la popolazione di ILC1 in sottogruppi. In condizioni normali, la maggior parte delle ILC1 nel grasso addominale non esprimeva sulla superficie una molecola chiamata CD127. Durante la peritonite acuta, tuttavia, è apparso ed è aumentato un nuovo gruppo di ILC1 CD127‑positive. Queste arrivate producevano meno dell’efficace segnale infiammatorio interferone‑gamma rispetto alle loro controparti CD127‑negative, contraddistinguendole come relativamente più moderate. Gli scienziati hanno dimostrato che molte di queste cellule non semplicemente si dividono in loco: invece, ILC1 dalla milza migrano tramite il circolo ematico verso il tessuto adiposo mesenterico, guidate in parte da un segnale chimico di “ritorno” chiamato CXCL10 e dal suo recettore CXCR3. Una volta nel grasso, mutano i loro marcatori di superficie, acquisendo CD127 e assumendo questa personalità più tranquilla e regolatoria.
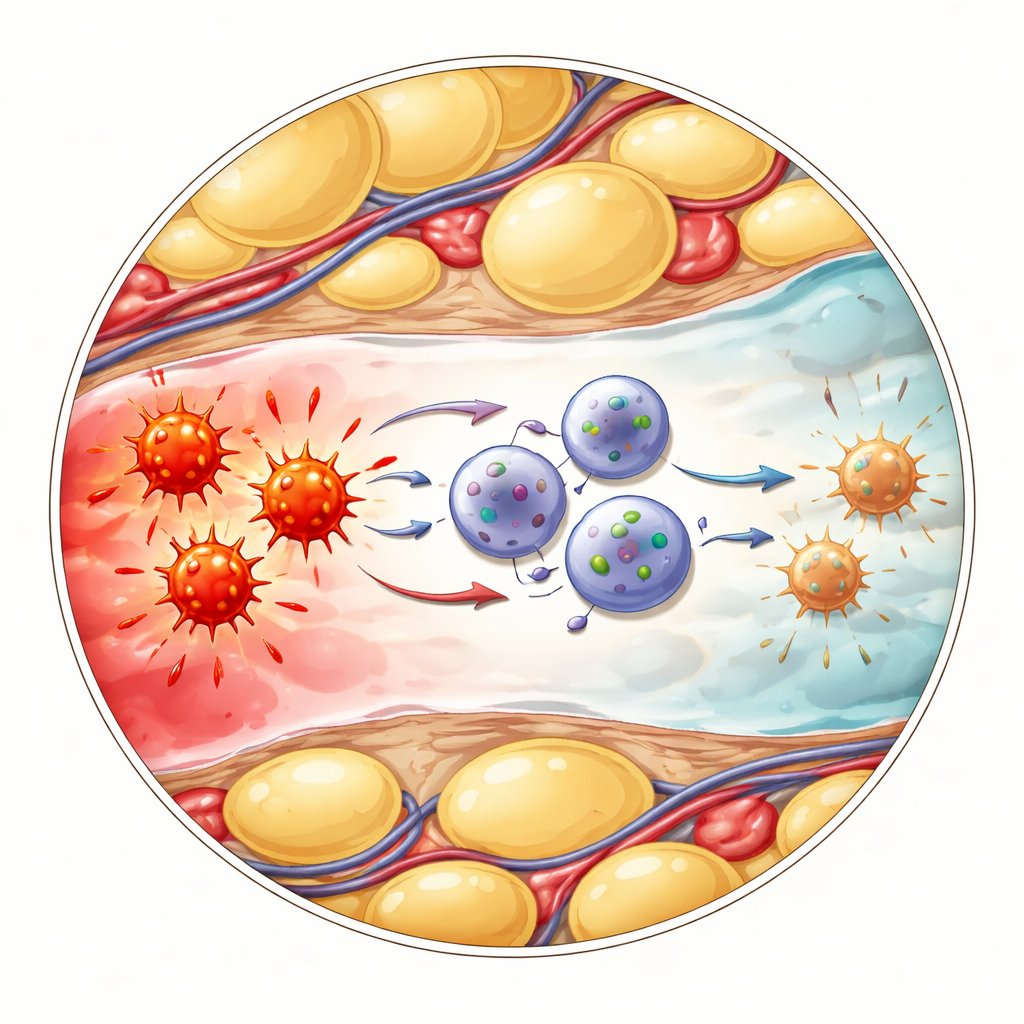
Come le cellule calmanti parlano con quelle infiammatorie
La domanda successiva era come queste ILC1 modificate effettivamente attenuassero l’infiammazione. I ricercatori si sono concentrati su un altro gruppo immunitario chiamato cellule T gamma‑delta, che rispondono rapidamente al pericolo e possono rilasciare grandi quantità della molecola d’allarme TNF. Le analisi a singola cellula hanno suggerito che le ILC1 CD127‑positive e le cellule T gamma‑delta comunicano tramite una nota via di “freno” che coinvolge le proteine di superficie PD‑L1 e PD‑1. Nel grasso addominale infiammato, le ILC1 appena arrivate aumentavano fortemente PD‑L1, mentre le vicine cellule T gamma‑delta esprimevano alti livelli di PD‑1. Quando il team ha bloccato PD‑1 con anticorpi, le cellule T gamma‑delta hanno prodotto più TNF, confermando che questo contatto di norma limita la loro risposta infiammatoria. Allo stesso modo, topi geneticamente privi di ILC1 hanno manifestato una malattia più grave, marcatori infiammatori più elevati e più TNF dalle cellule T gamma‑delta—effetti che potevano essere attenuati bloccando direttamente il TNF.
Cosa significa per futuri trattamenti
Mettere insieme questi risultati, gli autori propongono un asse “milza‑verso‑grasso addominale”: poco dopo che i batteri invadono l’addome, le ILC1 lasciano la milza, migrano al tessuto adiposo mesenterico e lì si trasformano in cellule ricche di CD127 e PD‑L1 che attenuano la produzione di TNF da parte delle cellule T gamma‑delta. Piuttosto che alimentare l’infiammazione, queste ILC1 specializzate agiscono come pacificatori locali, impedendo che la risposta infiammatoria sballi e contribuendo possibilmente a frenare la progressione della peritonite verso la sepsi fatale. A lungo termine, farmaci che potenziano o mimano questo circuito regolatorio nel grasso addominale potrebbero offrire un nuovo modo per trattare le infezioni gravi—modulando la risposta immunitaria in modo che rimanga sufficientemente forte per combattere i germi, senza diventare pericolosa per il paziente.
Citazione: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Parole chiave: peritonite, cellule linfoidi innate, tessuto adiposo mesenterico, regolazione immunitaria, sepsi