Clear Sky Science · it
Una strategia sintetica combinatoria per sviluppare vettori per la consegna di proteine di editing genomico mirati alla retina di topo
Nuova speranza per il trattamento della cecità ereditaria
Molte forme di cecità ereditaria iniziano con un singolo gene difettoso nelle cellule sensibili alla luce nella parte posteriore dell'occhio. Strumenti moderni di editing genico come CRISPR possono, in teoria, correggere questi errori, ma introdurre in sicurezza la macchina di editing nelle cellule giuste è stato un ostacolo importante. Questo studio descrive un nuovo modo per trasportare potenti editor genici direttamente nella retina di topo usando particelle appositamente progettate, aumentando la prospettiva di trattamenti una tantum che possano ripristinare la vista in persone con malattie genetiche dell'occhio.
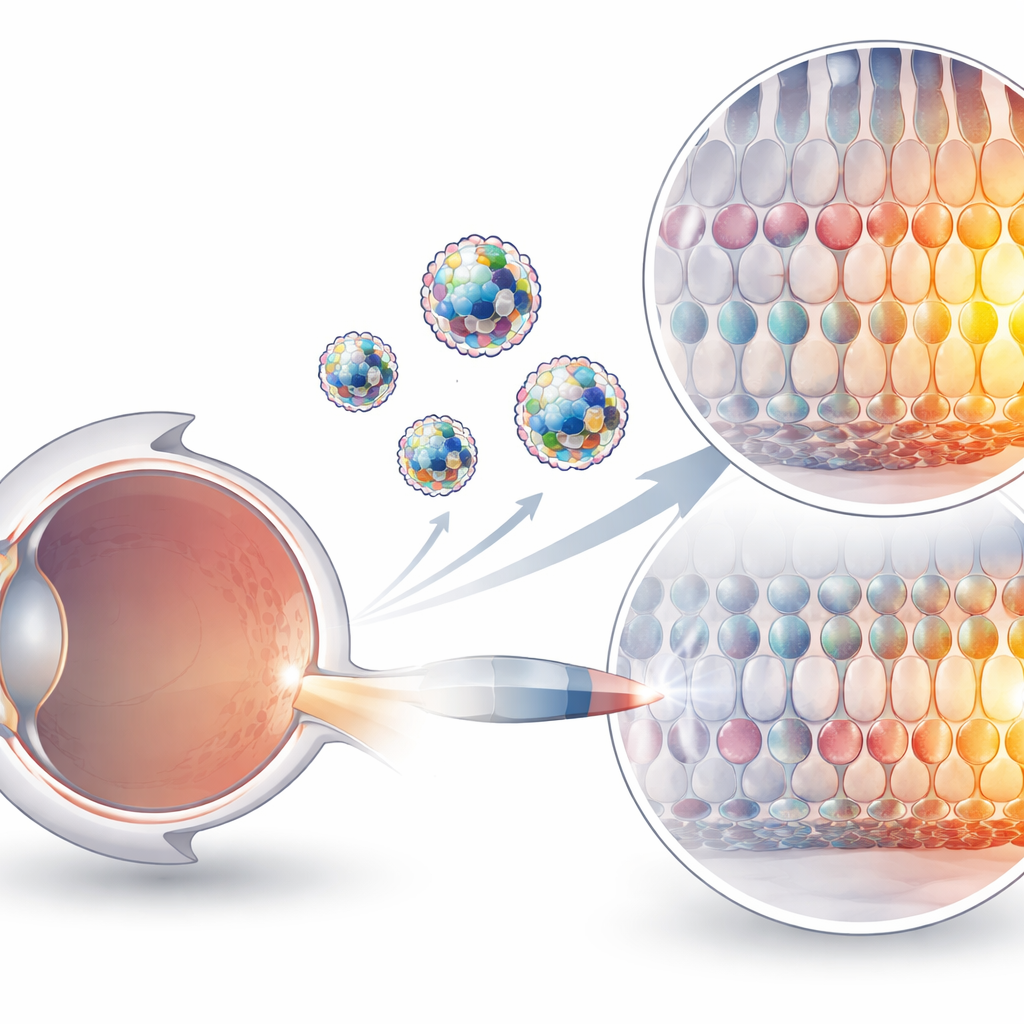
Perché è così difficile fornire gli editor genici
Gli strumenti basati su CRISPR possono ora cambiare singole lettere del DNA senza tagliare entrambi i filamenti, un progresso che li rende appetibili per il trattamento di malattie genetiche. Ma questi strumenti sono complessi complessi proteina–RNA, carichi elettricamente e fragili nell'organismo. I metodi di consegna attuali si basano in gran parte su virus modificati o su particelle che trasportano il progetto genetico per l'editor anziché l'editor stesso. I virus possono provocare reazioni immunitarie e hanno limiti di dimensione rigorosi, mentre la consegna di RNA messaggero funziona molto bene nel fegato ma rimane inefficiente in molti altri tessuti, compreso l'occhio. L'iniezione diretta dei complessi proteina–RNA pre-assemblati è concettualmente più pulita e sicura, tuttavia è mancato un veicolo adatto che li aiuti a attraversare le membrane cellulari e raggiungere i loro bersagli.
Un vettore ispirato a un colorante per le proteine
I ricercatori si sono rivolti a un punto di partenza inaspettato: il Coomassie Brilliant Blue, un colorante blu profondo comunemente usato nei laboratori di biologia e già approvato per alcuni interventi oculari. Questo colorante si lega saldamente a molte proteine diverse. Il team ha legato chimicamente teste di Coomassie a «code» simili a grassi per creare una famiglia di nuove molecole chiamate lipidoidi. In acqua, questi lipidoidi tendono ad aggregarsi in particelle, con le parti oleose sepolte all'interno e i gruppi Coomassie esposti all'esterno, dove possono catturare le proteine. Variando la lunghezza, il ramificarsi e la carica delle code, gli scienziati hanno costruito decine di composti candidati progettati per legare gli editor genici da un lato e interagire con le membrane cellulari dall'altro.
Testare la consegna di proteine alle cellule oculari
Per vedere quali design funzionavano effettivamente, il gruppo ha prima usato una proteina di prova semplice chiamata Cre recombinasi che inverte un interruttore genetico da fluorescenza verde a rossa o da rossa a verde in cellule e topi ingegnerizzati. Vari lipidoidi Coomassie hanno trasportato Cre in modo efficiente nelle cellule coltivate, trasformando ampie frazioni di cellule da verde a rosso. Quando iniettati sotto la retina di topi reporter, i composti selezionati hanno scatenato cambiamenti di colore evidenti sia nello strato pigmentato che supporta la visione sia nei fotorecettori sensibili alla luce, dimostrando che le proteine avevano raggiunto proprio le cellule più colpite in molte malattie che causano cecità. Questi esperimenti iniziali hanno inoltre rivelato che piccoli cambiamenti nella struttura del lipidoide possono modificare i tipi cellulari bersaglio, suggerendo che versioni future potrebbero essere ottimizzate per specifici strati retinici.
Potenziare l'editing genetico e recuperare la vista
Successivamente, il team ha caricato il sistema con un editor di basi adenina, una variante raffinata di CRISPR in grado di correggere la specifica mutazione a singola lettera che causa la perdita della vista nei topi rd12, un modello di una grave cecità infantile. Da sola, la complessa proteina–RNA dell'editor penetrava poco nelle cellule. Un lipidoide, soprannominato CBB11, migliorava la consegna ma tendeva ad agglomerarsi in soluzione. Per stabilizzarlo, i ricercatori hanno incorporato CBB11 in piccoli liposomi ben definiti—sfere cave costituite da diversi tipi di lipidi, inclusi componenti usati clinicamente nei vaccini a mRNA. In queste formulazioni, CBB11 sulla superficie del liposoma legava la parte proteica dell'editor, mentre altri lipidi aiutavano a legare la guida RNA, creando un guscio cooperativo che manteneva l'intero complesso all'esterno della particella.
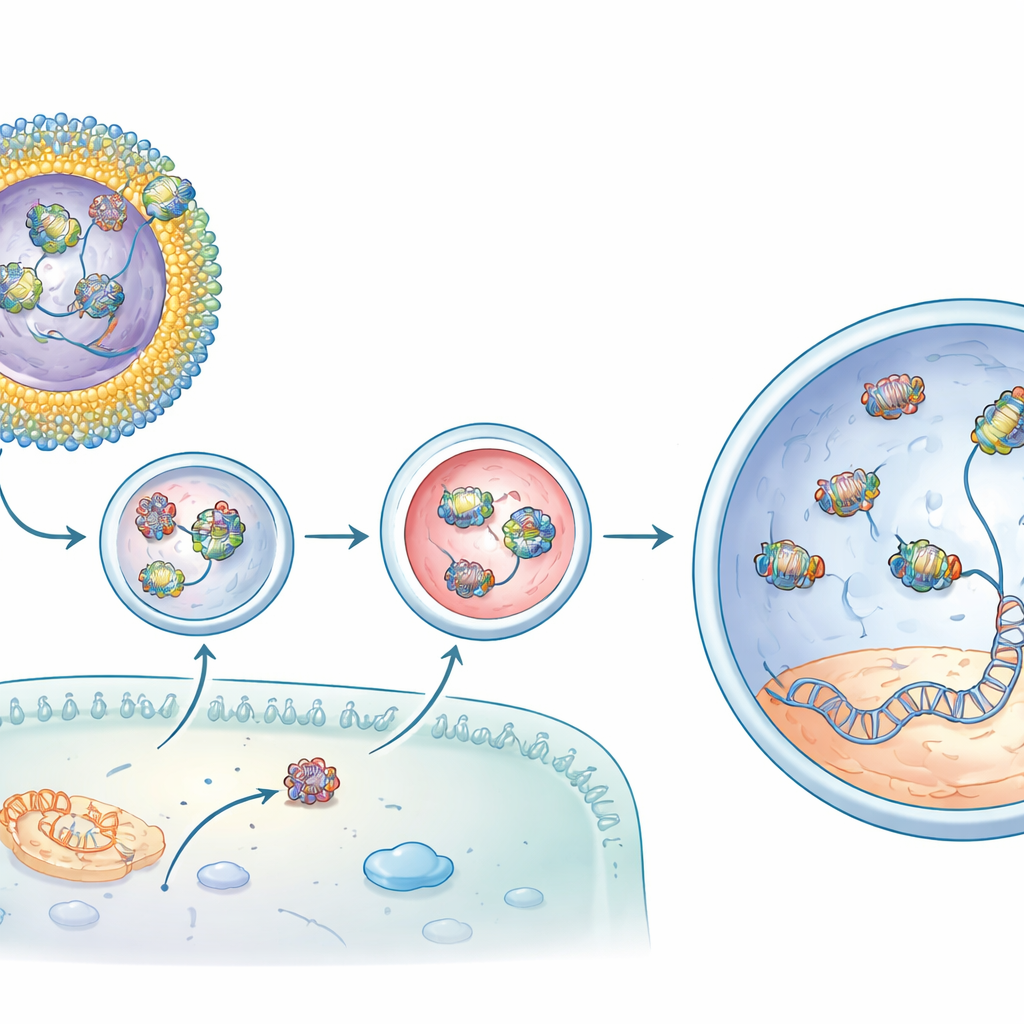
Dalla riparazione molecolare al ripristino delle risposte alla luce
Quando questi liposomi contenenti CBB11 che trasportavano l'editor di basi furono iniettati sotto la retina dei topi rd12, i risultati furono impressionanti. Rispetto all'editor iniettato da solo, la formulazione ottimizzata aumentò la correzione del DNA desiderata nel gene bersaglio di oltre un ordine di grandezza e produsse livelli ancora più elevati di RNA messaggero corretto. L'analisi chimica mostrò il recupero del pigmento retinico sensibile alla luce che manca nella malattia. Ancora più convincente, le registrazioni elettriche dagli occhi degli animali rivelarono che le cellule rod recuperarono gran parte della loro capacità di rispondere alla luce debole—fino a circa tre quarti del segnale di un topo normale nei casi migliori. Le alterazioni fuori bersaglio in altre parti del genoma risultarono a livelli di fondo, suggerendo che l'editing era sia potente sia preciso.
Cosa potrebbe significare per le terapie oculari future
Per un non specialista, il messaggio chiave è che gli autori hanno costruito un «autobus navetta» riutilizzabile per proteine di editing genico che funziona direttamente nell'occhio vivo. Decorando particelle lipidiche sicure, simili a vaccini, con un colorante che afferra le proteine, hanno creato un sistema in grado di catturare diversi editor sulla sua superficie, consegnarli nelle cellule retiniche, correggere mutazioni causanti malattia e ripristinare misurabilmente la vista nei topi dopo un singolo trattamento. Sebbene siano necessari ulteriori studi per valutare pienamente la sicurezza, migliorare il targeting e adattare il metodo all'uso umano, questa piattaforma indica la strada verso future medicine di precisione una tantum per le malattie retiniche ereditarie e, possibilmente, altre condizioni genetiche in cui una riparazione localizzata e accurata del DNA potrebbe fare la differenza tra cecità e vista.
Citazione: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Parole chiave: terapia genica retinica, editing base CRISPR, liposomi, consegna di proteine, cecità ereditaria