Clear Sky Science · it
Approfondimenti sulla struttura e la modulazione del TWIK-2 umano
Perché questo minuscolo cancello nelle nostre cellule conta
Nelle profondità delle nostre cellule, piccolissimi cancelli proteici controllano il flusso di atomi carichi, determinando come i nervi si attivano, come si contraggono i vasi sanguigni e come reagisce il sistema immunitario. Uno di questi cancelli, chiamato TWIK-2, è stato collegato a ipertensione polmonare e a infiammazione dannosa, ma finora gli scienziati sapevano poco sulla sua architettura o su come modulare la sua attività con farmaci. Questo studio rivela la struttura dettagliata del TWIK-2 umano, mostra il suo comportamento elettrico e delinea come potrebbe essere preso di mira per sviluppare nuovi farmaci anti‑infiammatori.
Un canale silenzioso con grandi implicazioni per la salute
TWIK-2 appartiene a una vasta famiglia di canali del potassio “di perdita” che aiutano a stabilire il potenziale di riposo delle cellule permettendo agli ioni potassio di diffondere attraverso la membrana. Mentre altri membri di questa famiglia, come i canali TREK e TASK, sono stati intensamente studiati e collegati a dolore e umore, TWIK-2 è rimasto oscuro perché è difficile da registrare ed è scarsamente espresso nei sistemi di laboratorio standard. Tuttavia studi su animali e cellule hanno collegato TWIK-2 a ipertensione polmonare, lesione polmonare acuta, perdita dell’udito e all’attivazione di un complesso immunitario chiamato inflamasoma NLRP3, che guida un’infiammazione dannosa in sepsi e altre malattie. Capire come funziona TWIK-2 è quindi essenziale sia per la biologia di base sia per la progettazione di terapie mirate.
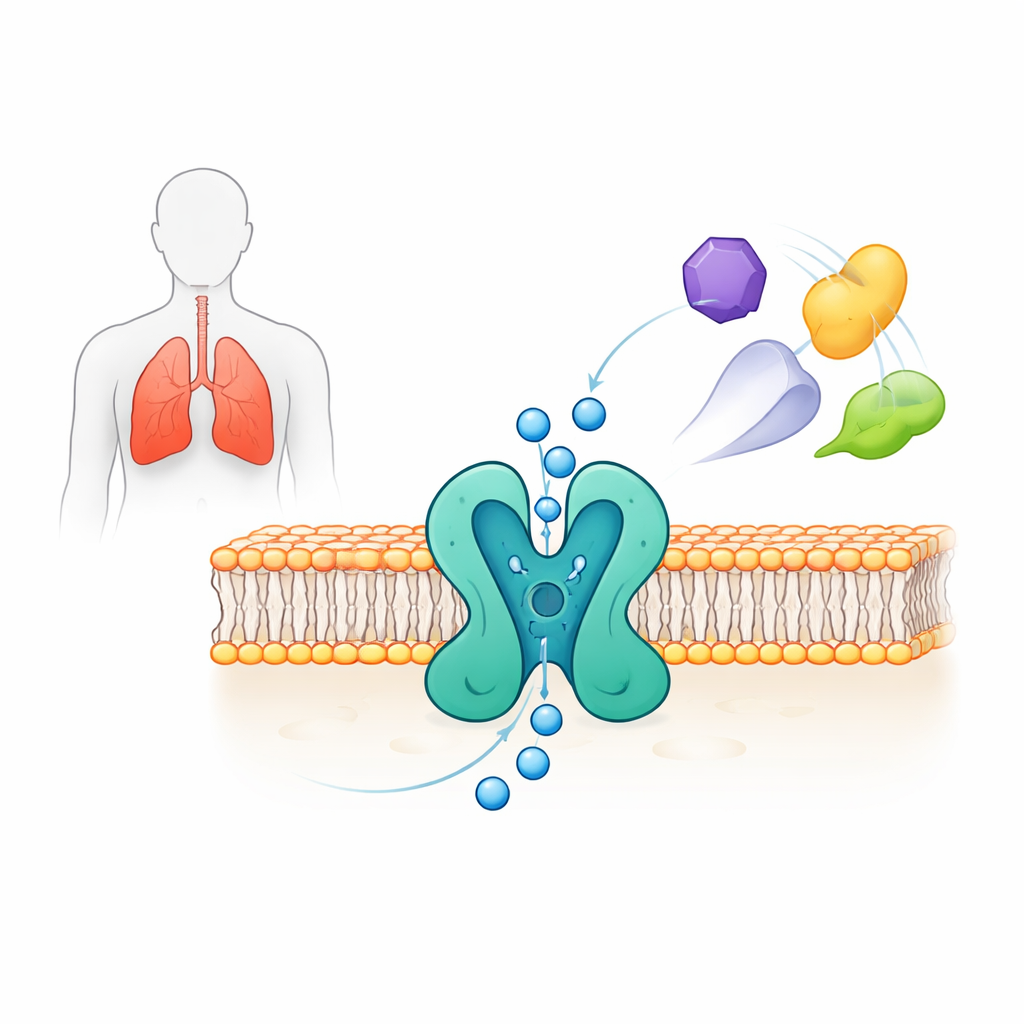
Vedere il cancello a livello atomico
I ricercatori hanno espresso il TWIK-2 umano a lunghezza intera in linee cellulari umane e hanno usato la criomicroscopia elettronica single-particle per determinarne la struttura tridimensionale a una risoluzione di circa 3,7 angstrom. Il canale forma un assemblaggio in due parti che insieme crea un poro centrale attraverso cui passano gli ioni potassio. Ciascuna metà contiene quattro segmenti transmembrana e due “eliche del poro” che modellano una regione stretta chiamata filtro di selettività, dove il potassio viene distinto dagli altri ioni. Sopra il poro, due strutture ad arco a forma di “cap” creano due percorsi di ingresso separati per gli ioni dall’esterno della cellula. La struttura rivela inoltre sottili asimmetrie tra i due lati del poro che conferiscono a TWIK-2 un arrangiamento pseudo‑quadripartito, un segno distintivo di questa famiglia di canali.
Lipidi nascosti e un percorso ionico finemente regolato
Lungo il percorso di conduzione ionica, il gruppo ha mappato come gli ioni potassio si muovono dall’interno della cellula, attraverso un “polsino” idrofobico, su per il filtro di selettività e fuori sotto il cap. Il punto più stretto è comunque sufficientemente largo perché il potassio viaggi in fila indiana. Sebbene la proteina sia stata purificata senza l’aggiunta di lipidi, le mappe cryo‑EM hanno mostrato densità tubolari annidate vicino alla parte inferiore del poro e in tasche laterali tra le eliche. Queste densità rappresentano probabilmente lipidi o code di detersivo rimaste attaccate a TWIK-2 durante la purificazione, suggerendo che i grassi naturali della membrana possano annidarsi in queste scanalature e modificare sottilmente la forma delle eliche vicine. Tali spostamenti, in particolare in un’elica chiamata M4 e nelle anse del filtro di selettività, si pensa modulino se il canale sia aperto, chiuso o in uno stato intermedio.
Esplorare il cancello con mutazioni e bloccanti
Per collegare struttura e funzione, gli scienziati hanno utilizzato un sistema di patch‑clamp automatizzato per misurare le correnti in cellule che esprimevano TWIK-2 normale o versioni con specifici amminoacidi modificati. Hanno scoperto che TWIK-2 è fortemente dipendente dal voltaggio ma, a differenza del parente TWIK-1, abbastanza insensibile alle variazioni di acidità esterna. Mutazioni in due treonine conservate alla base del filtro di selettività hanno reso il canale più rapido ad aprirsi e più conduttivo, suggerendo che questi siti agiscano come cerniere chiave che stabilizzano lo stato chiuso. Modifiche all’ingresso e all’uscita del poro hanno alterato la velocità con cui il canale si accendeva e si spegneva, rivelando quanto sia strettamente controllato il percorso ionico. Il team ha poi testato quattro piccole molecole note per modulare canali correlati. Due di esse, ML365 e NPBA, hanno bloccato potentemente TWIK-2, mentre le altre non hanno avuto effetto. Confrontando come varie mutazioni hanno cambiato la sensibilità ai farmaci, gli autori deducono che questi composti probabilmente si legano appena sotto il filtro di selettività e in cavità vicine, e che farmaci diversi utilizzano modalità di legame parzialmente sovrapposte ma distinte.
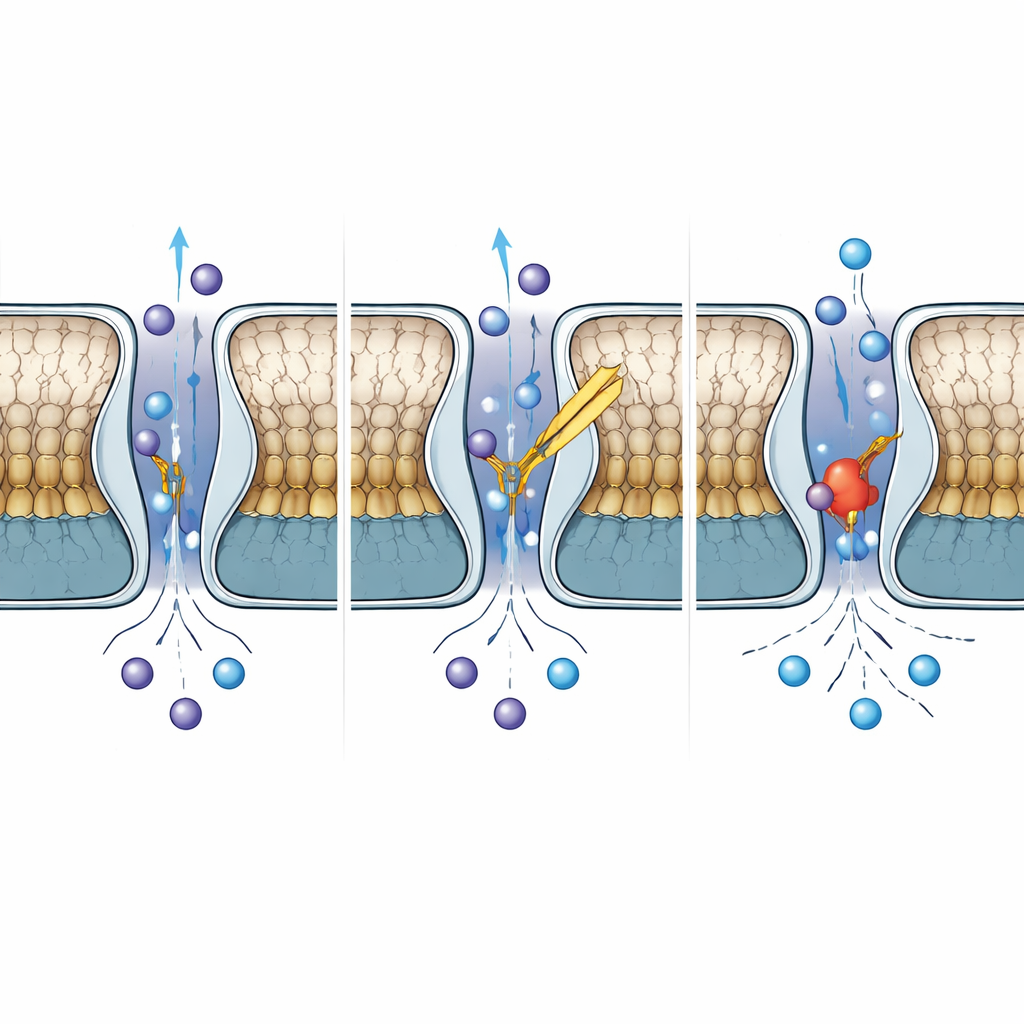
In cosa TWIK-2 differisce dai suoi parenti più stretti
Sebbene TWIK-2 condivida più della metà della sua sequenza con TWIK-1, il loro comportamento diverge in modi importanti. Confrontando TWIK-2 con strutture pubblicate di TWIK-1 a pH neutro e acido, gli autori hanno trovato che la regione del cap di TWIK-2 somiglia alla forma inibita dall’acido di TWIK-1, mentre il suo filtro di selettività resta organizzato come nella forma conduttiva e aperta. Una singola istidina in TWIK-1, nota per rilevare protoni e sporgersi nel poro per bloccare il flusso ionico a pH basso, è sostituita da una tirosina in TWIK-2. Anche quando il gruppo ha reintrodotto un’istidina in questa posizione in TWIK-2, il canale non è diventato sensibile al pH, mostrando che il controllo indotto dal pH in questi canali dipende da una rete più ampia di residui e movimenti, non solo da un singolo amminoacido “interruttore”.
Dalla struttura alle terapie future
Complessivamente, questo lavoro fornisce la prima immagine ad alta risoluzione del TWIK-2 umano e mappa come caratteristiche strutturali specifiche modellano il suo flusso ionico, la risposta al voltaggio e la suscettibilità a piccoli bloccanti molecolari. La scoperta che composti esistenti possono inibire selettivamente TWIK-2, unita a una piattaforma di screening automatizzato robusta, apre la strada a ricerche su larga scala per trovare farmaci più sicuri e potenti. Poiché l’attività di TWIK-2 nelle cellule immunitarie è stata collegata a infiammazione incontrollata, specialmente nei polmoni, tali farmaci potrebbero costituire la base di nuovi trattamenti anti‑infiammatori che agiscono “abbassando” con delicatezza questo minuscolo ma potente cancello nella membrana cellulare.
Citazione: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Parole chiave: canale del potassio TWIK-2, canali K2P a doppia porzione, struttura di canale ionico cryo-EM, modulatori dei canali del potassio, infiammazione polmonare