Clear Sky Science · it
FidlTrack: tracciamento di singole particelle sensibile alla struttura e ad alta fedeltà risolve il moto molecolare intracellulare negli organelli che rilevano l'elaborazione di APP
Osservare singole molecole all'interno delle cellule vive
All'interno di ogni cellula, innumerevoli molecole sono in continuo movimento, urtandosi, legandosi e dissociandosi. I microscopi moderni possono seguire singole molecole una per una, offrendo una visione dettagliata di come funziona la vita alle scale più piccole. Ma quando molte molecole si muovono rapidamente in spazi stretti e tortuosi come il reticolo endoplasmatico o i mitocondri, i loro percorsi si intrecciano e diventano facili da fraintendere. Questo articolo introduce FidlTrack, un nuovo approccio per districare quell'intreccio in modo che i ricercatori possano fidarsi di ciò che osservano quando tracciano singole molecole in tempo reale.
Perché è così difficile tracciare movimenti minimi
Il tracciamento di singole particelle funziona seguendo lo stesso punto luminoso attraverso molti fotogrammi di un filmato. Su una superficie cellulare relativamente piatta, dove le molecole si muovono lentamente e sono distanziate, questo è gestibile. Profondamente all'interno della cellula, tuttavia, le molecole diffondono molto più rapidamente e si ammucchiano in tubi e membrane sottili e avvolte. Tra un fotogramma e il successivo, lo stesso punto potrebbe essersi spostato molto, e più punti identici possono trovarsi a portata. Il software tradizionale deve «indovinare» quale punto nel fotogramma successivo corrisponde alla stessa molecola, e questi indovinelli possono facilmente essere sbagliati. Peggio ancora, percorsi corretti e incorretti possono apparire molto simili, perciò è difficile sapere quali parti dei dati meritino fiducia.
Progettare esperimenti per dati onesti
I ricercatori hanno prima costruito un simulatore realistico che genera filmati di «verità di riferimento» di molecole in diffusione, dove i percorsi reali sono noti. Hanno utilizzato questi set di dati sintetici per testare in modo sistematico come fattori chiave influenzino l'affidabilità del tracciamento: la velocità di movimento delle molecole, quante compaiono in ogni immagine, la frequenza di acquisizione delle immagini e quanto può saltare una molecola tra fotogrammi. Da ciò hanno creato mappe che mostrano, per qualsiasi situazione data, quali impostazioni massimizzano la frazione di movimenti ricostruiti correttamente. Queste mappe rivelano che per molecole che si muovono lentamente a densità moderate il tracciamento può essere molto affidabile, ma per molecole che si muovono rapidamente a densità elevate gli errori crescono rapidamente e aggiungere più molecole non migliora più le informazioni utili.
Individuare ed eliminare passaggi dubbi
I ricercatori hanno poi affrontato un'idea sottile ma potente: l'ambiguità. Un movimento è definito ambiguo quando più di un potenziale punto successivo si trova entro portata, costringendo l'algoritmo a scegliere tra diversi collegamenti plausibili. Utilizzando le loro simulazioni, gli autori hanno dimostrato che una grande parte degli errori di tracciamento deriva da questi passaggi ambigui. Hanno definito un Punteggio di Ambiguità che conta quanto spesso si verificano tali situazioni e poi hanno esplorato cosa accade se tutti i passaggi ambigui vengono rimossi dopo il tracciamento. Questo potatura sacrifica alcuni dati e accorcia i percorsi, ma aumenta nettamente l'affidabilità complessiva di ciò che resta e migliora le stime della velocità di movimento delle molecole. Applicato a filmati reali di un marcatore nel reticolo endoplasmatico, l'ambiguità era maggiore nelle regioni affollate vicino al nucleo cellulare, e rimuovere i collegamenti ambigui ha ripulito quelle aree senza danneggiare le regioni più semplici.
Lasciare che l'architettura cellulare guidi il tracciamento
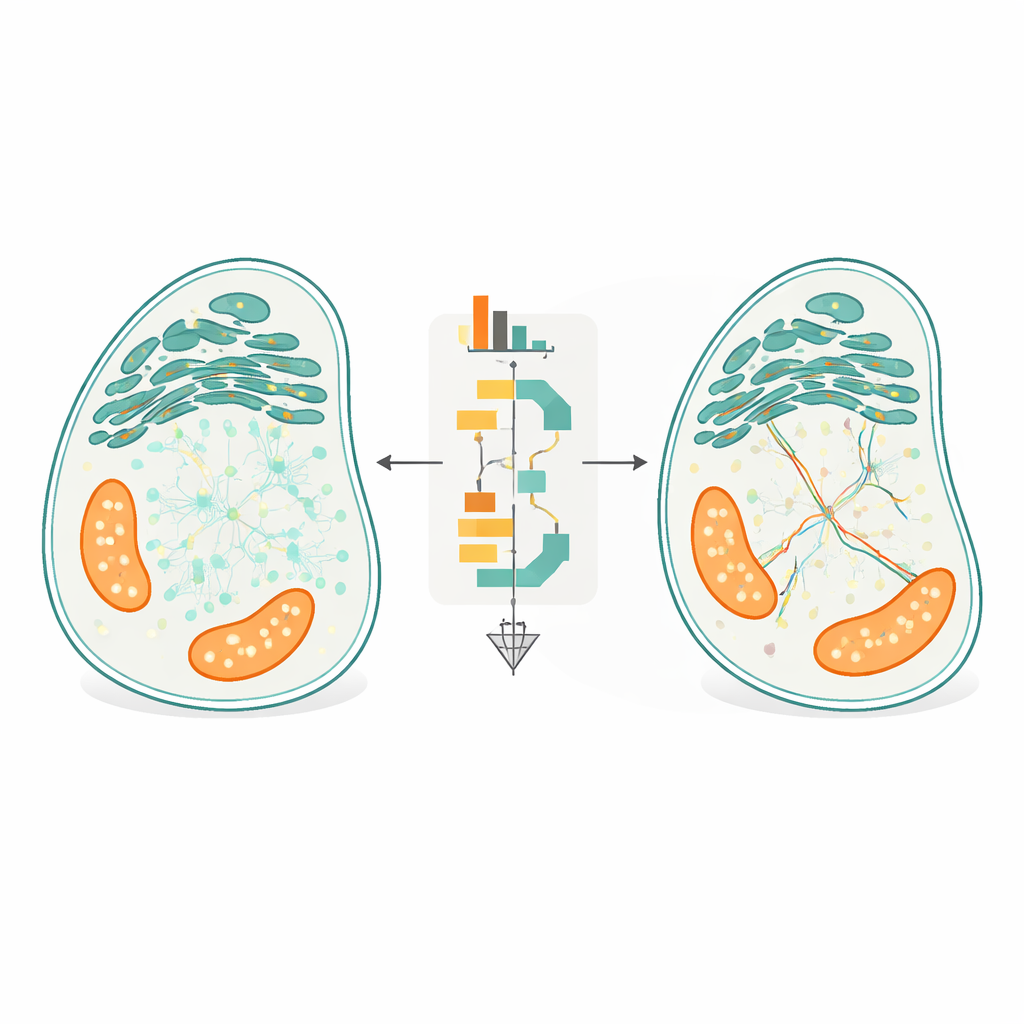
L'innovazione centrale di FidlTrack è il tracciamento «consapevole della struttura». Invece di trattare ogni punto come se si muovesse in uno spazio vuoto, il metodo utilizza immagini dell'architettura interna della cellula — come i contorni del reticolo endoplasmatico, dei mitocondri o delle sottili proiezioni neuronali — per limitare dove le molecole possono realisticamente spostarsi. L'immagine dell'organello viene convertita in un grafo di pixel connessi, e le distanze vengono misurate lungo questo grafo anziché con linee rette nello spazio. I collegamenti che richiederebbero a una molecola di saltare attraverso un gap tra due tubuli separati possono così essere contrassegnati come impossibili e respinti. Nelle simulazioni di tubi strettamente impaccati e nei filmati reali di processi neuronali e organelli, questa consapevolezza strutturale ha ridotto i collegamenti ambigui fino alla metà e aumentato di diversi fattori la quantità di dati di moto non-ambiguo e affidabile.
Rivelare comportamenti cellulari nascosti ed eventi rilevanti per le malattie
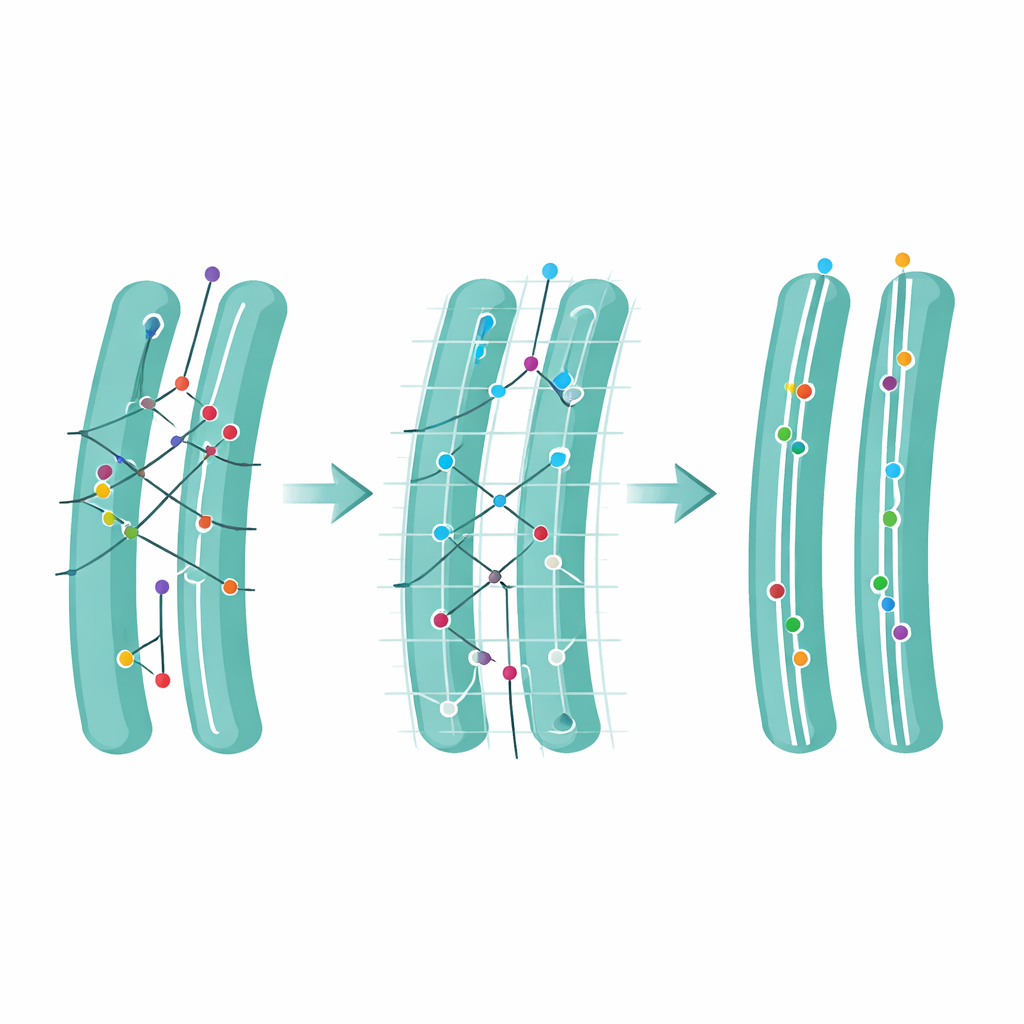
Con questi strumenti — impostazioni ottimizzate, filtraggio dell'ambiguità e consapevolezza strutturale — gli autori hanno riesaminato diverse questioni biologiche che prima erano fuori portata. Nel reticolo endoplasmatico, sono riusciti a tracciare chiaramente come le proteine si muovono mentre interagiscono con siti di uscita che convogliano il carico verso l'apparato di Golgi, distinguendo brevi "passaggi" da permanenze più lunghe. Hanno catturato momenti rari in cui la proteina correlata all'Alzheimer APP viene tagliata dall'enzima BACE1, visibili come un improvviso passaggio da un moto lento ancorato alla membrana a una diffusione libera più rapida. Hanno anche seguito molecole ingegnerizzate simili ad anticorpi nel reticolo endoplasmatico e, dalle variazioni del loro moto, dedotto quando erano legate al bersaglio rispetto a quando fluttuavano liberamente. In questi diversi casi, FidlTrack ha recuperato traiettorie più affidabili e ha evidenziato differenze che il tracciamento standard tendeva a sfumare o sottovalutare.
Cosa significa questo per la biologia cellulare futura
Per i non specialisti, il messaggio chiave è che non tutte le tracce di singole molecole sono uguali: alcune sono affidabili, altre fuorvianti, e fino ad ora era difficile discriminarle. FidlTrack offre un modo pratico e open source per misurare quanto sia affidabile un dato set di dati e per migliorarne l'affidabilità regolando le condizioni sperimentali, eliminando i passaggi ambigui e usando la geometria stessa della cellula come guida. Questo rende possibile osservare con maggiore fiducia come le molecole navigano l'intrico interno della cellula e rilevare eventi rari o sottili, dal triage delle proteine ai processi rilevanti per le malattie, che prima erano sepolti nel rumore.
Citazione: Parutto, P., Yuan, Y., Davì, V. et al. FidlTrack: high-fidelity structure-aware single particle tracking resolves intracellular molecular motion in organelles sensing APP processing. Nat Commun 17, 2639 (2026). https://doi.org/10.1038/s41467-026-69067-y
Parole chiave: tracciamento di singole particelle, dinamiche intracellulari, struttura degli organelli, moto delle proteine, malattia di Alzheimer