Clear Sky Science · it
Myofibroblasti Tenascin C+ esacerbano l’iperplasia neointimale vascolare propagando interazioni nervo-macrofago nei topi
Quando i vasi sanguigni si riparano nel modo sbagliato
Procedure che riaprono arterie ostruite, come l’angioplastica e il bypass, salvano innumerevoli vite. Tuttavia spesso lasciano un problema nascosto: col tempo il vaso trattato può cicatrizzare verso l’interno, restringendosi di nuovo e rimettendo i pazienti a rischio. Questo studio nei topi svela una inattesa conversazione a tre tra cellule di supporto, nervi e cellule immunitarie nella parete vascolare che guida questo eccesso di riparazione dannosa, e individua una molecola chiamata tenascina C come un promettente bersaglio per spezzare il ciclo.
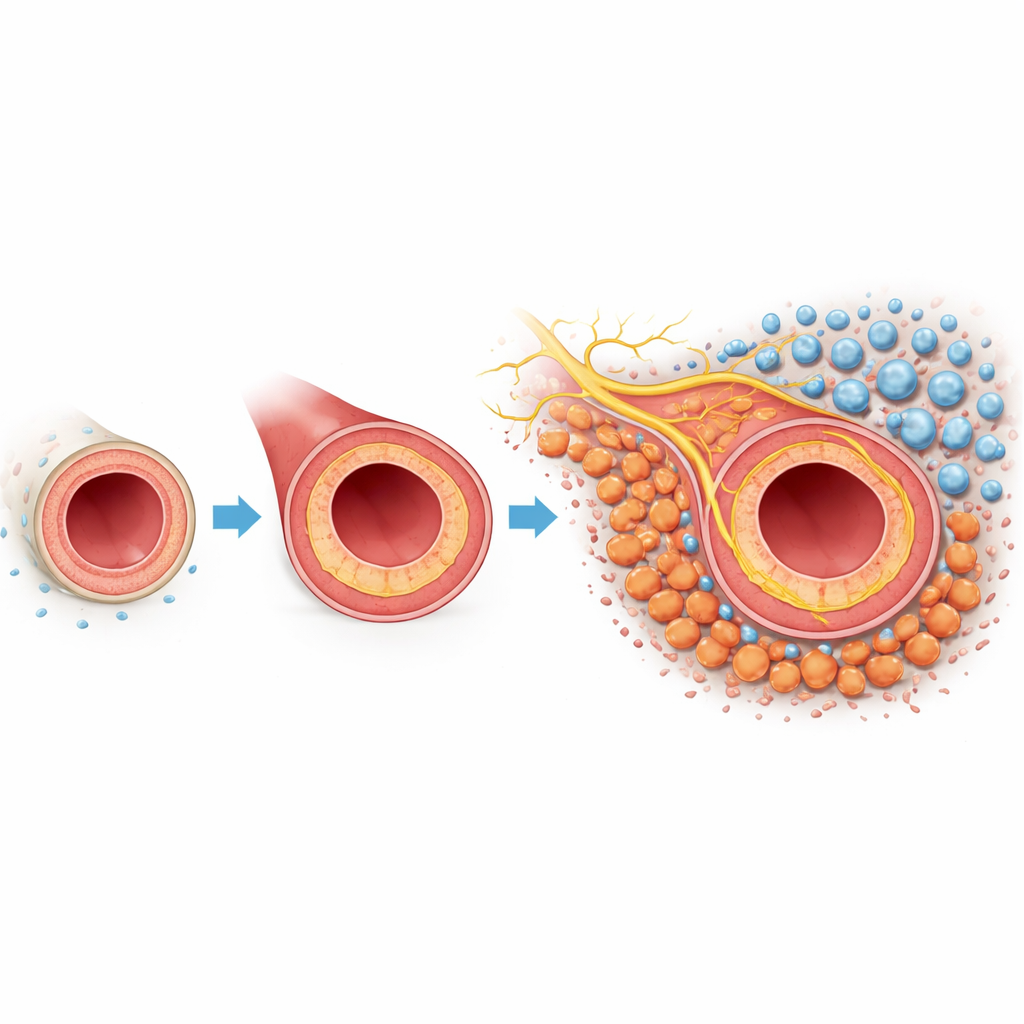
Uno sguardo più attento alla cicatrizzazione problematica nelle arterie
Quando un’arteria viene lesionata o manipolata durante un intervento, il rivestimento interno può ricrescere in modo troppo aggressivo. Questa crescita verso l’interno, chiamata iperplasia neointimale, ispessisce la parete del vaso e riduce il lume attraverso cui scorre il sangue. Lo strato più esterno del vaso, l’avventizia, contiene fibroblasti—cellule di supporto che normalmente mantengono la struttura del vaso. In questo modello murino, dove l’arteria carotide è stata parzialmente legata per mimare un danno, i ricercatori hanno usato il profiling genetico a singola cellula e la mappatura spaziale per catalogare ogni principale tipo cellulare coinvolto. Hanno trovato che i fibroblasti erano particolarmente abbondanti e cambiavano drasticamente comportamento dopo la lesione, suggerendo che queste cellule potrebbero essere attori centrali nella risposta di cicatrizzazione.
L’emergere delle cellule produttrici di cicatrice Tenascin C
Addentrandosi nella popolazione di fibroblasti, il team ha scoperto un sottotipo distinto che compariva solo dopo la lesione. Queste cellule presentavano i caratteri tipici dei miofibroblasti—alti livelli della proteina contrattile actina muscolare liscia α e un altro marcatore chiamato periostina—segnalando che erano passate a una modalità di produzione di cicatrice. Crucialmente, questo sottogruppo produceva anche grandi quantità di tenascina C, una proteina della matrice normalmente scarsa nei tessuti adulti sani ma abbondante nelle malattie e nella riparazione tissutale. Esperimenti in vitro hanno mostrato che esporre fibroblasti avventiziali normali al TGF-β o a tenascina C aggiuntiva li spingeva a diventare questi miofibroblasti Tenascin C–positivi. Le cellule quindi secernevano ancora più tenascina C, creando un circuito auto‑rafforzante attraverso una specifica coppia di recettori di superficie, l’integrina αvβ1, che ampliava progressivamente la popolazione formante cicatrice.
I nervi e le cellule immunitarie si trasferiscono nel quartiere
La storia non si è fermata alla formazione di tessuto cicatriziale. Usando imaging 3D su preparazioni intere e trascrittomica spaziale, i ricercatori hanno osservato che i miofibroblasti ricchi di tenascina C si raggruppavano vicino a fibre nervose in crescita e a cellule immunitarie chiamate macrofagi nella parete esterna del vaso. Le arterie lesionate mostravano nervi sensoriali densi e aggrovigliati e più strutture simili a sinapsi rispetto al normale, sia nei topi sia in campioni umani di arterie con iperplasia neointimale. I macrofagi in queste regioni mostravano un’impronta infiammatoria, producendo molecole come IL‑1β e TGF‑β1 che possono ulteriormente alimentare la cicatrizzazione. Nel complesso, i dati dipingevano il quadro di un microambiente riorganizzato in cui cellule produttrici di cicatrice, nervi e macrofagi si mescolano fisicamente e si influenzano a vicenda.
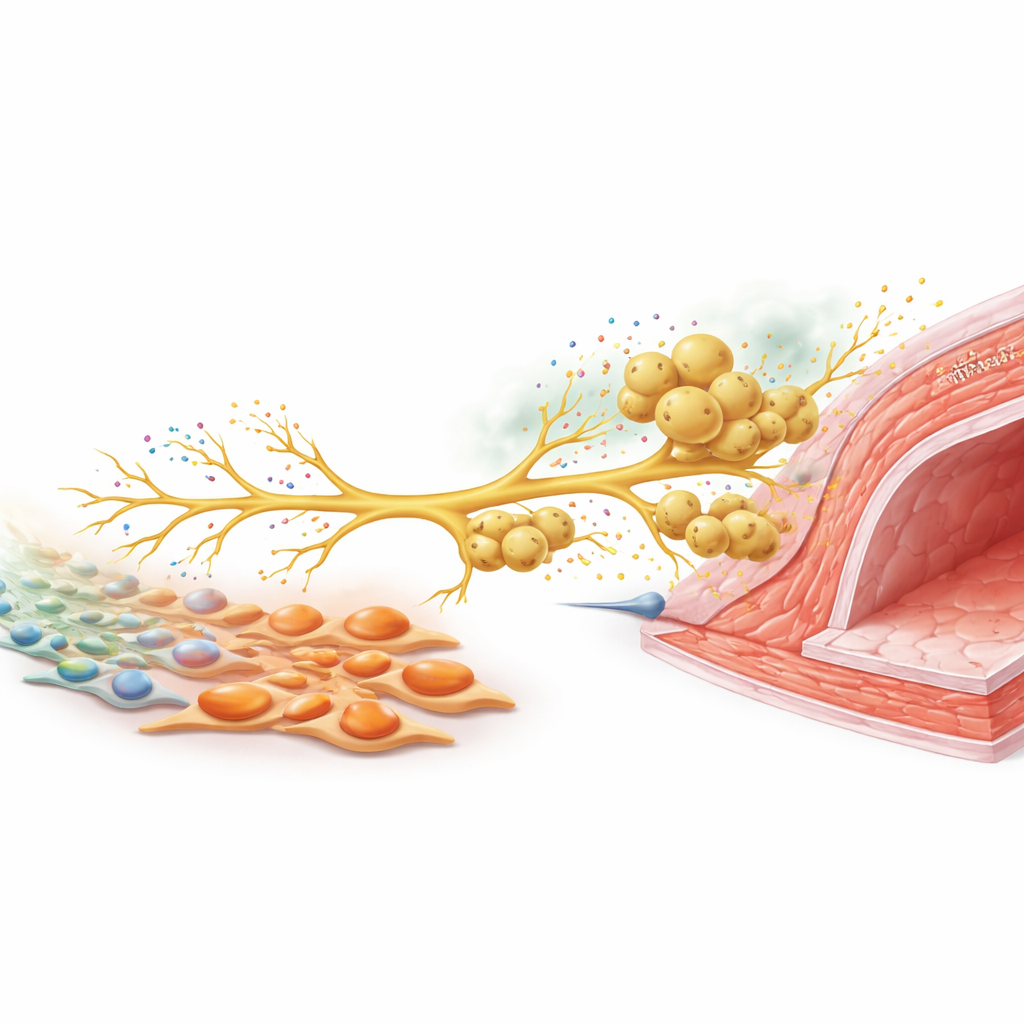
Un segnale nervoso che richiama più difensori
Per capire come questi tipi cellulari comunicano, il team si è concentrato sui nervi sensoriali che rilevano stimoli dannosi. In coltura, i miofibroblasti ricchi di tenascina C hanno aumentato la crescita delle fibre nervose dai neuroni dei gangli della radice dorsale. Nei topi lesionati, questi neuroni sensoriali aumentavano la produzione di CCL2, un segnale chimico ben noto per attrarre macrofagi. Quando neuroni e macrofagi venivano coltivati insieme, i macrofagi migravano lungo le fibre nervose in crescita, proprio come avveniva intorno alle arterie in vivo. Silenziare la produzione di CCL2 nei neuroni riduceva nettamente il reclutamento dei macrofagi. Negli animali, ridurre l’attività dei nervi sensoriali con una tossina, o eliminare selettivamente la tenascina C solo nei fibroblasti, abbassava entrambe la densità nervosa, i livelli di CCL2, l’accumulo di macrofagi e, in ultima analisi, l’ispessimento della parete vascolare. Combinare entrambe le interventi non aggiungeva un beneficio extra, suggerendo che agiscono lungo la stessa via.
Perché questo nuovo percorso è importante
Nel loro insieme, i risultati rivelano un circolo vizioso: la lesione induce i fibroblasti a diventare miofibroblasti produttrici di tenascina C; queste cellule rimodellano la matrice e stimolano i nervi sensoriali; i nervi attivati rilasciano CCL2, che richiama i macrofagi; e i macrofagi secernono fattori infiammatori e fibrotici che peggiorano la cicatrizzazione e restringono l’arteria. Identificando la tenascina C e il suo asse nervo–macrofago come motori centrali di questo circuito, il lavoro suggerisce che terapie mirate a questa molecola o ai suoi partner di segnalazione potrebbero aiutare a mantenere le arterie riparate più a lungo, offrendo ai pazienti una protezione più duratura dopo le procedure cardiovascolari.
Citazione: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Parole chiave: iperplasia neointimale, tenascina C, rimodellamento vascolare, nervi sensoriali, infiammazione dei macrofagi