Clear Sky Science · it
Il paclitaxel promuove l’espansione di macrofagi TREM2+ alla base della sua efficacia terapeutica inferiore rispetto al Nab‑paclitaxel
Perché questo studio è importante
Molte donne con cancro al seno ricevono chemioterapici appartenenti alla famiglia dei taxani, più comunemente paclitaxel o una versione più recente legata a piccole particelle di albumina, nota come nab‑paclitaxel. I medici sospettavano da tempo che il farmaco più nuovo funzioni spesso meglio, ma le ragioni non erano chiare. Questo studio esamina sia i dati dei pazienti sia esperimenti su animali per mostrare che il paclitaxel standard può involontariamente favorire la diffusione del cancro ai polmoni rimodellando le cellule del sistema immunitario e indica una strategia per bloccare questo effetto dannoso.
Due farmaci simili, due esiti diversi
I ricercatori hanno prima confrontato le prestazioni nel mondo reale di paclitaxel e nab‑paclitaxel in migliaia di donne con cancro al seno. Aggregando i risultati di 17 studi clinici che hanno coinvolto 6.486 pazienti, hanno scoperto che il nab‑paclitaxel produceva tassi di riduzione tumorale più alti e una scomparsa più completa del cancro nella mammella e nei linfonodi vicini prima dell’intervento chirurgico. Questo vantaggio era particolarmente marcato nei pazienti trattati dopo il fallimento di terapie precedenti. Eppure entrambi i farmaci venivano somministrati a dosi simili e sono progettati per colpire le cellule tumorali in divisione allo stesso modo, suggerendo che qualcosa al di là della semplice uccisione diretta delle cellule tumorali dev’essere diverso tra loro.
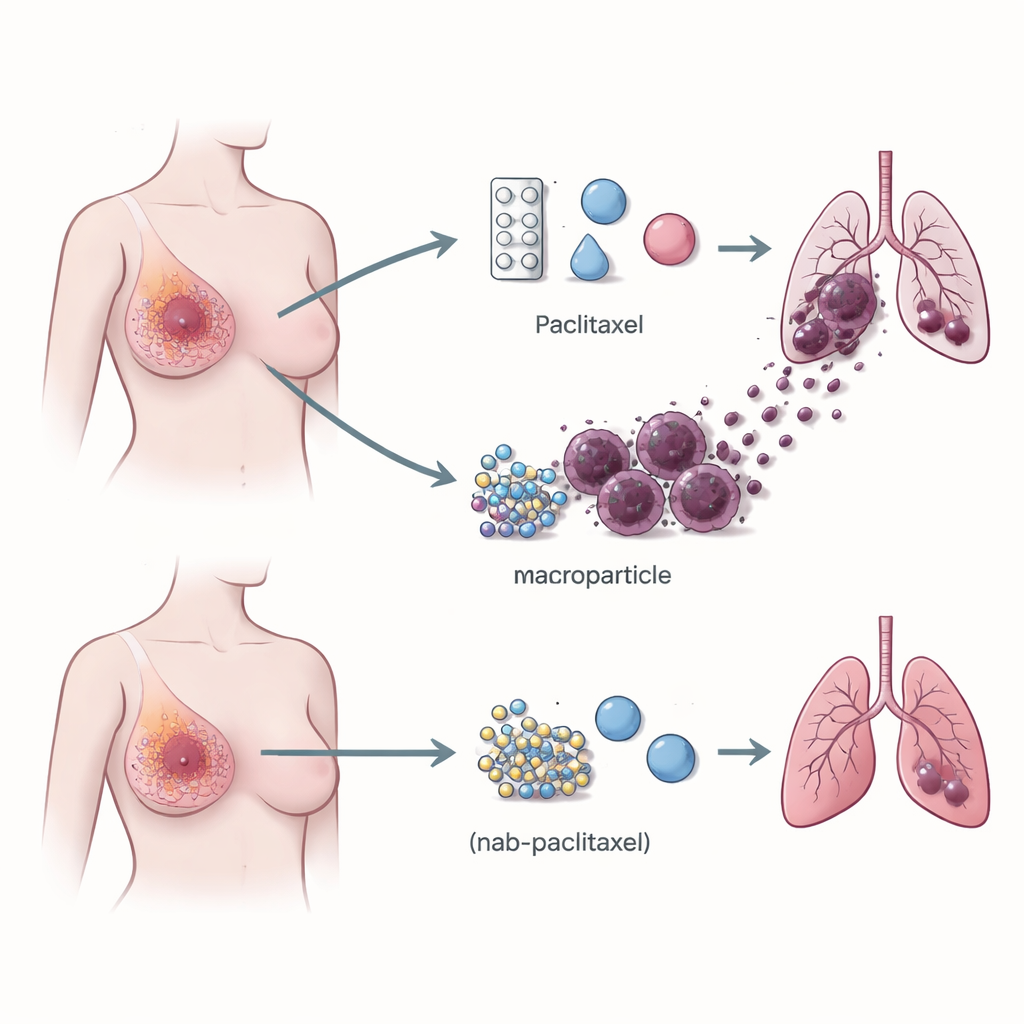
Cellule immunitarie che aiutano il cancro a viaggiare
L’attenzione si è spostata sul microambiente immunitario del tumore — il mix di globuli bianchi che può o combattere il cancro o, sorprendentemente spesso, favorirne la crescita. Utilizzando il sequenziamento dell’RNA a singola cellula, che legge l’attività genica in migliaia di singole cellule, il gruppo ha confrontato i tumori di pazienti trattati con paclitaxel rispetto a quelli trattati con nab‑paclitaxel. Hanno osservato che i tumori trattati con paclitaxel contenevano molti più macrofagi che esprimono sulla superficie un recettore chiamato TREM2. Questi macrofagi TREM2‑positivi erano arricchiti ai margini del tumore e risultavano molto più abbondanti nei pazienti che in seguito svilupparono metastasi polmonari rispetto a quelli il cui cancro rimase localizzato. Questo schema è stato confermato in gruppi più ampi di pazienti e in modelli murini, stabilendo un forte collegamento tra questo tipo di macrofago e il rischio di diffusione del cancro.
Quando la terapia riduce i tumori ma favorisce la diffusione
Nei topi con tumori mammari, il paclitaxel ha fatto ciò che deve fare: ha rallentato o ridotto i tumori primari. Ma allo stesso tempo ha aumentato il numero di depositi tumorali nei polmoni e ha incrementato i macrofagi TREM2‑positivi nei tumori e nel sangue. Il nab‑paclitaxel, al contrario, riduceva le dimensioni del tumore senza promuovere metastasi polmonari né espandere questi macrofagi, pur essendo altrettanto efficace nel ridurre il tumore principale. Quando il gene TREM2 è stato eliminato nei topi, o quando TREM2 è stato ridotto mediante oligonucleotidi antisenso (brevi frammenti di DNA che silenziano geni specifici), il paclitaxel ha continuato a ridurre i tumori primari ma ha in gran parte perso la capacità di favorire la diffusione ai polmoni. Ciò dimostra che i macrofagi che portano TREM2 non sono semplici spettatori; sono partner necessari nella metastasi indotta dal paclitaxel.
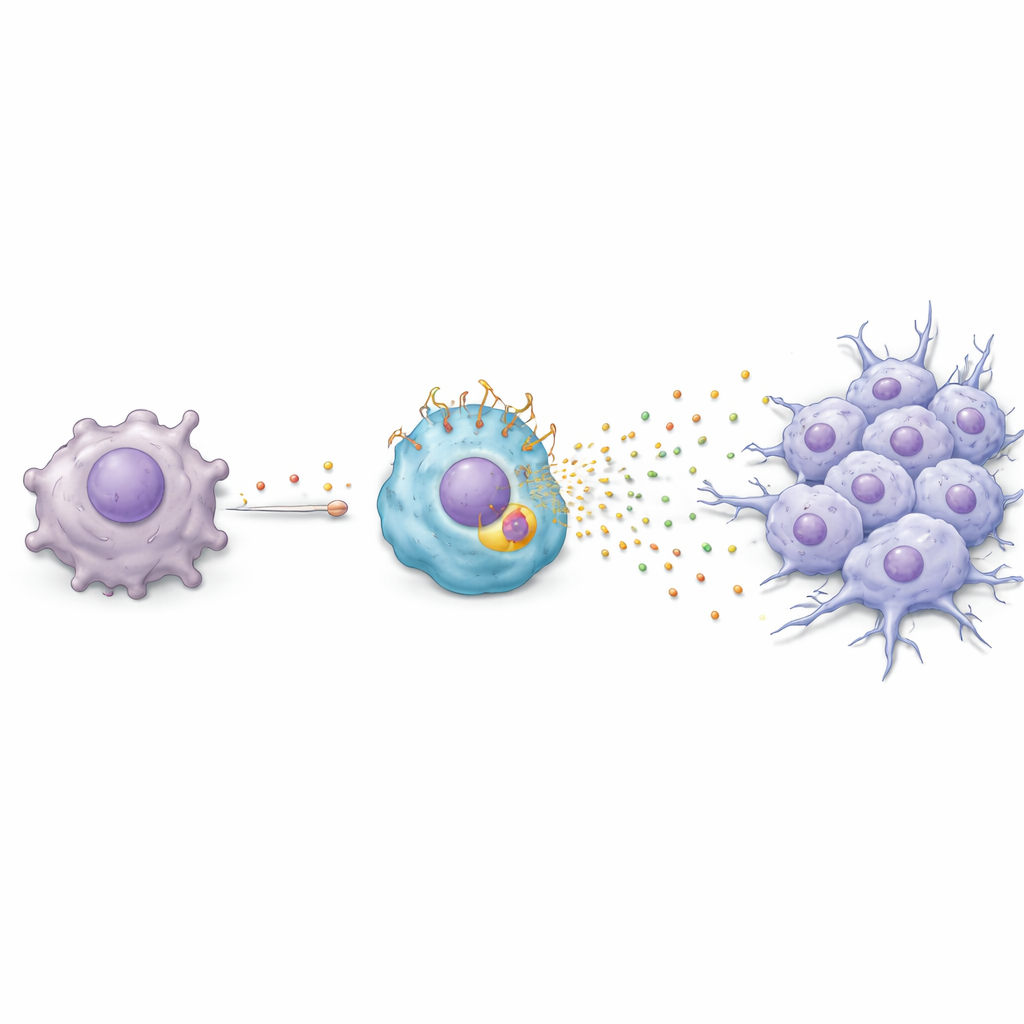
Una catena chimica dal tumore alla cellula immunitaria
Il gruppo si è quindi chiesto come il paclitaxel induca i macrofagi a trasformarsi in questo stato dannoso ricco di TREM2. Hanno scoperto una reazione a catena: il paclitaxel induce le cellule tumorali ad attivare un gene della risposta allo stress chiamato ATF3, che a sua volta aumenta la produzione di un fattore di crescita chiamato FGF2. Le cellule tumorali rilasciano quindi FGF2 nell’ambiente circostante, dove agisce sui macrofagi vicini. In quei macrofagi, FGF2 attiva un altro regolatore, EGR1, che innalza i livelli di TREM2. Una volta che TREM2 è elevato, i macrofagi iniziano a secernere un cocktail di proteine — tra cui Serpin E1, HGF, CCL3 e CXCL2 — che spingono le cellule tumorali verso una forma più mobile e invasiva nota come transizione epitelio‑mesenchimale. In provetta e nei topi, questo dialogo chimico rendeva le cellule tumorali più propense a migrare e invadere, passaggi chiave sulla strada verso le metastasi.
Trasformare una spada a doppio taglio in uno strumento più sicuro
Dal punto di vista divulgativo, il messaggio chiave è che il paclitaxel può agire come una spada a doppio taglio: mentre attacca i tumori, istruisce anche certe cellule immunitarie ad aiutare il cancro a fuggire verso organi distanti. Il nab‑paclitaxel sembra evitare di scatenare questo particolare errore immunitario. La notizia incoraggiante è che bloccare TREM2 — o parti della via di segnalazione FGF2–EGR1–TREM2 — può separare i benefici del paclitaxel nella riduzione del tumore dai suoi rischi nel promuovere le metastasi nei modelli animali. Se strategie simili si dimostrassero sicure ed efficaci negli esseri umani, i medici potrebbero continuare a usare un farmaco chemioterapico familiare e ampiamente disponibile limitando la sua tendenza a favorire la diffusione del cancro, con potenziali migliori risultati a lungo termine per i pazienti.
Citazione: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Parole chiave: cancro al seno, paclitaxel, microambiente tumorale, macrofagi, metastasi