Clear Sky Science · it
Riadattamento affidabile dell’interactoma degli anticorpi all’interno della cellula
Trasformare gli anticorpi in minuscoli strumenti all’interno delle nostre cellule
Gli anticorpi sono noti come armi di precisione del flusso sanguigno, capaci di riconoscere virus e altre minacce. Tuttavia, gran parte dell’azione in molte malattie, tra cui Alzheimer, Parkinson e alcuni tumori, si svolge all’interno delle cellule, dove gli anticorpi convenzionali raramente arrivano o funzionano bene. Questo studio mostra come ricostruire sistematicamente anticorpi esistenti in versioni più piccole—"intrabodies"—che funzionano in modo affidabile all’interno di cellule umane vive, aprendo la strada a nuovi strumenti diagnostici, di ricerca e, potenzialmente, a terapie che operano direttamente nel cuore dei processi patologici.
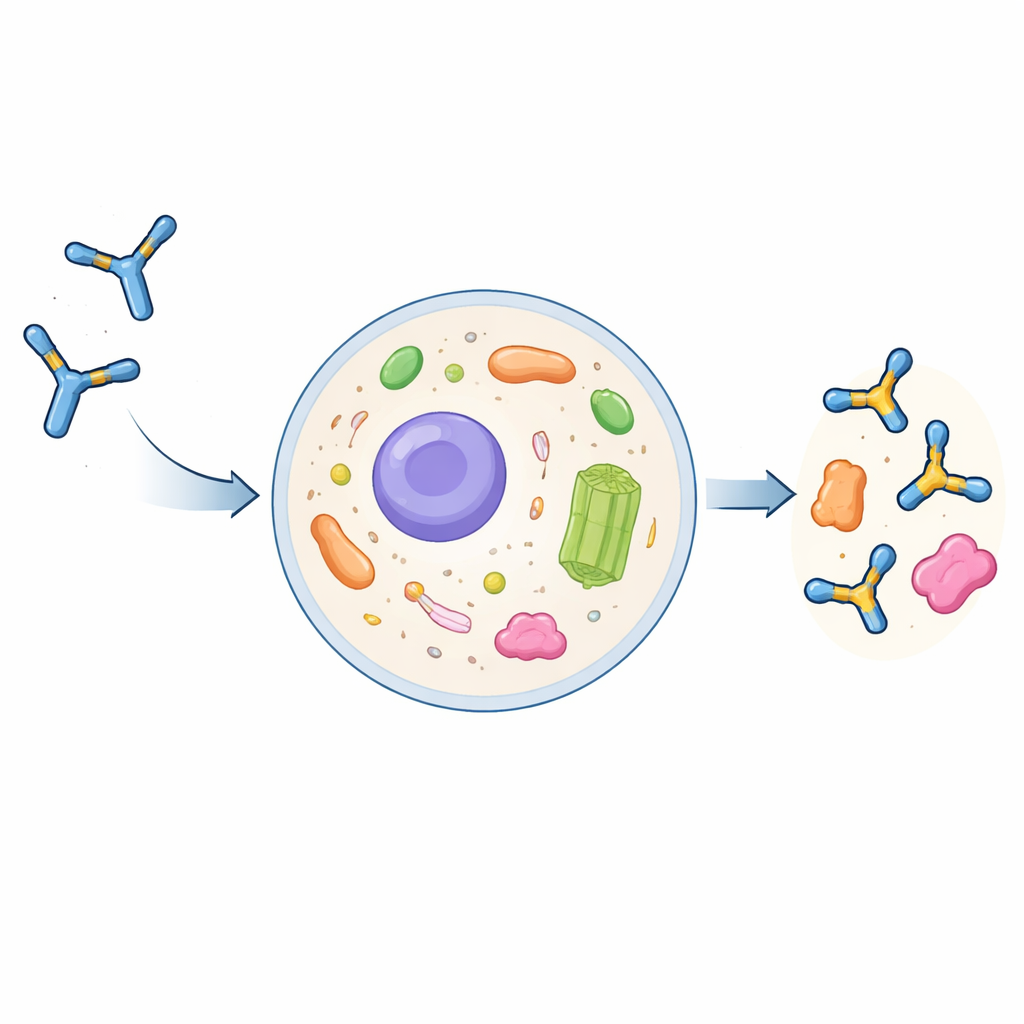
Perché gli anticorpi normali fanno fatica all’interno delle cellule
Gli anticorpi di dimensioni complete sono grandi proteine a forma di Y evolute per operare all’esterno delle cellule. Vengono assemblati e modificati chimicamente nel percorso secretorio della cellula e poi rilasciati nel flusso sanguigno. Se vengono riassorbiti dalle cellule, di solito finiscono in compartimenti degradativi piuttosto che nel fluido interno della cellula, il citoplasma. Gli scienziati possono ridurre gli anticorpi alle loro parti essenziali di riconoscimento, chiamate frammenti variabili a singola catena (scFv), ed esprimerle come intrabodies all’interno delle cellule. Tuttavia, queste intrabodies spesso formano aggregati, diventano insolubili e perdono la capacità di legare i loro bersagli. Fino ad ora non esisteva una ricetta generale e affidabile per trasformare un anticorpo convenzionale in un intrabody ben comportato.
Trovare le regole di progetto per intrabodies solubili
I ricercatori hanno iniziato misurando quanto restassero dissolte 45 diverse intrabodies prodotte in cellule umane. Hanno confrontato sistematicamente molte caratteristiche proteiche—come idrofobicità complessiva, qualità strutturale predetta e proprietà delle anse di legame—per capire quali spiegassero meglio se un’intrabody restasse solubile. È emerso un fattore semplice: la carica elettrica complessiva a pH vicino a quello fisiologico. Le intrabodies con carica netta fortemente negativa avevano molto più probabilità di restare solubili, mentre quelle con carica neutra o positiva tendevano ad aggregare. Altri predittori sofisticati, inclusi i punteggi di confidenza strutturale dal sistema AlphaFold, non correlavano con la solubilità. Ciò ha permesso al team di costruire un modello pratico basato sulla carica che può stimare quanta parte di un’intrabody si troverà nella frazione solubile di un estratto cellulare.
Riprogettare linker e domini per un comportamento migliore
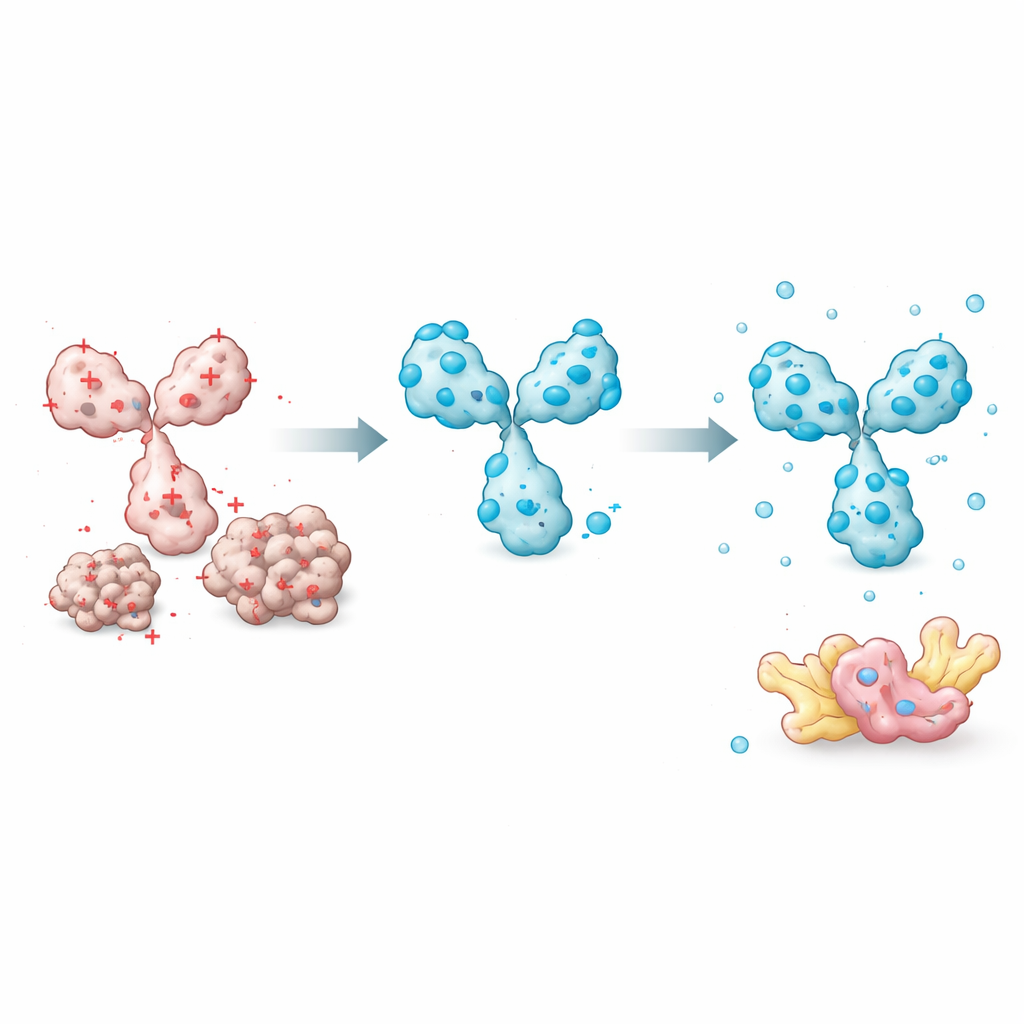
Con questa intuizione, il gruppo si è concentrato su caratteristiche che potevano facilmente modulare senza alterare il riconoscimento del bersaglio. Un elemento chiave è il breve peptide "linker" che collega i due domini variabili. La maggior parte dei progetti esistenti usa linker neutri che non modificano la carica. Sostituendo questi siti con aminoacidi carichi negativamente, i ricercatori sono riusciti ad abbassare la carica complessiva dell’intrabody, migliorandone drasticamente la solubilità pur preservando il legame con il bersaglio. Hanno inoltre scoperto che l’ordine dei domini variabili (se la parte heavy o la light viene prima) e posizioni specifiche del framework al di fuori delle anse di legame influenzano quanto facilmente la proteina si ripiega e resta dissolta. Scegliere un ordine dei domini che protegga le regioni più fragili e introdurre mutazioni mirate di scambio di carica ha ulteriormente aumentato le prestazioni.
Uso dell’intelligenza artificiale per costruire intrabodies su larga scala
Per andare oltre il metodo prova‑ed‑errore uno per uno, gli autori hanno combinato le loro semplici regole di carica con software avanzati di progettazione proteica basati sull’apprendimento profondo. Partendo da spalle di anticorpi note, hanno usato un approccio di “inverse folding” per suggerire nuove sequenze che mantenessero la forma desiderata ma presentassero caratteristiche superficiali—in particolare schemi di carica—favorevoli alla stabilità e alla solubilità. Hanno limitato i cambiamenti nelle anse di legame chiave per preservare il riconoscimento, permettendo però all’algoritmo di riprogettare le superfici circostanti. I test hanno mostrato che molte di queste intrabodies guidate dall’IA non solo erano altamente solubili ma anche più stabili termicamente rispetto a varianti progettate dall’uomo, mantenendo la capacità di legare bersagli rilevanti per la malattia come SOD1 malripiegata, p53, α‑sinucleina e altre proteine associate alla neurodegenerazione.
Costruire una libreria di catturaproteine intracellulare
Applicando queste regole e strumenti su larga scala, il team ha riformattato computazionalmente 672 anticorpi in intrabodies previste funzionare bene all’interno delle cellule. Queste molecole ingegnerizzate coprono oltre 60 diversi bersagli intracellulari, incluse proteine coinvolte nelle malattie di Alzheimer, Parkinson e Huntington, oltre a fattori legati al cancro e modificazioni post‑traduzionali come fosforilazione e acetilazione. Negli esperimenti, intrabodies selezionate sono riuscite a pescare forme proteiche specifiche legate a malattie, come SOD1 mutato o particolari conformazioni di α‑sinucleina, ignorando le versioni normali. Tutte le sequenze sono rilasciate pubblicamente e gli autori forniscono uno strumento web che permette ad altri di stimare la solubilità di un’intrabody dalla sequenza usando lo stesso modello basato sulla carica.
Cosa significa per le future medicine e la ricerca
In termini pratici, questo lavoro trasforma l’enorme collezione esistente di anticorpi—molti già studiati in clinica—in una cassetta degli attrezzi che può essere adattata in modo affidabile per l’uso intracellulare. Seguendo un insieme semplice di regole di progettazione, i ricercatori possono ora creare intrabodies che probabilmente funzioneranno al primo tentativo, risparmiando tempo e costi. Per un lettore non specialista, il messaggio chiave è che gli scienziati hanno trovato un modo semplice per “ricablare” i nostri migliori rilevatori proteici affinché funzionino nell’affollato interno delle cellule vive, dove molte malattie hanno origine. Questo potrebbe accelerare lo sviluppo di nuovi metodi per tracciare, studiare e, eventualmente, trattare condizioni guidate da proteine malripiegate o malfunzionanti.
Citazione: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Parole chiave: intrabodies, ingegneria degli anticorpi, solubilità delle proteine, malattie neurodegenerative, intelligenza artificiale in biologia