Clear Sky Science · it
Dual RNA-Seq in vivo rivela effectori chiave della rottura della barriera epiteliale da parte di un patogeno extracellulare
Come alcuni germi superano le nostre recinzioni cellulari
I nostri organi sono rivestiti da cellule strettamente addossate che funzionano come muri, mantenendo sangue, microbi e tossine al loro posto. Eppure certi germi riescono comunque a insinuarsi tra queste cellule e a diffondersi nel corpo. Questo studio descrive in modo vivido come il batterio responsabile della leptospirosi, una malattia grave e diffusa a livello mondiale, raggiunge silenziosamente organi come fegato e reni e poi usa un espediente che coinvolge il calcio all’interno delle nostre cellule per aprire queste barriere protettive.
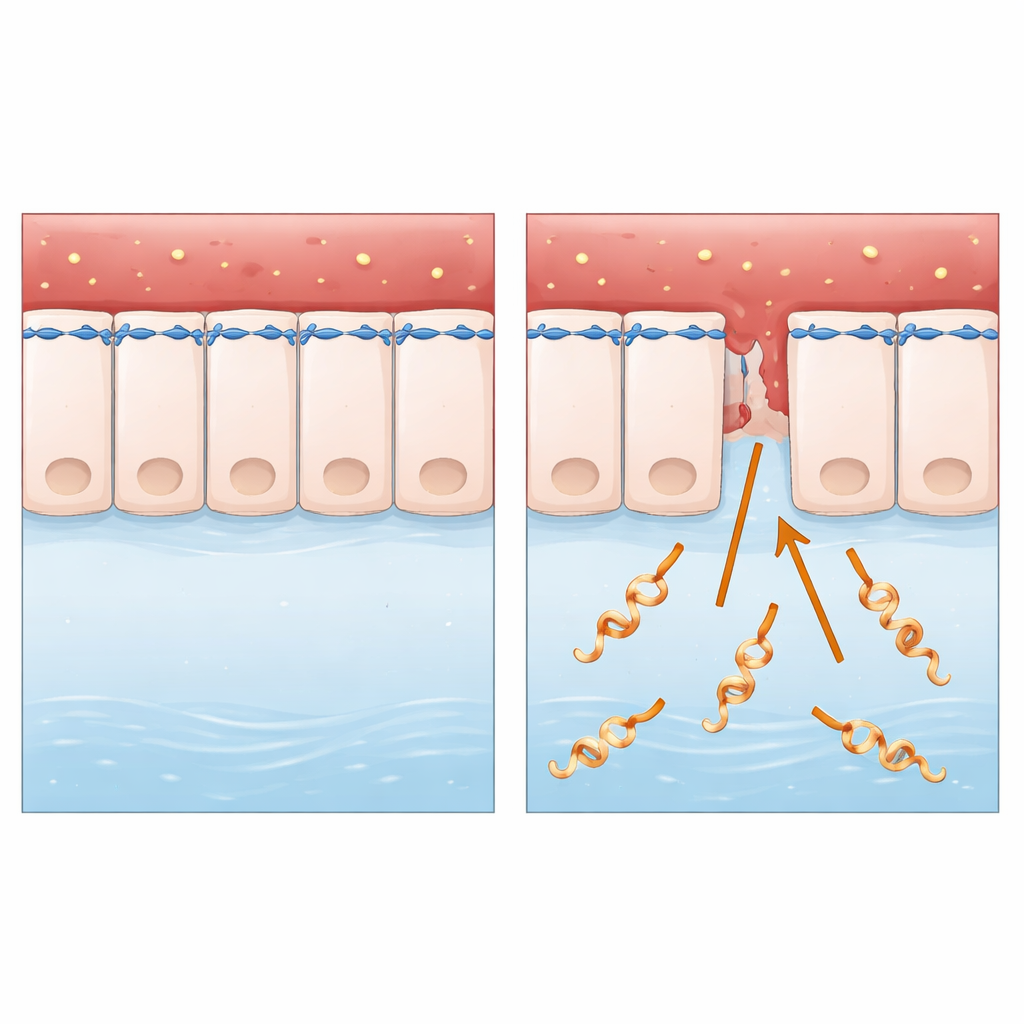
Un invasore furtivo dei tessuti animali e umani
La ricerca si concentra su Leptospira interrogans, un batterio a forma di spirale trasmesso principalmente dagli animali all’uomo tramite acqua o suolo contaminati. Dopo essere entrato tramite piccole lesioni cutanee o mucose, viaggia nel flusso sanguigno e può scatenare malattie gravi, tra cui insufficienza epatica e renale e emorragie interne. A differenza di molti microrganismi ampiamente studiati, Leptospira vive all’esterno delle cellule e manca di alcune delle “armi molecolari” classiche che gli scienziati cercano di solito. Questo lo ha reso un caso di studio ideale per porre una domanda fondamentale: come fa un batterio apparentemente semplice e extracellulare a attraversare strati cellulari intatti in modo così efficiente?
Osservare contemporaneamente i geni dell’ospite e del germe
Per catturare il processo infettivo all’interno di un animale vivente, il team ha utilizzato il sequenziamento RNA duale nei criceti, un modello per la leptospirosi acuta. Questo metodo legge quali geni sono attivati o spenti sia nell’ospite sia nel patogeno contemporaneamente. Gli scienziati hanno infettato i criceti e raccolto tessuto di fegato e rene dopo uno e tre giorni. Nelle fasi iniziali, nonostante l’elevato numero di batteri, le cellule degli animali hanno mostrato pochi cambiamenti nell’attività genica, suggerendo che Leptospira inizialmente sfugge al radar del sistema immunitario. Al terzo giorno, però, entrambi gli organi hanno mostrato una forte reazione, in particolare il fegato: geni coinvolti nell’infiammazione, nelle giunzioni cellula‑cellula e nello scheletro interno delle cellule sono apparsi fortemente alterati, indicando un rimodellamento attivo delle barriere tissutali.
Smontare la cerniera cellulare dall’esterno verso l’interno
Gli strati cellulari sono sigillati da giunzioni strette e giunzioni aderenti, che collegano le cellule vicine e le ancorano a un anello di actina e miosina, la stessa coppia proteica che permette ai muscoli di contrarsi. La microscopia di cellule epiteliali umane infettate con Leptospira ha mostrato che la loro forma cambiava, si aprivano spazi tra le cellule e le proteine chiave delle giunzioni si indebolivano o venivano riposizionate. È significativo che le cellule non morissero, il che indica che la barriera veniva smantellata, non distrutta. I ricercatori hanno anche osservato segnali di stress nelle officine di ripiegamento proteico delle cellule, ma bloccare questo stress non ha ripristinato le giunzioni, indirizzando l’indagine verso un altro sospettato.
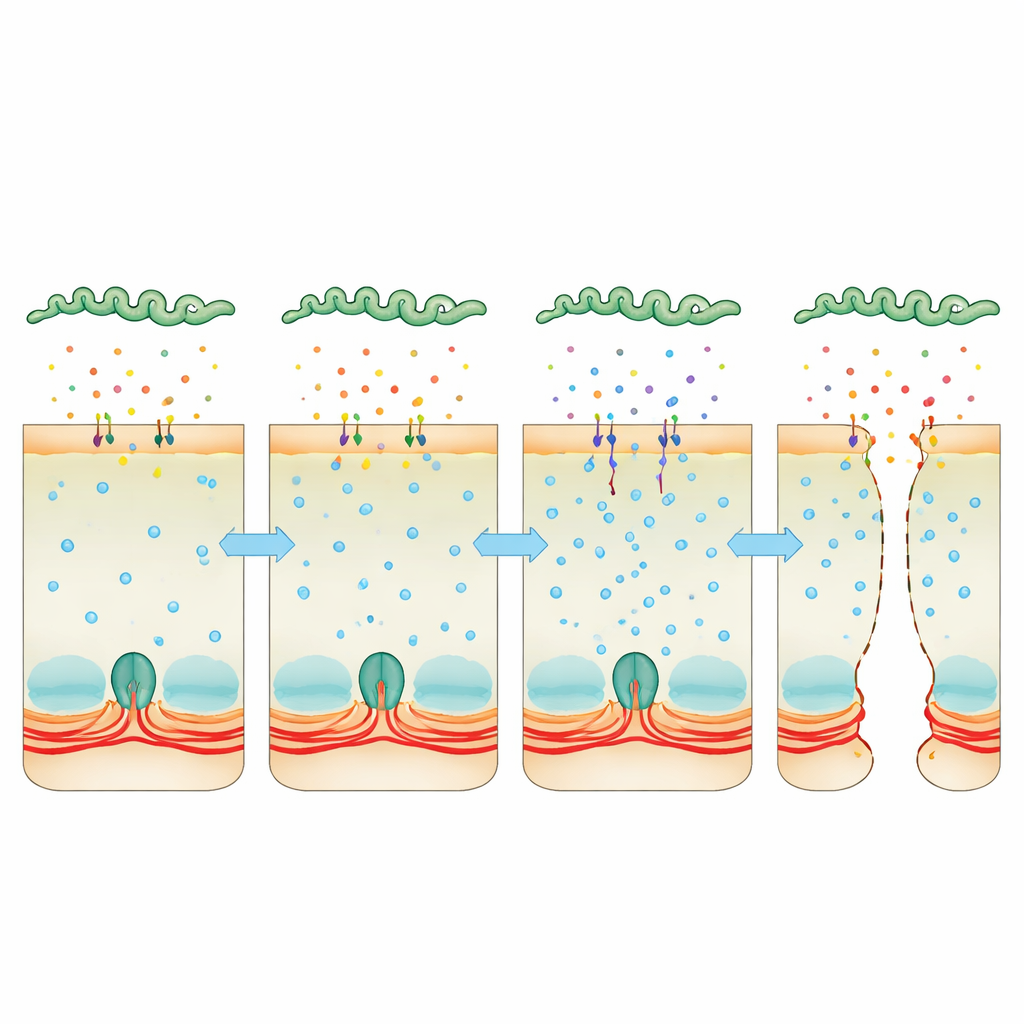
Dirottare il calcio come una leva nascosta
L’attenzione si è spostata sul calcio, un segnale universale all’interno delle cellule che può stringere o rilassare l’anello actina‑miosina. Le cellule infettate accumulavano più calcio, collegato a una maggiore attività della chinasi della catena leggera della miosina, un enzima che fa contrarre l’anello e tirare sulle giunzioni. Quando il team ha usato un composto che sequestra il calcio, o farmaci che inibiscono la calmodulina o questa chinasi, gli strati cellulari si sono mantenuti più integri e i batteri hanno avuto maggiore difficoltà a farsi strada. Allo stesso tempo, il sequenziamento profondo dell’RNA batterico ha rivelato che, all’interno dell’ospite, Leptospira aumenta fortemente la produzione di due proteine “Virulence‑Modifying” che somigliano a tossine. Queste proteine vengono secrete nell’ambiente circostante, si legano alle cellule ospiti e sono rinvenute all’interno di esse. Quando i batteri erano privi di una o di entrambe queste proteine, avevano molta meno capacità di attraversare gli strati cellulari o di causare malattia letale, e il loro brodo secreto non aumentava più i livelli di calcio né smontava le giunzioni con la stessa efficacia.
Cosa significa per la malattia e per le difese future
Nel complesso, i risultati delineano una storia chiara. Dopo essere penetrata nell’organismo quasi inosservata, Leptospira inizia a secernere proteine simili a tossine chiamate Virulence‑Modifying. Queste proteine si legano alle cellule epiteliali e perturbano l’equilibrio del calcio interno, il che a sua volta attiva una via contrattile che scuce la “cerniera” cellulare che mantiene unite le cellule vicine. Allentandosi le giunzioni strette e aderenti, compaiono gap microscopici che permettono ai batteri di passare tra le cellule, colonizzare gli organi e scatenare malattia grave. Identificando questo meccanismo guidato dal calcio e le proteine batteriche coinvolte, lo studio apre la strada a nuove strategie — come bloccare queste proteine o il loro percorso di segnalazione — per rinforzare le nostre recinzioni cellulari e limitare la diffusione della leptospirosi e, possibilmente, di altre infezioni che sfruttano tattiche simili.
Citazione: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Parole chiave: leptospirosi, barriera epiteliale, segnalazione del calcio, tossine batteriche, interazioni ospite‑patogeno