Clear Sky Science · it
La nDIA-MS potenziata con supercaricamento abilita il profiling globale degli spostamenti di solubilità del proteoma indotti dai farmaci
Perché il comportamento delle proteine conta oltre la semplice quantità
I medicinali possono modificare non solo la quantità di una proteina prodotta da una cellula, ma anche dove quella proteina si localizza e se è libera o aggregata su strutture cellulari. Questi spostamenti nel “dove” e nel “come” le proteine esistono all’interno delle cellule sono strettamente legati a malattie come il cancro e le neurodegenerazioni, ma sono difficili da misurare su larga scala. Questo studio presenta un modo rapido e potente per analizzare migliaia di proteine umane contemporaneamente e osservare come la loro solubilità — se sono in uno stato libero o più vincolato — cambia quando le cellule sono esposte a due farmaci sperimentali largamente usati.
Un modo più veloce e nitido per osservare le proteine
Gli autori si basano su una tecnologia fondamentale della biologia moderna: la spettrometria di massa, una tecnica che pesa e conta frammenti proteici. I metodi standard sono già molto efficaci nel dirci quanto di ogni proteina è presente, ma faticano a rivelare cambiamenti nello stato proteico, come il legarsi al DNA o la formazione di assemblaggi densi. Qui i ricercatori perfezionano una versione della spettrometria chiamata acquisizione indipendente dai dati a finestra stretta (nDIA-MS). Aggiungendo piccoli coadiuvanti chimici, detti reagenti di supercaricamento, al liquido che trasporta i peptidi nello strumento, aumentano le cariche elettriche di questi frammenti e potenziano notevolmente il segnale.
Dopo aver testato due additivi di supercaricamento comuni, dimetilsolfossido (DMSO) e m‑nitrobenzilalcol (mNBA), osservano che il 3% di DMSO offre l’aumento di segnale complessivo maggiore e il numero più elevato di proteine rilevate, mentre mNBA è più efficace nell’aumentare il numero e la carica dei singoli frammenti peptidici. Con la configurazione ottimizzata, il gruppo riesce a identificare circa 9.600 proteine umane da appena un microgrammo di un digest cellulare standard in una corsa di 15 minuti — una combinazione notevole di velocità e profondità per esperimenti di routine. Questa prestazione prepara il terreno per usare nDIA-MS non solo per quantificare le proteine, ma anche per sondare come il loro stato fisico risponda allo stress.
Convertire la solubilità in una misura dei cambiamenti cellulari
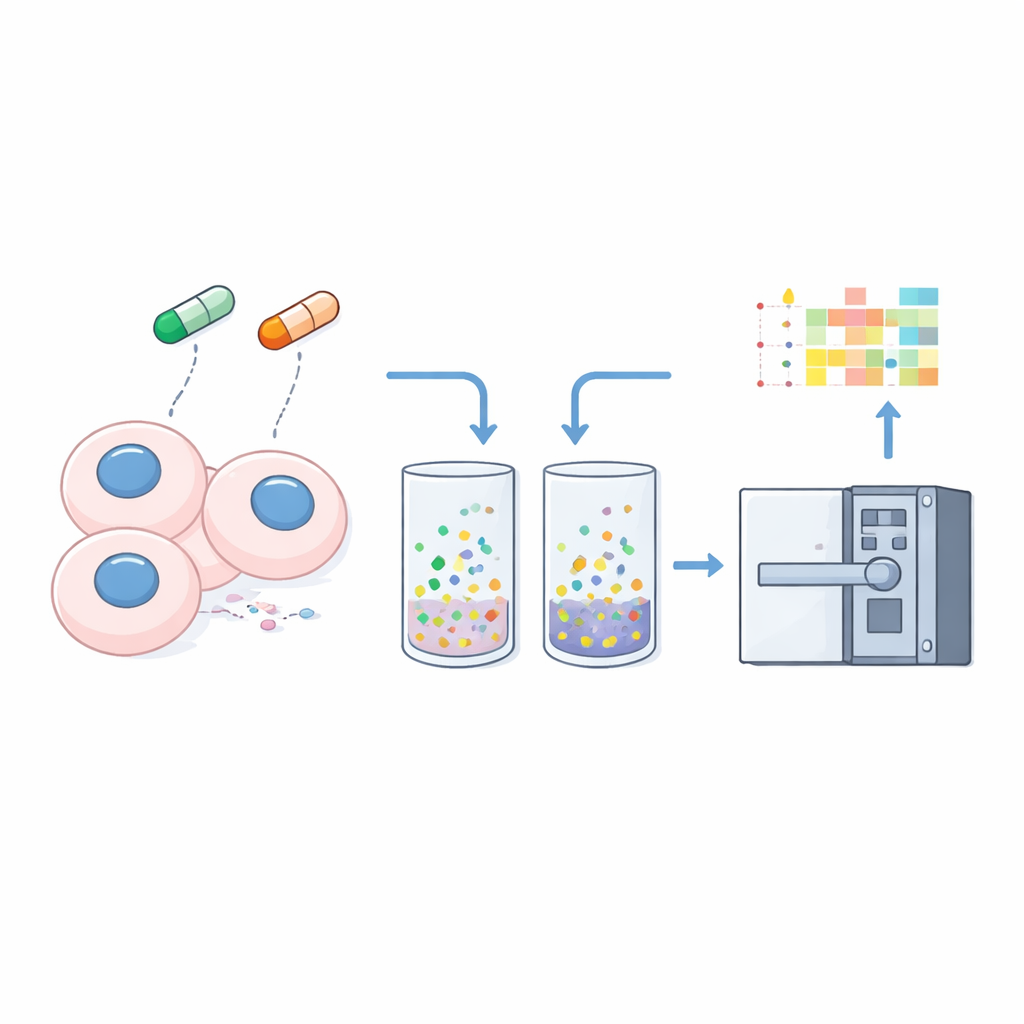
Per trasformare la solubilità in un segnale misurabile, i ricercatori pretrattano delicatamente le cellule con un detergente lieve che estrae le proteine liberamente solubili, lasciando dietro di sé materiale fortemente legato al DNA, alle membrane o ad altre strutture. Analizzano sia il lisato cellulare totale sia questo pellet “insolubile” proveniente da tre linee cellulari tumorali usando il metodo nDIA-MS ottimizzato. Confrontando l’abbondanza di ciascuna proteina nel pellet rispetto al campione totale, calcolano un semplice “rapporto di insolubilità” — valori più alti suggeriscono un’associazione più forte con le strutture cellulari, valori più bassi indicano uno stato più solubile e libero.
Il team poi espone le cellule per solo un’ora a due farmaci: MG132, un bloccante del proteasoma che impedisce alle cellule di degradare proteine indesiderate, e ML‑792, un inibitore dell’attivazione della SUMO che interferisce con un importante sistema di marcatura delle proteine. Questa breve esposizione è deliberata; mira a catturare spostamenti rapidi e precoci nel comportamento proteico prima che i cambiamenti nell’espressione genica si siano completamente manifestati. Anche in questa finestra temporale ristretta, riescono a quantificare cambiamenti di solubilità e abbondanza per 8.694 proteine e confermare che la loro frazionamento separa nettamente le proteine classiche solubili, come la tubulina, dalle proteine legate alla cromatina, come gli istoni.
Farmaci che rimodellano il panorama proteico della cellula
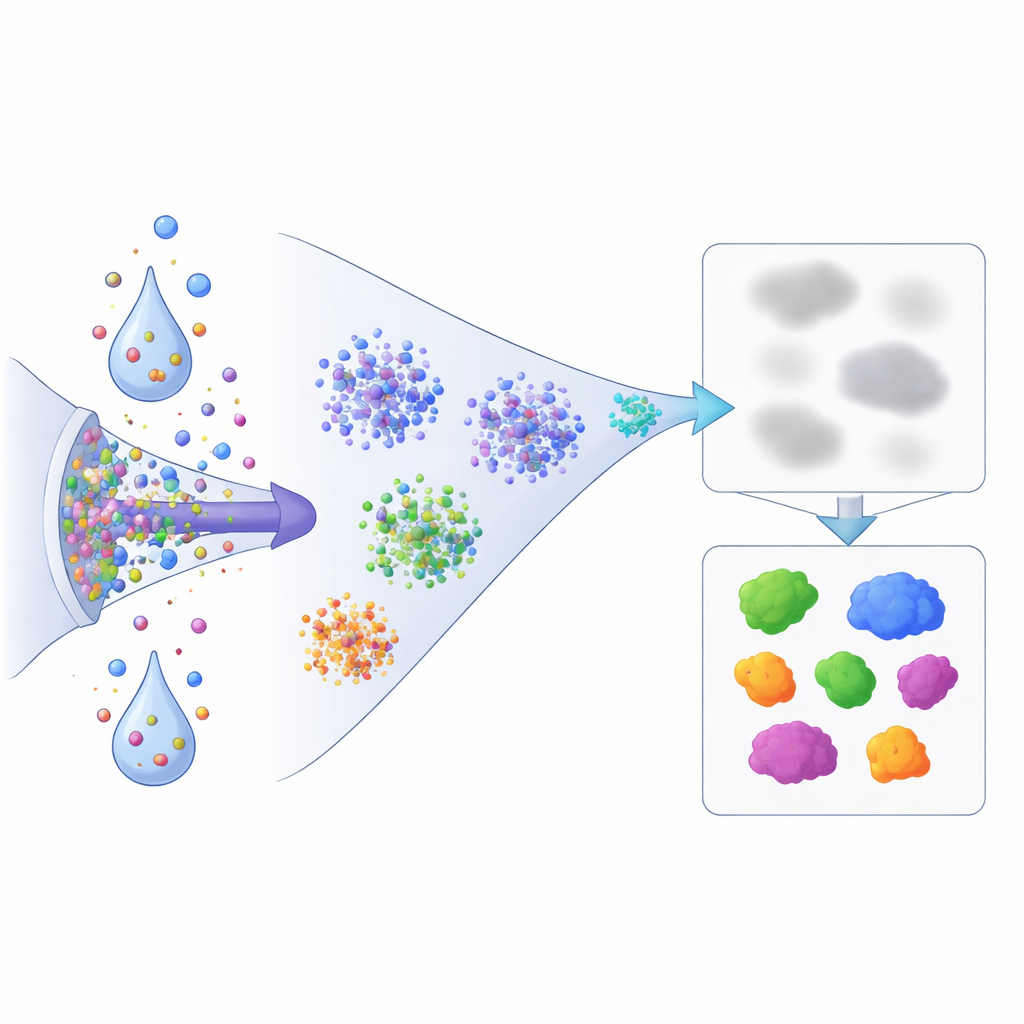
MG132 e ML‑792 producono una rimodellamento diffuso ma distinto della solubilità proteica. MG132 rende oltre mille proteine più insolubili e più di seicento più solubili nelle tre linee cellulari. Molte delle proteine coinvolte si trovano all’intersezione del controllo della qualità proteica, della risposta al danno al DNA, della regolazione genica e dell’autofagia — il sistema di pulizia cellulare. Ad esempio, componenti del complesso attivatore del proteasoma e adattatori che aiutano a marcare le proteine difettose diventano meno solubili, suggerendo che quando la degradazione è bloccata, i fattori chiave del controllo qualità si ritrovano intrappolati su strutture come la cromatina o le membrane cellulari. Proteine legate all’autofagia e attori della risposta al danno, incluso il regolatore dello stress HSF1, si spostano anch’essi verso stati più insolubili simili a condensati, coerenti con la formazione di corpi di stress nucleari.
ML‑792, al contrario, colpisce in modo marcato proteine coinvolte nella trascrizione e nel sistema SUMO stesso. Centinaia di proteine diventano o più insolubili o più solubili quando l’attivazione della SUMO è bloccata, e le proteine SUMO centrali si spostano nel pool solubile, come previsto. Lo studio mette in evidenza comportamenti notevoli: sottounità della RNA polimerasi III diventano più insolubili, suggerendo un import nucleare alterato o un legame con la cromatina; repressori chiave associati ai corpi nucleari, come SP100 e DAXX, diventano più solubili, indicando che i marcatori SUMO contribuiscono a mantenerli sequestrati in questi compartimenti. Quando entrambi i farmaci sono applicati singolarmente o in sequenza, alcune proteine, inclusi NAB2, SMAD2 e RB1, mostrano spostamenti di solubilità coordinati o addirittura opposti, rivelando un’interazione sfumata tra i sistemi di marcatura ubiquitina e SUMO nel controllo della localizzazione proteica.
Implicazioni per la scoperta di farmaci futura
Per i non specialisti, il messaggio centrale è che le proteine non si limitano a salire o scendere in quantità quando le cellule sono sotto stress o trattate con farmaci; si spostano, condensano e cambiano quanto strettamente sono legate alle strutture cellulari. Questo lavoro fornisce un modo ad alta velocità e su scala di proteoma per osservare questi spostamenti. Combinando un workflow di spettrometria di massa ottimizzato con un semplice confronto solubile‑versus‑insolubile, gli autori dimostrano che farmaci sperimentali comuni riorganizzano rapidamente il panorama proteico interno in modi che le misure standard di abbondanza non rileverebbero. L’approccio apre la strada a mappare come i candidati farmaci rimodellino gli stati proteici in tutta la cellula, aiutando i ricercatori a scoprire bersagli inattesi, vie di stress e punti di rottura che potrebbero essere cruciali per comprendere sia l’azione terapeutica sia gli effetti collaterali.
Citazione: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Parole chiave: solubilità del proteoma, spettrometria di massa, inibitore del proteasoma MG132, inibitore della SUMOilazione ML-792, transizioni di stato delle proteine