Clear Sky Science · it
Architettura interna progettata di nanoparticelle lipidiche core-shell favorisce un efficiente rilascio endosomico di mRNA
Perché questo nuovo trucco di delivery è importante
Molti dei farmaci più promettenti, dai vaccini contro la COVID-19 ai trattamenti sperimentali contro il cancro, si basano su RNA messaggero, o mRNA. Ma esiste un problema persistente: una volta che questi filamenti fragili entrano nelle nostre cellule, la maggior parte di essi resta intrappolata e viene distrutta in piccole sacche interne chiamate endosomi. Questo studio introduce una riorganizzazione intelligente delle piccole bolle lipidiche, note come nanoparticelle lipidiche, che trasportano l’mRNA. Riorganizzando la loro struttura interna attorno a un nucleo d’oro solido, i ricercatori migliorano drasticamente la quantità di mRNA che riesce a fuggire nello spazio di lavoro della cellula, dove può effettivamente produrre proteine utili.
Un progetto corporeo migliore per i piccoli corrieri
I vaccini e le terapie a mRNA attuali si basano per lo più su particelle morbide e amorfe costituite da una miscela di lipidi che avvolgono l’mRNA. In teoria, lipidi “ionizzabili” presenti in queste particelle dovrebbero assumere carica positiva nell’interiore acido degli endosomi e lacerare la membrana endosomica, liberando l’mRNA. In pratica, la carica negativa dell’mRNA annulla gran parte di questo effetto, perciò solo circa il 2% dell’mRNA somministrato raggiunge la macchina cellulare per la produzione di proteine. Gli autori si sono posti una domanda semplice ma potente: invece di cambiare soltanto la chimica dei lipidi, che succede se riprogettano l’architettura interna della particella per controllare dove si trovano l’mRNA e i lipidi l’uno rispetto all’altro?
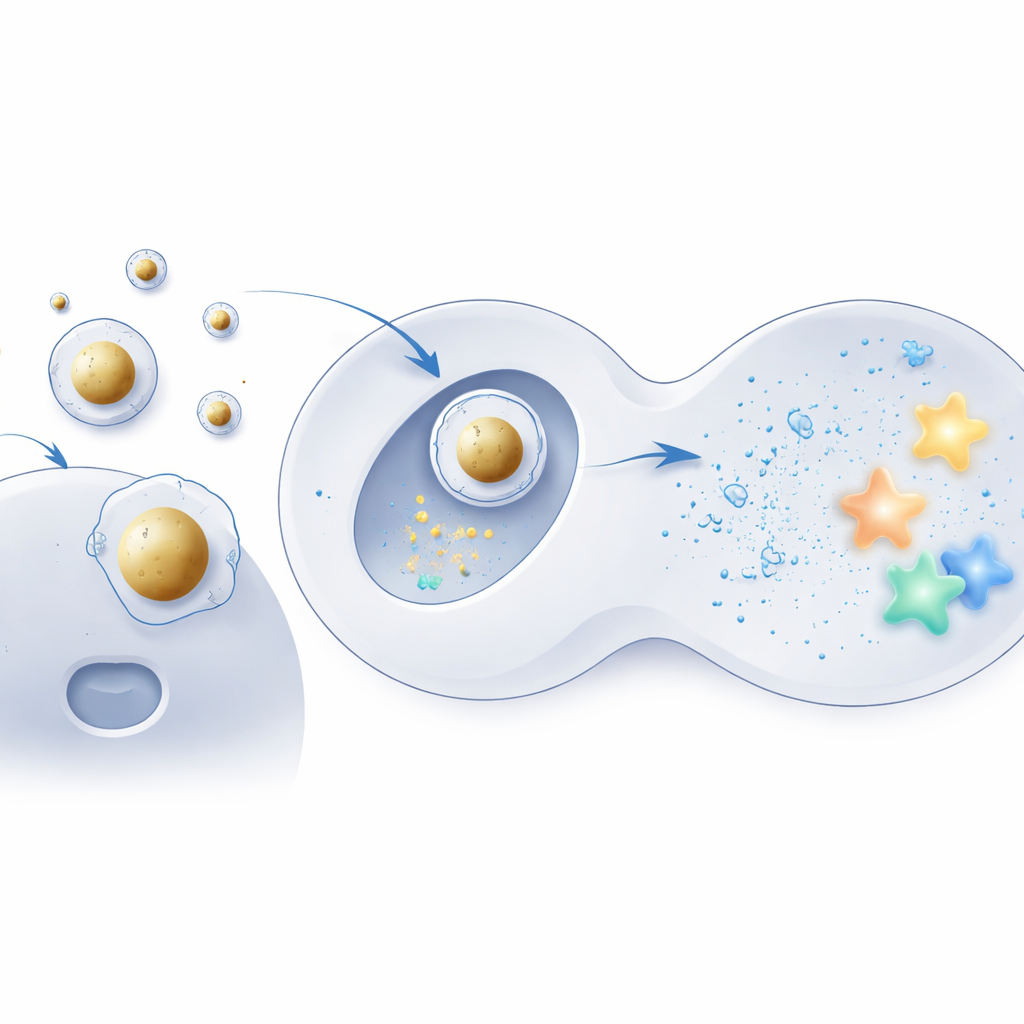
Costruire un guscio di delivery centrato sull’oro
Per mettere alla prova questa idea, il team ha usato piccole sfere d’oro come nuclei rigidi e le ha ricoperte con gli stessi lipidi ionizzabili usati nelle formulazioni convenzionali. L’mRNA carico negativamente è stato prima condensato su questi nuclei e solo in seguito l’assemblato è stato avvolto in una miscela familiare di lipidi ausiliari e molecole stabilizzanti, creando una struttura ordinata core–shell. Microscopia elettronica e simulazioni al computer hanno mostrato che queste “Au‑LNP” erano altamente uniformi, termodinamicamente stabili e mantenevano bene la loro forma in condizioni acquose simili a quelle biologiche. Importante, la composizione lipidica complessiva rimaneva la stessa delle particelle standard, isolando la struttura interna — non gli ingredienti — come il cambiamento chiave.
Come un interno riorganizzato favorisce la fuga
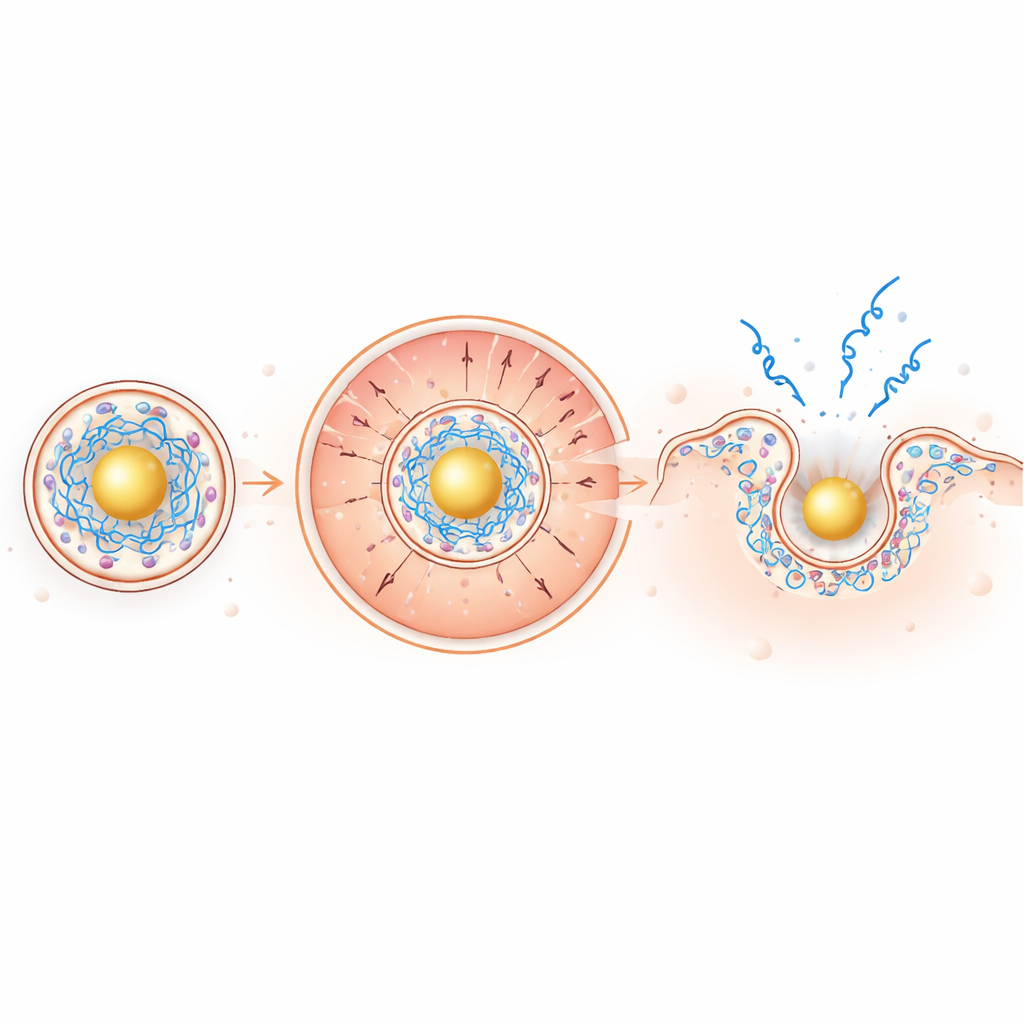
All’interno del lieve ambiente acido degli endosomi, il nucleo a base d’oro diventa fortemente positivo, attirando l’mRNA carico negativamente verso l’interno mentre spinge i lipidi ionizzabili carichi positivamente verso l’esterno, in direzione della membrana circostante. Questa segregazione guidata dalle cariche concentra i lipidi capaci di perturbare la membrana esattamente dove sono necessari. Nei test su membrane modello e su globuli rossi, le nuove particelle sono risultate più efficaci nel perforare le membrane a pH basso restando inerti a pH neutro, una caratteristica di sicurezza desiderabile. Nelle cellule vive, l’imaging dell’mRNA fluorescente ha rivelato circa un aumento di due volte nella fuga endosomica e un sorprendente aumento di circa 100 volte nella diffusione dell’mRNA nel citoplasma rispetto alle particelle convenzionali.
Da colture a topi: segnali più forti e protezione aumentata
Questi vantaggi fisici si sono tradotti in veri guadagni biologici. In diversi tipi cellulari, le particelle con nucleo d’oro hanno indotto una produzione di proteine reporter molto più elevata rispetto alle formulazioni standard, specialmente a basse dosi. Nei topi, hanno aumentato la produzione di proteine dirette dall’mRNA fino a cinque‑sette volte dopo iniezioni nel muscolo o nelle vene, senza modificare la distribuzione corporea preferenziale delle particelle. Quando impiegate per veicolare un vaccino a mRNA per la proteina Spike del SARS‑CoV‑2, le particelle riprogettate hanno approssimativamente raddoppiato i livelli di anticorpi dopo la prima dose e li hanno ulteriormente aumentati dopo un richiamo, producendo anche anticorpi neutralizzanti del virus più potenti. In un impegnativo modello di carcinoma mammario triplo negativo, i vaccini antitumorali a mRNA veicolati dalle nuove particelle hanno ridotto i tumori in modo più efficace, abbassato i segnali di attività tumorale e prolungato notevolmente la sopravvivenza.
Sicurezza e un percorso verso medicine future
Nonostante l’uso dell’oro al loro interno, le particelle sono apparse ben tollerate nei topi. Pesi corporei, marcatori infiammatori e esami tissutali non hanno mostrato tossicità importante, e i livelli di oro negli organi sono tornati verso il basale entro due giorni. Gli autori sottolineano che l’oro serve principalmente come scaffold proof‑of‑concept: lo stesso principio di design interno potrebbe essere applicato ad altri materiali sicuri o biodegradabili. Il messaggio centrale per i non specialisti è che il modo in cui impacchettiamo l’mRNA all’interno del suo piccolo vettore può contare quanto ciò con cui lo impacchettiamo. Dando alle nanoparticelle lipidiche una disposizione interna più disciplinata, questo lavoro offre un nuovo modo per superare un collo di bottiglia di lunga data nella consegna di mRNA — sbloccando vaccini e terapie più efficaci contro malattie infettive, cancro e oltre.
Citazione: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Parole chiave: consegna di mRNA, nanoparticelle lipidiche, fuga endosomica, nanomedicina, vaccini a RNA