Clear Sky Science · it
FGF13 funziona come regolatore dell’asse ERK/glicolisi aerobica nello stato infiammatorio durante il danno polmonare settico
Perché questo studio è importante per i pazienti con infezioni gravi
La sepsi è una complicanza potenzialmente letale di un’infezione che può provocare il collasso respiratorio in poche ore, costringendo i pazienti a ventilazione assistita e a un elevato rischio di morte. Questo studio esplora una proteina poco conosciuta all’interno delle nostre cellule, chiamata FGF13, e mette in luce come contribuisca a guidare l’infiammazione incontrollata e il consumo energetico eccessivo che danneggiano gravemente i polmoni durante la sepsi. Tracciando questo circuito di controllo nascosto, il lavoro indica nuovi bersagli farmacologici che potrebbero calmare la tempesta nei polmoni senza spegnere l’intero sistema immunitario dell’organismo.
Un attore nascosto nel danno polmonare da sepsi
I ricercatori hanno cominciato confrontando tessuto polmonare di topi e pazienti umani settici con tessuto di controlli non settici. Hanno esaminato una famiglia di molecole note come fattori di crescita dei fibroblasti, che contribuiscono al mantenimento della salute polmonare. Tra questi, FGF13 è emerso come particolarmente significativo: i suoi livelli risultavano marcatamente ridotti nei polmoni dei pazienti e degli animali settici. Mappando la localizzazione di FGF13, lo hanno trovato principalmente all’interno di due tipi cellulari chiave: le cellule endoteliali, che costituiscono il rivestimento interno dei vasi sanguigni, e i macrofagi, cellule immunitarie che percepiscono e amplificano l’infiammazione. Nei polmoni settici, le cellule endoteliali e i macrofagi positivi per FGF13 risultavano fortemente ridotti, suggerendo che le variazioni di questa molecola possano essere correlate al grave danno polmonare.
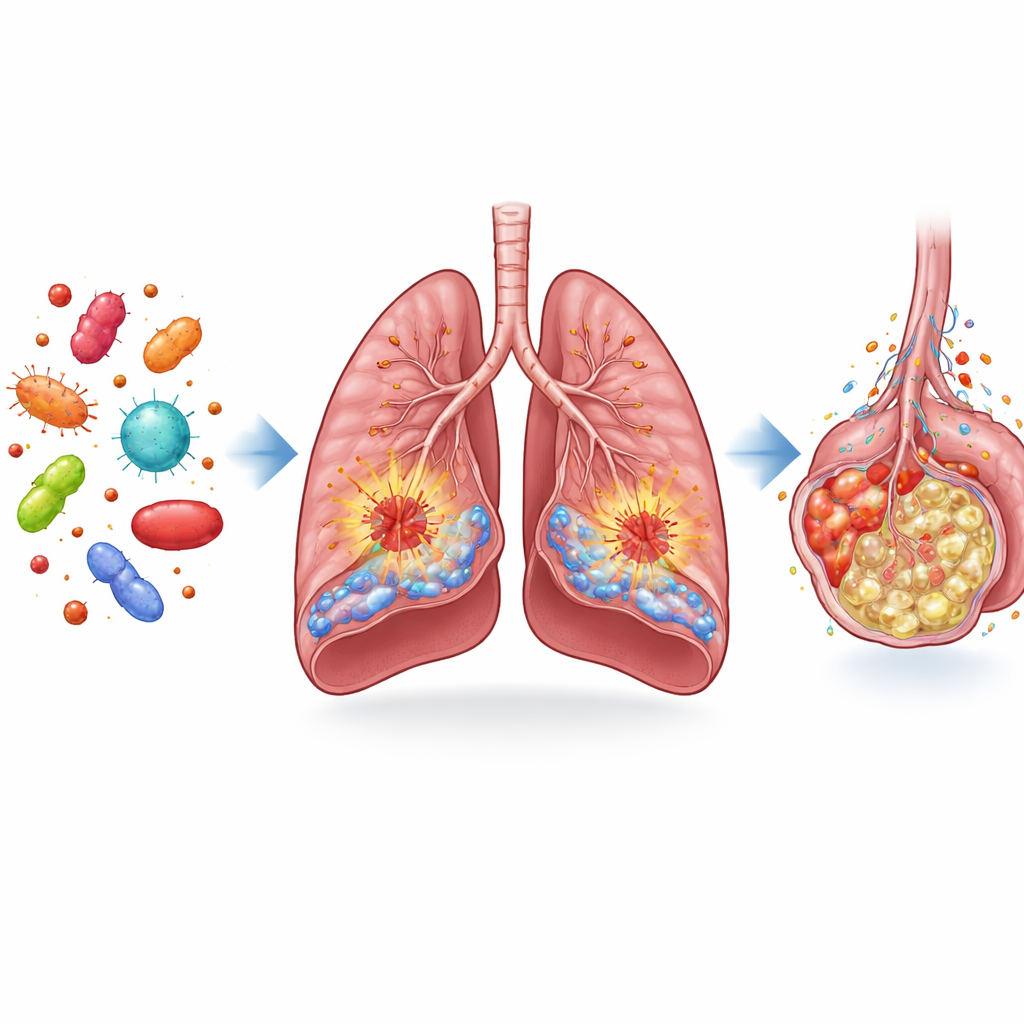
Come FGF13 trasforma i difensori polmonari in promotori di danno
Per verificare cosa faccia realmente FGF13, il gruppo ha usato strumenti genetici nei topi per rimuoverlo da cellule specifiche o indurre in quelle stesse cellule una sovraespressione. Quando FGF13 è stato eliminato solo nelle cellule endoteliali, i topi settici presentavano polmoni con meno perdita di liquidi e gonfiore, meno infiltrazione di cellule immunitarie e una sopravvivenza migliore. L’opposto si è osservato quando le cellule endoteliali sono state ingegnerizzate per sovraprodurre FGF13: edema polmonare, sanguinamento e accumulo di cellule infiammatorie sono peggiorati. Un quadro simile è emerso anche nei macrofagi. I topi privi di FGF13 in queste cellule immunitarie mostravano risposte infiammatorie attenuate e minor danno polmonare, mentre i macrofagi indotti a esprimere FGF13 in eccesso rilasciavano più molecole infiammatorie e aggravavano il danno. In colture cellulari, la riduzione di FGF13 rendeva le cellule vascolari e i macrofagi meno adesivi, meno infiammati e meno tossici per le cellule vicine.
Le cellule infiammate passano a una modalità vorace di zuccheri
Le cellule infiammate, come quelle tumorali, spesso modificano la loro strategia energetica: invece di ossidare lentamente il carburante con l’ossigeno, degradano rapidamente gli zuccheri in un processo chiamato glicolisi aerobica, generando acido lattico. Gli autori hanno scoperto che FGF13 promuove fortemente questo switch. Nei topi settici privi di FGF13 nelle cellule endoteliali o nei macrofagi, i livelli ematici di lattato erano inferiori. In coltura, le cellule con FGF13 ridotto captavano meno glucosio e producevano meno lattato dopo stimolo infiammatorio, mentre le cellule con FGF13 in eccesso mostravano una glicolisi potenziata. Quando i ricercatori bloccarono la glicolisi con un farmaco, l’effetto pro-infiammatorio dell’eccesso di FGF13 risultò in gran parte attenuato, collegando direttamente il ruolo dannoso della molecola a questo programma di combustione degli zuccheri.
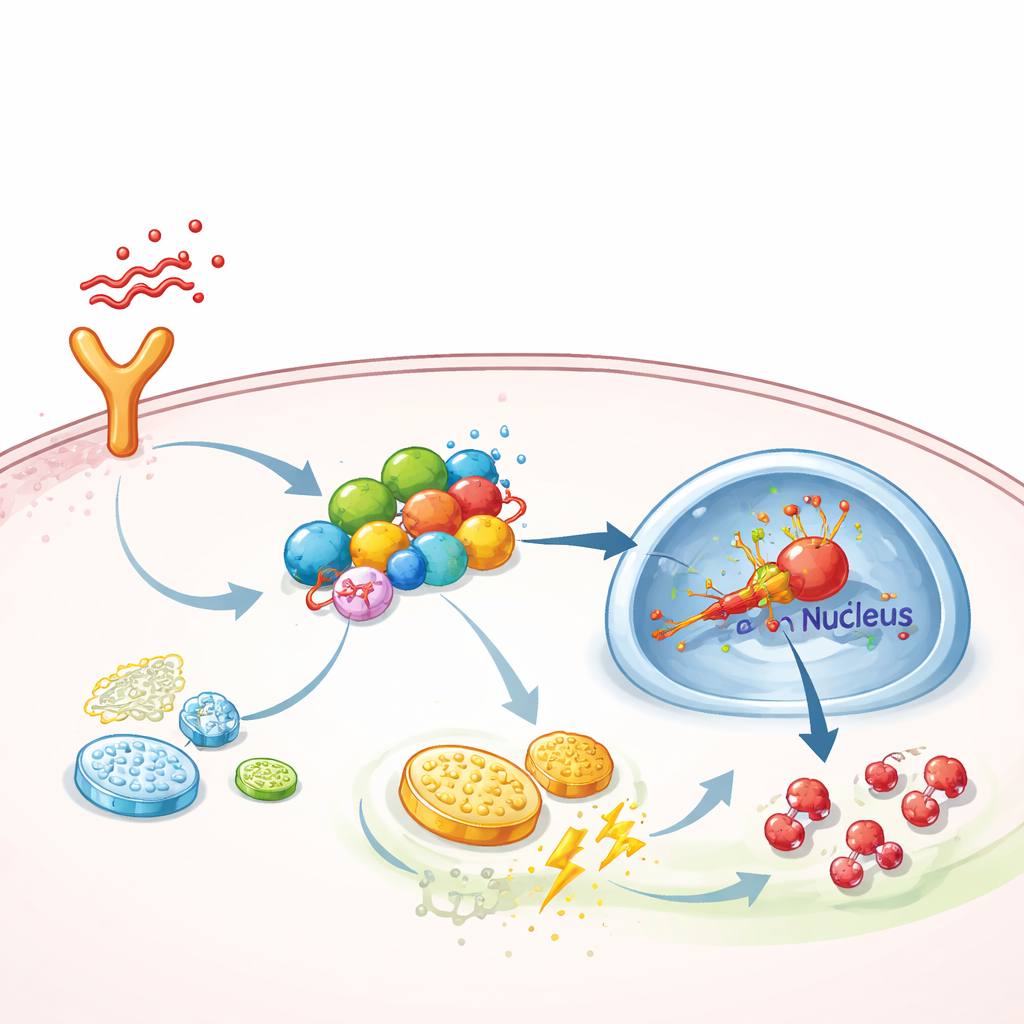
Un’impalcatura molecolare che amplifica la segnalazione infiammatoria
Approfondendo i meccanismi, il team ha indagato come FGF13 spinga le cellule verso questo metabolismo ad alto regime. Hanno scoperto che FGF13 si lega fisicamente a diversi proteine di segnalazione che formano una catena dai recettori di superficie fino al nucleo cellulare—specificamente il percorso TAK1–MEK–ERK, noto per attivare un regolatore principale delle risposte a basso ossigeno chiamato HIF-1α. FGF13 agisce come uno scaffold, mantenendo questi componenti insieme in modo che i segnali viaggino più efficacemente. Quando FGF13 veniva ridotto, l’attivazione di ERK e HIF-1α diminuiva e la glicolisi si affievoliva; quando FGF13 era aumentato, la via diventava iperattiva. La sovraespressione di HIF-1α nei topi annullò il beneficio protettivo dell’eliminazione di FGF13, mentre un inibitore selettivo di ERK, SCH772984, neutralizzò il danno causato dalla sovrapproduzione di FGF13 e migliorò le condizioni polmonari negli animali settici.
Cosa significa per le future terapie della sepsi
Per un lettore non specialista, il messaggio chiave è che il danno polmonare settico non è solo una distruzione casuale dei tessuti; è alimentato da un circuito molecolare specifico all’interno delle cellule endoteliali e dei macrofagi. FGF13 sta al centro di questo circuito, contribuendo ad assemblare un hub di segnalazione che costringe le cellule in uno stato altamente infiammatorio e a consumo di zucchero. Sebbene i livelli di FGF13 diminuiscano durante la sepsi—probabilmente come parte di una risposta allo stress più ampia—questo studio mostra che la proteina residua è comunque un potente promotore di danno. Bloccando i partner di segnalazione di FGF13 o lo spostamento glicolitico che promuove, potrebbe essere possibile ridurre il gonfiore polmonare, la perdita di barriera e l’infiammazione senza paralizzare la capacità dell’organismo di combattere l’infezione. Questo lavoro quindi evidenzia FGF13 e l’asse ERK–HIF‑1α–glicolisi come piste promettenti per sviluppare trattamenti più mirati e sicuri per l’insufficienza polmonare legata alla sepsi.
Citazione: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Parole chiave: danno polmonare settico, FGF13, infiammazione endoteliale, glicolisi aerobica, segnalazione ERK