Clear Sky Science · it
AACRNL passato da fattore di virulenza a parassita epigenetico che guida l’espansione del genoma in eucarioti liberi
Quando vecchie tossine imparano nuovi trucchi
I nostri genomi non sono manuali di istruzioni silenziosi. Sono arene affollate in cui geni, virus e DNA mobile lottano costantemente per spazio e controllo. Questo studio svela un attore sorprendente in quella lotta: una proteina che ha avuto origine come tossina usata dai microbi per attaccare gli ospiti, ma che è stata poi riconvertita all’interno di animali liberi come una specie di “parassita epigenetico” che favorisce l’espansione della propria impronta nel genoma.
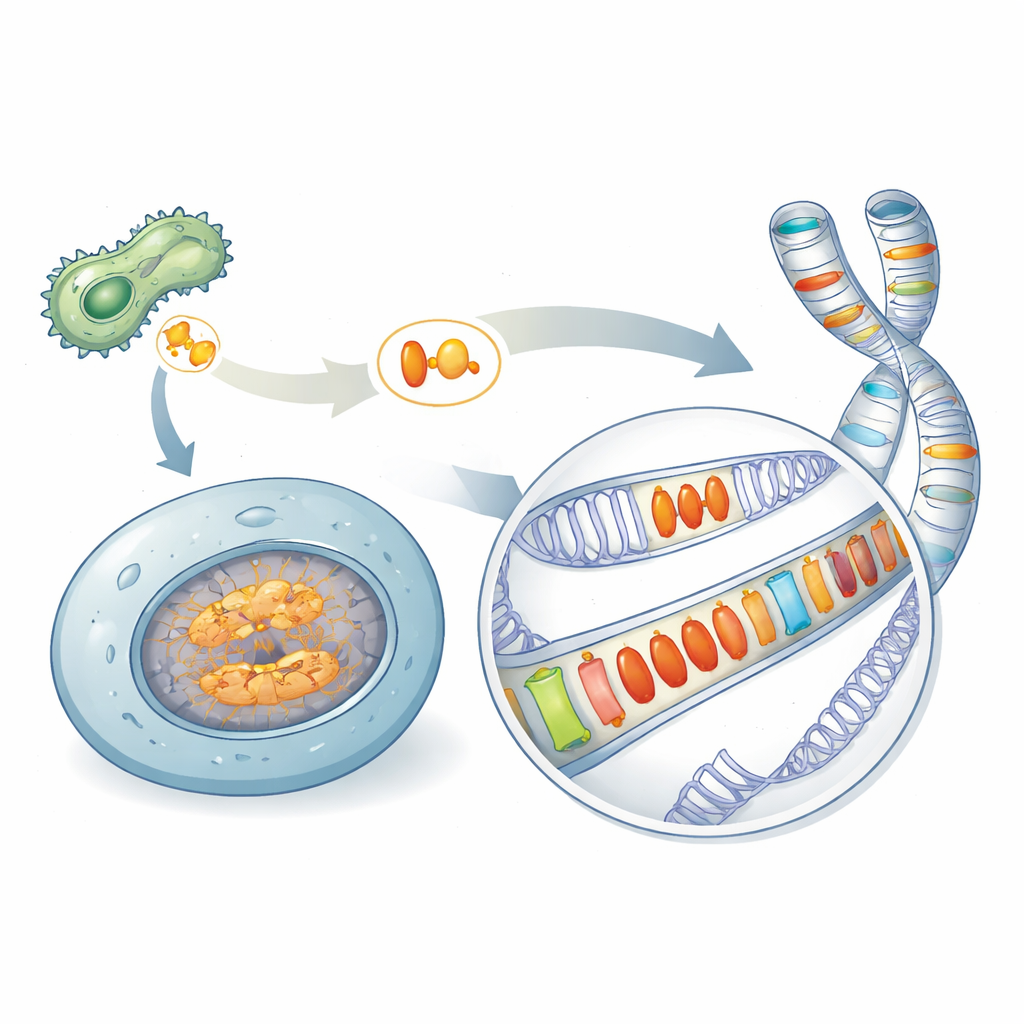
Un’eredità nascosta di armi microbiche
Molti microbi patogeni fanno affidamento su proteine speciali, chiamate effettori, per sabotare le difese degli organismi che infettano. Una famiglia famosa, nota come Crinklers, era ritenuta presente solo nei patogeni. Scansionando una vasta gamma di specie, gli autori hanno scoperto proteine affini — qui raggruppate sotto il nome AACRNL — in luoghi inaspettati, tra cui spugne, coralli, ricci di mare e pesci ossei che non sono patogeni classici. Queste proteine AACRNL conservano il nucleo simile a una tossina che può modificare chimicamente altre proteine, ma la loro porzione anteriore di “consegna”, che i patogeni usano per invadere le cellule ospiti, si è perlopiù disintegrata. Questo cambiamento strutturale suggerisce uno spostamento dall’attaccare altri organismi all’agire all’interno delle stesse cellule dell’ospite.
Un interruttore egoista nel genoma
Nei pesci ossei, i geni AACRNL si trovano in copie multiple sparse su cromosomi differenti. Confrontando tratti di DNA adiacenti, i ricercatori hanno mostrato che alcune linee di AACRNL hanno smesso di copiarsi, mentre altre si sono moltiplicate con l’aiuto di segmenti di DNA mobili vicini chiamati transposoni. Questi transposoni fungono da navette genomiche: quando si muovono o si duplicano, possono trascinare con sé AACRNL. Il risultato è un patchwork di copie ripetute di AACRNL incastonate tra sequenze di transposoni, un marchio di fabbrica di un gene che si diffonde per ottenere vantaggio proprio più che per quello dell’ospite.
Spezzare il tasto muto del genoma
Di norma, le cellule tengono questo DNA mobile sotto rigoroso controllo. Una salvaguardia chiave è un marchio chimico sulle proteine che impacchettano il DNA, noto come H3K27me3, che contribuisce a mantenere spente le regioni pericolose o rumorose. Gli autori hanno trovato che una versione attiva di AACRNL nei pesci, chiamata AACRNLβ, può modificare chimicamente EZH2, l’enzima che deposita questo marchio repressivo. Quando AACRNLβ altera EZH2, la quantità di H3K27me3 al proprio indirizzo genetico e nei transposoni vicini diminuisce, il DNA locale si apre e sia AACRNLβ sia i transposoni adiacenti vengono espressi più intensamente. In pratica, la proteina preme il proprio pulsante di “accensione” e solleva i freni sugli stessi elementi mobili che possono portarla in nuovi punti del genoma.
Eludere i cani da guardia immunitari
Scatenare transposoni e attività genetica insolita rischia di attirare l’attenzione del sistema immunitario. Lo studio mostra che AACRNLβ affronta anche questo problema. Essa aggiunge un piccolo marchio chimico a TRAF6, una proteina centrale che aiuta ad attivare segnali antivirali e infiammatori. Marcato in questo modo, TRAF6 diventa meno stabile ed è sempre più indirizzato allo smaltimento dalla macchina cellulare di riciclo. Con questo hub di segnalazione indebolito, le vie difensive chiave si attivano meno intensamente, creando un ambiente più tollerante in cui AACRNLβ e i transposoni associati possono persistere e copiarsi con minori conseguenze di essere rilevati.
Una delicata corsa agli armamenti dentro la cellula
La storia non finisce con AACRNLβ che corre indisturbata. La stessa proteina TRAF6 presa di mira da AACRNLβ può, a sua volta, aggiungere i propri marchi ad AACRNLβ, contrassegnando la proteina simile a un parassita per la distruzione. Questo scambio somiglia a una corsa agli armamenti molecolare: AACRNLβ usa la chimica derivata dalle tossine per piegare la cromatina e l’immunità a suo vantaggio, mentre le proteine dell’ospite contrastano degradandola e mantenendo la sua attività sporadica e rischiosa. Gli autori sostengono che questa lotta ha permesso a un’antica arma microbica di sopravvivere come un residente egoista nei genomi di organismi liberi, espandendo il contenuto di DNA e rimodellando le regole del conflitto genetico dall’interno.
Perché questo cambia la nostra visione dei genomi
Per un non specialista, il messaggio chiave è che i genomi non sono solo progetti ottimizzati per la sopravvivenza dell’ospite. Contengono anche opportunisti. Questo lavoro dimostra che persino tossine classiche possono essere addomesticate in elementi di questo tipo, usando la loro chimica distruttiva originale per eludere serrature epigenetiche e allarmi immunitari, e per diffondersi nel genoma nel corso dell’evoluzione. Capire questo tipo di conflitto nascosto aiuta a spiegare perché i genomi sono così grandi, complessi e dinamici — e suggerisce che altre tossine “in pensione” potrebbero silenziosamente riscrivere il DNA in molte specie, forse anche nella nostra.
Citazione: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Parole chiave: elementi genetici egoisti, evoluzione del genoma, regolazione epigenetica, transposoni, immunità innata