Clear Sky Science · it
Immobilizzazione sinergica multicomponente tramite strategie di scambio dinamico e in situ per la costruzione di biofarmaci gerarchici
Perché è importante costruire farmaci più intelligenti
Molti dei farmaci più potenti oggi sono grandi e fragili molecole biologiche come proteine ed enzimi. Possono combattere il cancro, uccidere batteri dannosi e accelerare la guarigione, ma sono facilmente danneggiabili e difficili da consegnare nel punto giusto del corpo. Questo articolo descrive un nuovo modo di “imballare” diversi di questi componenti delicati insieme all’interno di un materiale protettivo simile a una spugna, così che possano agire in sequenza con maggiore efficacia e meno effetti collaterali.
Trasformare un cristallo in un condominio molecolare
I ricercatori partono da un materiale poroso speciale composto da ioni metallici e piccoli blocchi organici. Si comporta un po’ come un minuscolo condominio flessibile pieno di stanze e corridoi. Dimostrano che questo impalcamento, chiamato zeolitic pyrimidine framework, può crescere attorno alle proteine in modo che queste risultino protette all’interno del cristallo. Questo intrappolamento «in situ» non schiaccia né inattiva le proteine, e immagini accurate confermano che sono distribuite uniformemente all’interno, proprio come inquilini che occupano tutti i piani di un edificio.
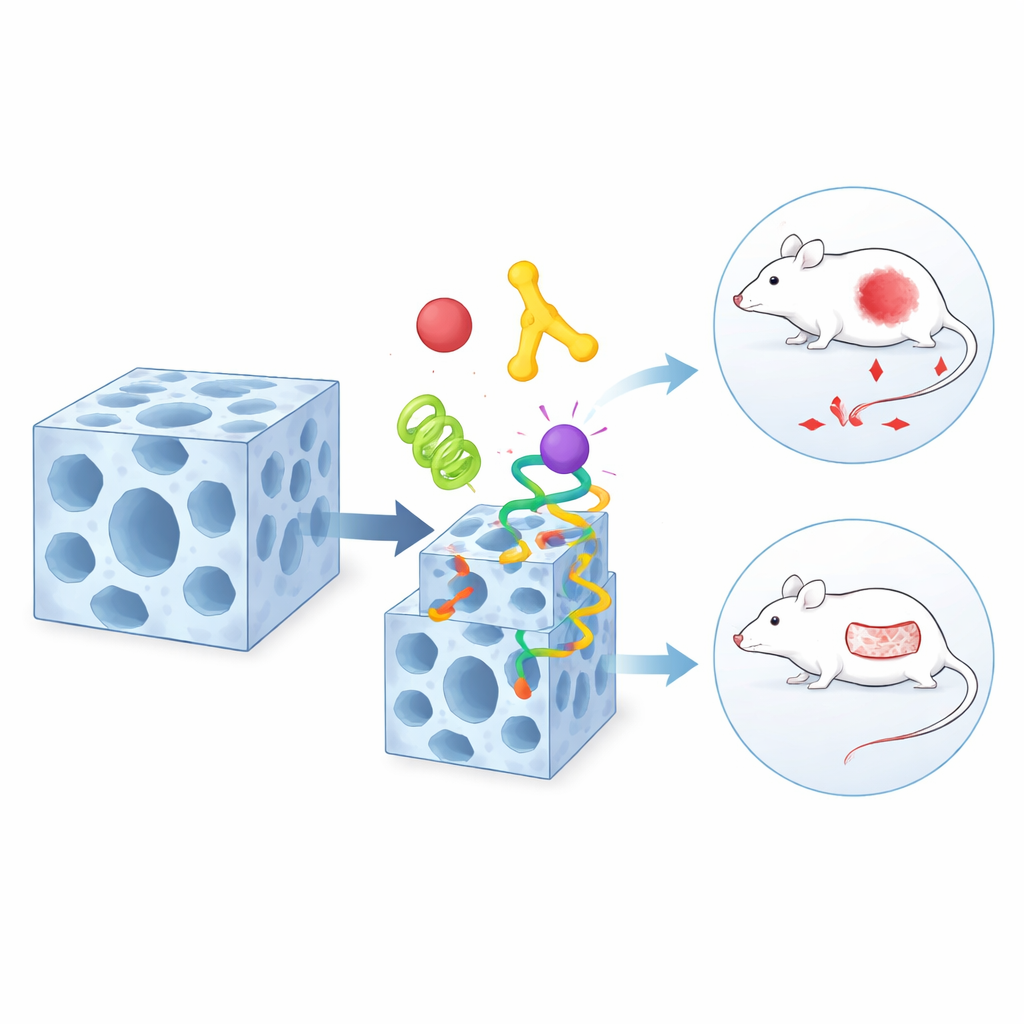
Un ospite che cambia forma per decorare la superficie
Lo stesso materiale ha un sorprendente secondo trucco: può modificare reversibilmente la sua struttura interna quando viene esposto a certi solventi o all’acqua. Durante questo delicato cambiamento di forma, alcune delle connessioni chimiche nell’impalcatura si allentano e poi si riformano. Il team ha scoperto che particolari gruppi chimici presenti sulla superficie delle proteine — come quelli di alcuni amminoacidi — possono sfruttare questo momento di debolezza. Competono temporaneamente con i blocchi costituenti originali del framework e si inseriscono in nuovi «difetti» formatisi vicino alla superficie. Di conseguenza, uno strato di proteine si ancora principalmente all’esterno del cristallo, mentre quelle interne rimangono al loro posto. Questo processo di scambio dinamico permette agli scienziati di decidere quali componenti abitano in profondità e quali decorano la scorza esterna.
Progettare catene di montaggio enzimatiche
Con il controllo sia degli spazi interni sia di quelli esterni, gli autori costruiscono piccole «catene di montaggio» enzimatiche. In un esempio, un enzima che trasforma lo zucchero in un sottoprodotto dannoso è intrappolato all’interno del framework, mentre un secondo enzima che degrada in modo sicuro quel sottoprodotto è fissato vicino alla superficie. Questo arrangiamento interno–esterno rende la reazione più rapida ed efficiente rispetto a progettazioni core–shell più tradizionali o a miscele casuali di enzimi. Poiché gli enzimi esterni sono più facilmente raggiungibili dalle molecole, e l’intermedio dannoso viene rimosso rapidamente, il sistema rimane attivo per molti cicli e tollera meglio calore, condizioni severe e usi ripetuti.
Confezioni intelligenti anticancro e antibatteriche
La vera potenza di questo approccio emerge quando viene applicato alla medicina. Il team combina in una singola particella stratificata una proteina che riconosce i tumori, un enzima che consuma glucosio e un farmaco chemioterapico classico. Il componente di targeting sulla superficie guida la particella verso le cellule tumorali, l’enzima prosciuga il loro apporto energetico consumando lo zucchero locale, e il farmaco a piccole molecole infligge un ulteriore colpo letale. In topi con impianti tumorali umani, questo pacchetto tripartito riduce i tumori molto più efficacemente di ciascuno dei componenti da solo o di miscele disposte in modo più semplice. In un progetto separato, gli autori adattano il framework per ferite cutanee infette collocando un peptide antibatterico e un enzima rimodellante dei tessuti in regioni diverse dello stesso vettore. In modelli su ratto, queste particelle riducono nettamente l’infezione e accelerano la chiusura di ferite difficili rispetto ai trattamenti convenzionali.

Come questo lavoro fa progredire la medicina
Per un non specialista, il messaggio chiave è che questo studio trasforma un singolo cristallo poroso in una casa programmabile per molti tipi di molecole terapeutiche. Decidendo chi vive all’interno, chi risiede sulla superficie e in quale proporzione, i ricercatori possono orchestrare trattamenti a tappe — prima il targeting, poi l’attacco, poi la riparazione — all’interno di un unico oggetto minuscolo. Questa strategia non solo protegge farmaci biologici fragili, ma permette anche che essi si aiutino a vicenda, portando a terapie anticancro e antibatteriche più potenti e più precise. Gli stessi principi di progettazione potrebbero essere adattati a molti futuri «farmaci intelligenti» che richiedono più componenti che lavorino insieme nel posto giusto al momento giusto.
Citazione: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Parole chiave: framework metallorganici, immobilizzazione di enzimi, nanomedicina oncologica, guarigione delle ferite, consegna di biofarmaci