Clear Sky Science · it
La matrice extracellulare media il raggruppamento delle cellule tumorali circolanti nella metastasi del carcinoma mammario triple-negative
Come le cellule del cancro al seno si coalizzano nel flusso sanguigno
Quando il cancro al seno si diffonde, spesso ciò avviene perché cellule tumorali isolate si introducono nel flusso sanguigno e impiantano tumori in organi distanti. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: come fanno le cellule di carcinoma mammario più aggressive, che hanno perso il loro “velcro” abituale per aderire le une alle altre, a viaggiare comunque in stretti ammassi — e perché questo le rende così letali?
Un rivestimento zuccherino appiccicoso che sostituisce la colla cellulare classica
Gli autori si concentrano sul carcinoma mammario triple-negative (TNBC), una forma particolarmente aggressiva che spesso rilascia nel sangue cellule tumorali circolanti (CTC). In molti tumori, gli ammassi di CTC sono molto più propensi a dare metastasi rispetto alle cellule isolate. Tipicamente, tali ammassi sono tenuti insieme da giunzioni aderenti epiteliali — complessi proteici specializzati che fungono da rivetti molecolari tra cellule vicine. Ma le cellule TNBC perdono frequentemente queste proteine di giunzione, sollevando un paradosso: senza la colla abituale, che cosa mantiene integri i loro ammassi? Analizzando grandi database genici sul cancro, i ricercatori hanno scoperto che i tumori TNBC sono arricchiti di geni coinvolti nella struttura esterna della cellula, nota come matrice extracellulare. Un gene rilevante, HAS2, codifica un enzima che produce ialuronano (HA), un lungo polimero zuccherino che riveste le cellule. Livelli elevati di HAS2 e di HA sono stati fortemente associati a caratteristiche tumorali aggressive e metastatiche.
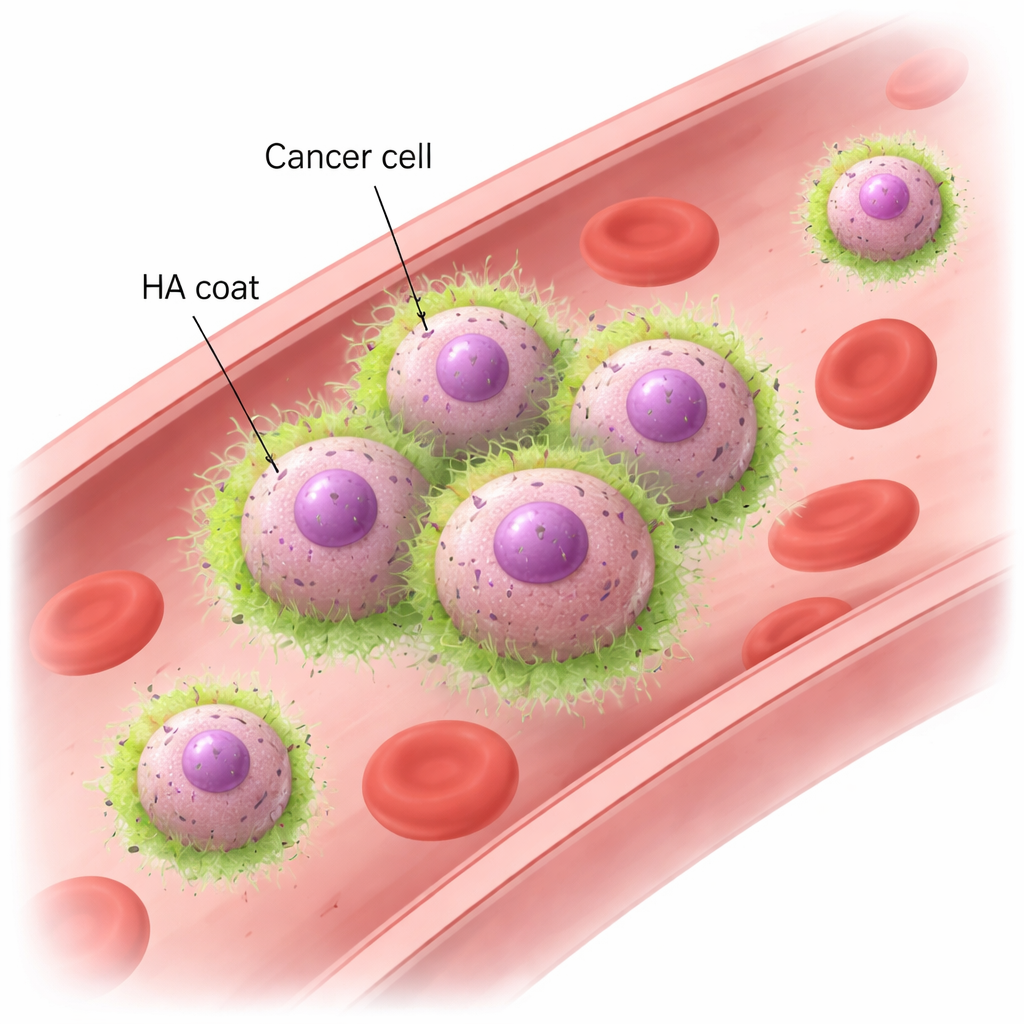
Ialuronano e CD44: un nuovo modo per le cellule di “darsi la mano”
Utilizzando modelli murini e linee cellulari di carcinoma mammario umano, il gruppo ha mostrato che le cellule TNBC metastatiche formano rapidamente ammassi quando sono esposte a un fluido vorticoso che imita il flusso sanguigno. Questi ammassi rimangono integri anche sotto forze simili a quelle dei vasi reali, mentre le cellule di tumori meno aggressive si sfasciano e deragliano come singole. La microscopia ha rivelato che le cellule metastatiche sono avvolte da un “mantello” di HA, che si concentra esattamente dove le cellule si toccano. Rimuovere l’HA con enzimi, o ridurre l’espressione di HAS2, ha fatto perdere alle cellule la capacità di raggrupparsi sotto flusso, anche se potevano comunque sedimentare insieme se lasciate indisturbate. Il partner chiave sulla superficie cellulare è CD44, un recettore comune che lega l’HA. Le cellule prive di CD44 non riuscivano più a mantenere l’HA sulla loro superficie né a formare ammassi. Al contrario, cellule che normalmente non raggruppano, ma ingegnerizzate per esprimere sia HAS2 sia CD44, hanno acquisito una robusta capacità di aggregazione. Questi esperimenti dimostrano che l’interazione HA–CD44 è sia necessaria sia sufficiente per far aderire cellule tumorali nel flusso sanguigno veloce.
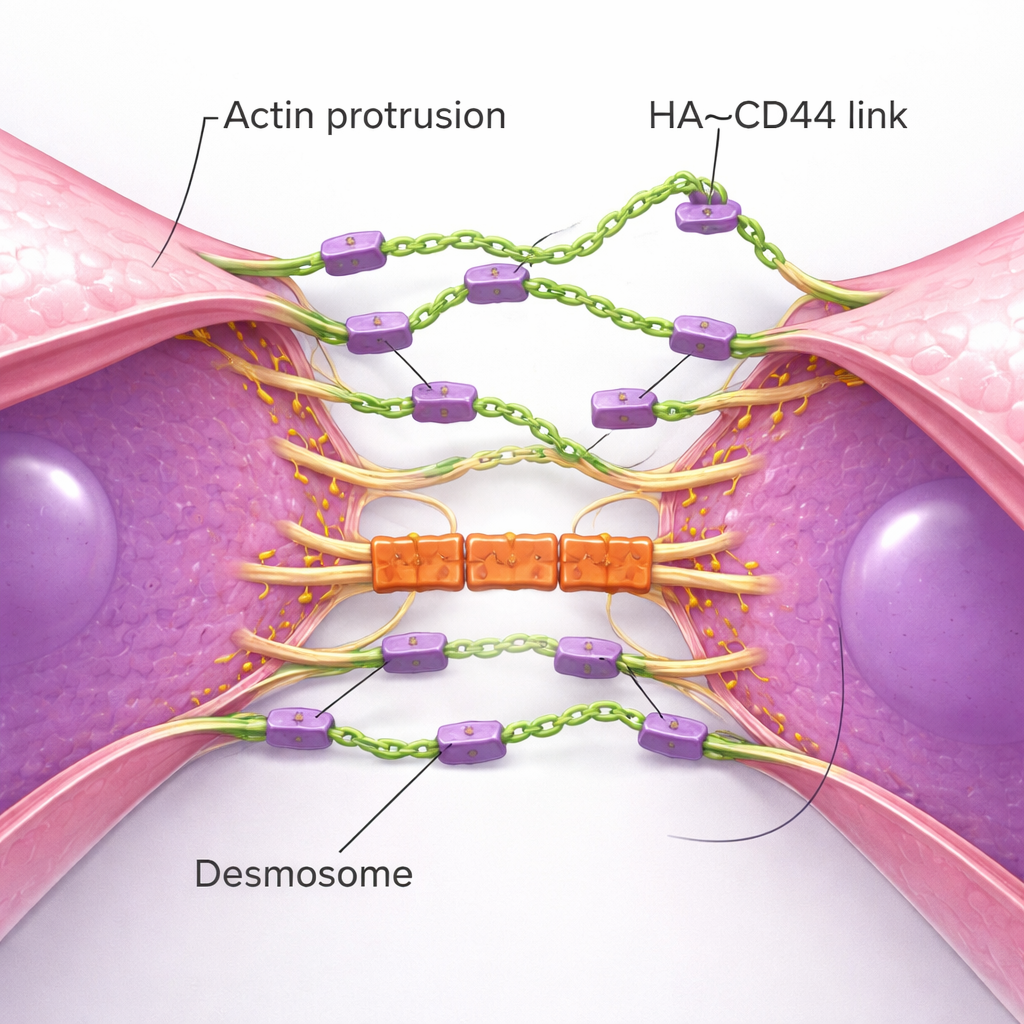
Minuscole protrusioni e serrature meccaniche costruiscono ammassi solidi
Immagini ad alta risoluzione hanno svelato la coreografia fisica di come si formano gli ammassi. Le singole cellule TNBC estendono numerose sottili protrusioni di membrana basate su actina — come tentacoli — punteggiate di CD44 e rivestite di HA. Quando due cellule si avvicinano, questi tentacoli si incontrano per primi, formando ponti iniziali HA–CD44. Col tempo, le protrusioni scorrono una accanto all’altra, avvicinando i corpi cellulari fino a posizionare ampie aree di membrana quasi fianco a fianco. Questo processo richiama la formazione delle giunzioni aderenti nelle cellule epiteliali normali, ma qui è guidato da un rivestimento zuccherino flessibile invece che da catene proteiche rigide. Man mano che la zona di contatto matura, entra in gioco un secondo insieme di strutture: i desmosomi, giunzioni robuste che collegano le membrane cellulari allo scheletro interno. Le proteine desmosomiali si accumulano solo dopo l’instaurarsi del contatto mediato dall’HA e fungono da “serrature” meccaniche che aiutano gli ammassi a resistere alle forze laceranti del flusso sanguigno. Quando i componenti dei desmosomi erano ridotti, gli ammassi si formavano ma si rompevano a livelli di taglio più elevati.
Perché il raggruppamento conta per la sopravvivenza e le metastasi
Il sistema di aggregazione basato su HA si è rivelato qualcosa di più di un semplice modo per restare insieme: migliorava direttamente la sopravvivenza. In condizioni prolungate di flusso sanguigno simulato, gli ammassi ricchi di HA mostravano livelli molto più bassi di specie reattive dell’ossigeno dannose e molta meno morte cellulare rispetto alle singole cellule deprivate di HA. Nei modelli murini, le cellule TNBC prive di HAS2 producevano molte meno CTC, formavano solo piccoli ammassi e generavano drasticamente meno metastasi polmonari — nonostante i loro tumori primari crescessero altrettanto bene. Quando ammassi preformati di cellule di controllo e prive di HAS2 venivano iniettati nei topi, le cellule povere di HA erano molto meno propense a colonizzare con successo i polmoni. Inoltre, le CTC rivestite di HA potevano “reclutare” altre cellule — sia cellule tumorali prive di HA sia cellule immunitarie normali come i neutrofili — in ammassi misti, a patto che questi partner esprimessero CD44. Campioni di sangue di pazienti donne con TNBC metastatico mostravano lo stesso schema: le CTC spesso portavano un mantello di HA, con l’HA arricchita nei punti di contatto tra cellule tumorali e tra cellule tumorali e non tumorali.
Cosa significa per i pazienti e le terapie future
Per un non specialista, la conclusione principale è che alcune delle cellule del cancro al seno più letali non viaggiano da sole ma come minuscole squadre cooperative tenute insieme da un rivestimento esterno zuccherino e dal suo recettore, piuttosto che dai classici “rivetti” cellula–cellula presenti nei tessuti normali. Questo meccanismo HA–CD44 aiuta le cellule tumorali a sopravvivere al flusso sanguigno ostile, a unirsi tra loro e con cellule sanguigne di supporto, e a impiantare nuovi tumori in organi distanti in modo più efficiente. Mirare alla produzione di HA (per esempio inibendo HAS2) o bloccarne l’interazione con CD44 potrebbe, in teoria, indebolire questi ammassi e rendere più difficile la metastasi del TNBC, offrendo una nuova prospettiva per futuri trattamenti anti-metastatici.
Citazione: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Parole chiave: carcinoma mammario triple-negative, cellule tumorali circolanti, ialuronano, CD44, metastasi