Clear Sky Science · it
Escherichia coli favorisce le metastasi del tumore colorettale mantenendo i loop enhancers-promotori tramite il rilascio di trappole extracellulari dei neutrofili
Microrganismi intestinali e l’autostrada segreta del cancro
Il carcinoma colorettale spesso uccide non per il tumore originario nell’intestino, ma perché le cellule tumorali migrano al fegato e lì si insediano. Questo studio svela un complice inatteso in quel viaggio: un comune batterio intestinale, Escherichia coli. Seguendo la catena di eventi dal batterio nell’intestino ai tumori aggressivi nel fegato, i ricercatori mostrano come microbi, cellule immunitarie e l’architettura del DNA all’interno delle cellule tumorali possano cooperare per alimentare le metastasi — e suggeriscono nuovi modi per interrompere questa catena.
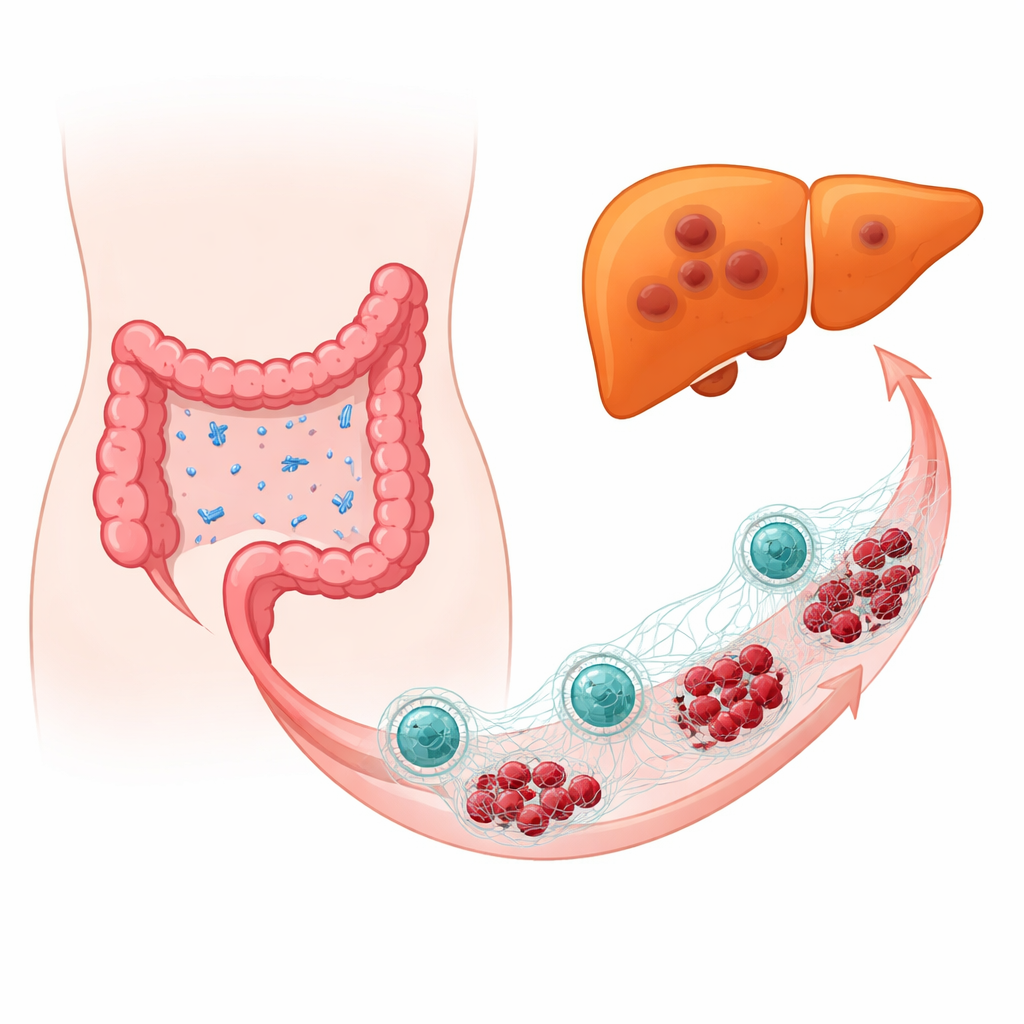
Quando batteri “amici” diventano ostili
Il gruppo ha analizzato campioni tumorali di persone con carcinoma colorettale, confrontando chi aveva sviluppato metastasi epatiche con chi non le aveva. Utilizzando profilazione microbica ad alta risoluzione basata sul DNA, hanno trovato che E. coli era molto più abbondante nei tumori che avevano già colonizzato il fegato. In modelli murini e in topi con sistema immunitario umanizzato, l’introduzione deliberata di E. coli in prossimità dei tumori colorettali ha reso le metastasi epatiche più grandi e più frequenti e ha spinto le cellule tumorali verso uno stato più mobile e invasivo. Anche quando la maggior parte della flora intestinale normale è stata rimossa con antibiotici e solo E. coli è stato reintrodotto, il batterio ha comunque aumentato crescita e diffusione tumorale, indicando il ruolo di E. coli in sé piuttosto che un mero squilibrio generale del microbioma.
Reti immunitarie che aiutano il cancro a fuggire
I neutrofili — cellule immunitarie di prima linea che normalmente intrappolano e uccidono i microbi — sono emersi come intermediari cruciali. In risposta a E. coli, i neutrofili hanno rilasciato strutture filamentose chiamate trappole extracellulari, composte da DNA e proteine tossiche. Queste reti sono pensate per catturare i batteri, ma in questo contesto hanno protetto e potenziato involontariamente le cellule tumorali. Quando i ricercatori hanno degradato le trappole con enzimi o bloccato enzimi chiave necessari alla loro formazione, le metastasi epatiche si sono ridotte e i tumori sono diventati meno aggressivi. L’eliminazione dei neutrofili ha avuto un effetto protettivo simile, evidenziando un paradosso: la stessa risposta immunitaria che combatte l’infezione viene dirottata per favorire la diffusione del cancro.
Dai segnali elettrici agli interruttori genici
Come possono reti adesive di DNA esterne a una cellula tumorale cambiare ciò che avviene nel suo nucleo? La risposta è risultata nel calcio, un semplice ione che funge da segnale elettrico nelle cellule. Lo studio ha dimostrato che le trappole neutrofiliche aumentavano il livello sulla superficie delle cellule tumorali colorettali di una proteina-canale, TRPC1. TRPC1 ha permesso un afflusso maggiore di calcio nella cellula, che a sua volta ha attivato un regolatore sensibile al calcio chiamato NFATC3 e ha creato un circuito autorinforzante che manteneva elevati i livelli di TRPC1. Questa impennata di calcio favoriva l’associazione di due piccole proteine, S100A8 e S100A9, che poi si legavano a una proteina di controllo della crescita di grande rilievo, STAT3. Il complesso si spostava nel nucleo dove compiva qualcosa di particolarmente rilevante: contribuiva a piegare e far interagire il DNA affinché regioni regolatorie distanti e siti di iniziatore genico venissero a contatto, stabilizzando fisicamente i “loop enhancer–promotore” che aumentano l’espressione di certi geni.
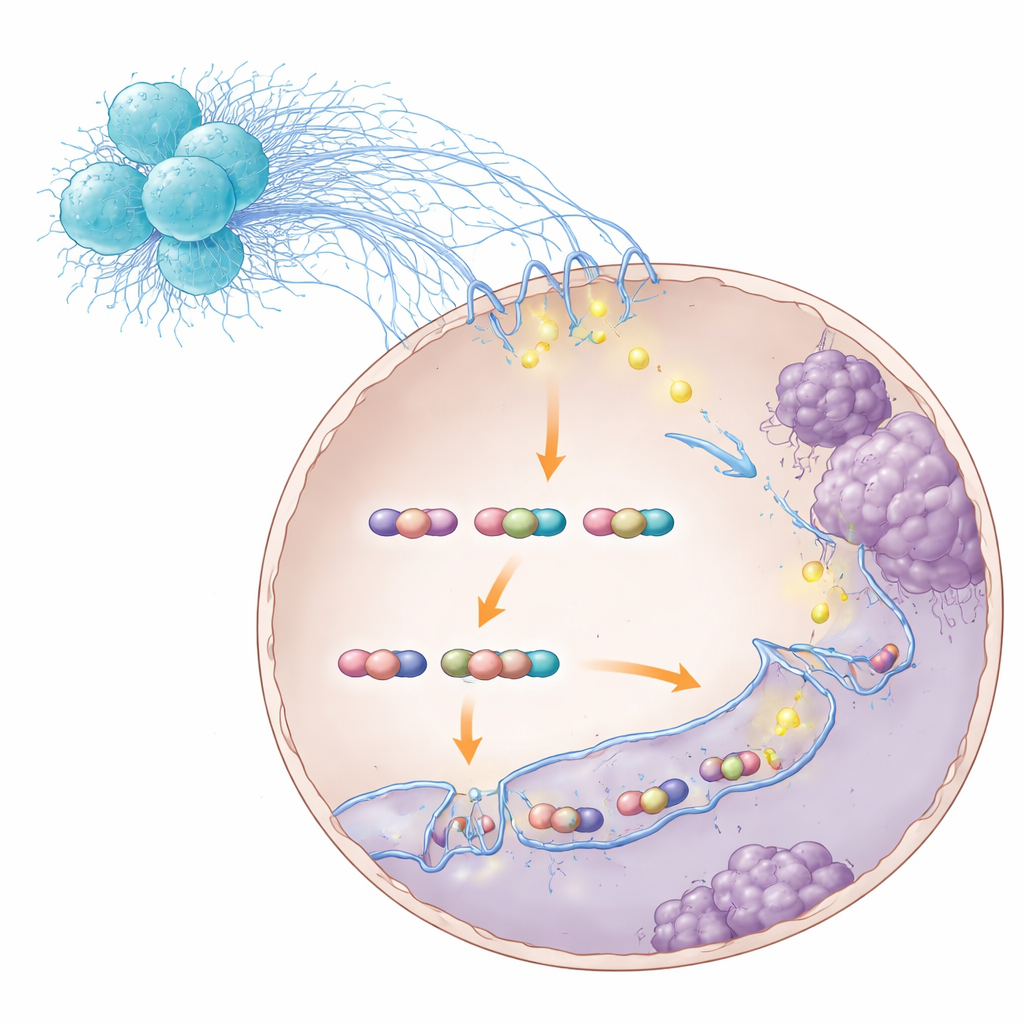
Riprogrammare le cellule tumorali per le metastasi
Mappando i contatti tridimensionali lungo il genoma, i ricercatori hanno scoperto che il complesso STAT3–S100A8/9 promuoveva loop che favorivano geni coinvolti nel movimento e nell’invasione cellulare. Un gene particolarmente importante è risultato essere TNS1, che spinge le cellule ad allentare gli attacchi e a migrare più facilmente. Quando il complesso STAT3–S100A8/9 è stato perturbato, molti di questi loop si sono indeboliti o sono scomparsi, i livelli di TNS1 sono diminuiti e le cellule tumorali hanno perso parte della loro capacità di invadere e colonizzare il fegato. È significativo che questa perturbazione non abbia impedito del tutto l’interazione di STAT3 con il DNA — ha specificamente destabilizzato l’architettura dei loop che potenziava i programmi metastatici. In modelli animali, bloccare passaggi diversi di questa catena — dal sensore batterico RIPK2 nei neutrofili, a S100A8/9, fino a STAT3 stesso — ha ridotto le metastasi epatiche e migliorato la sopravvivenza.
Spezzare la catena tra microbi e tumori
Per i non specialisti, il messaggio chiave è che un comune batterio intestinale può favorire la diffusione del carcinoma colorettale provocando prima le cellule immunitarie a lanciare reti di DNA, e poi usando quelle reti per innescare una catena a base di calcio che riorganizza il modo in cui i geni tumorali vengono attivati. Piuttosto che affidarsi ad antibiotici di largo spettro, che possono danneggiare microbi benefici e attenuare l’immunoterapia anticancro, il lavoro indica bersagli farmacologici più precisi: sensori batterici come RIPK2, la cascata TRPC1–calcio–S100A8/9 e i loop di DNA guidati da STAT3 che mantengono i geni metastatici iperattivi. Interrompere questa catena in uno o più punti potrebbe offrire una nuova strategia per impedire che il carcinoma colorettale evolva da problema locale nell’intestino a malattia mortale nel fegato.
Citazione: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Parole chiave: metastasi del cancro colorettale, microbioma intestinale, trappole extracellulari dei neutrofili, segnalazione STAT3, regolazione epigenetica dei geni