Clear Sky Science · it
La progettazione di inibitori covalenti conferisce attività contro le forme legate a GDP e GTP di KRAS G12C
Perché questo conta per i futuri trattamenti contro il cancro
I tumori guidati da mutazioni in un gene chiamato KRAS sono stati a lungo considerati tra i più difficili da trattare. Recentemente, nuovi farmaci che bloccano una forma mutante comune, KRAS G12C, sono arrivati ai pazienti e hanno cominciato a cambiare questo scenario. Questo articolo esplora un’idea ancora più ambiziosa: possiamo progettare farmaci che blocchino KRAS G12C in entrambe le sue principali modalità operative all’interno della cellula, e questo renderebbe il trattamento del cancro più rapido, più efficace o più duraturo?
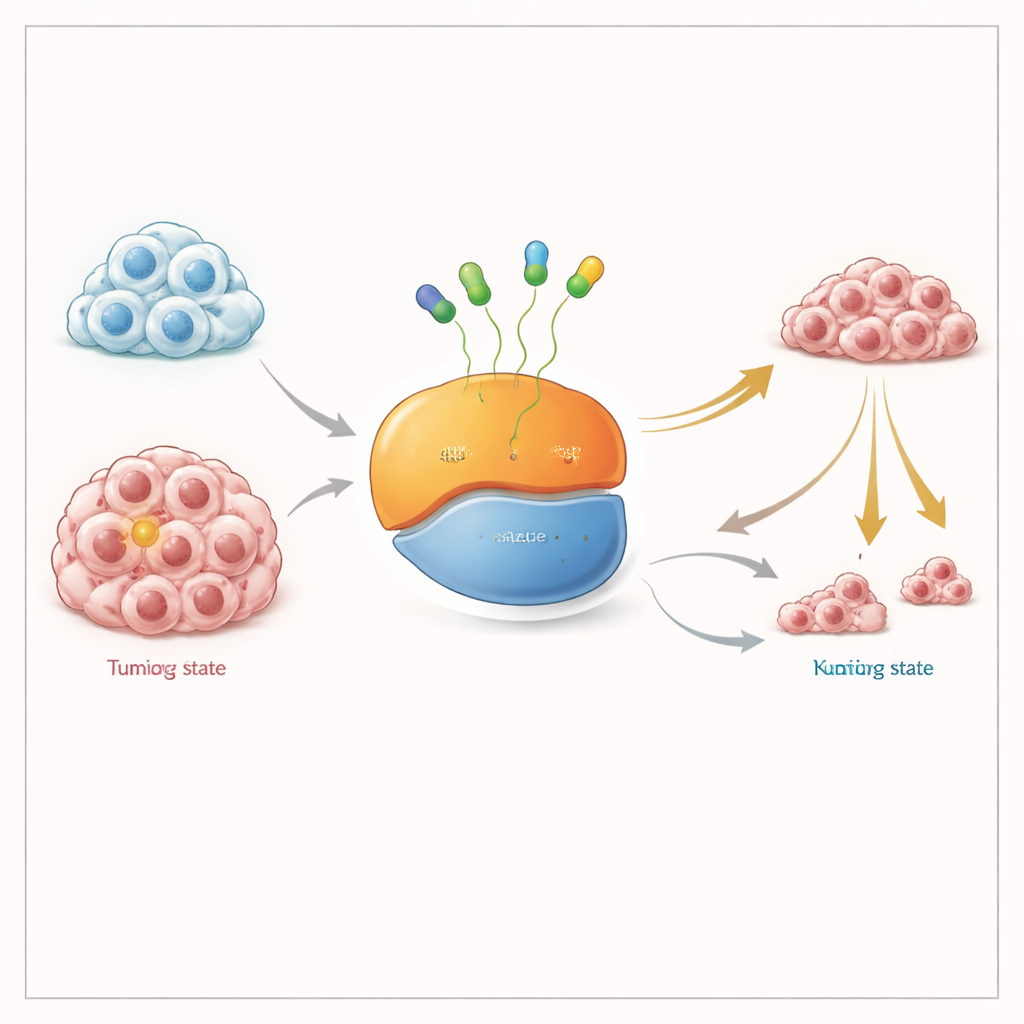
Spegnere un interruttore molecolare in due posizioni
KRAS funziona come un piccolo interruttore acceso–spento per i segnali di crescita cellulare. Alterna uno stato “spento”, in cui è legato a una molecola energetica (GDP), e uno stato “acceso”, in cui è legato a un’altra (GTP). La mutazione KRAS G12C mantiene parzialmente questo interruttore in posizione accesa e alimenta la crescita tumorale. I farmaci approvati dalla FDA si attaccano alla forma “spenta” e la bloccano; col tempo, man mano che più molecole KRAS passano attraverso quello stato, l’intero pool di proteina mutante viene disattivato. Molti scienziati hanno ipotizzato che un farmaco in grado di legare KRAS in entrambe le forme, accesa e spenta, dovrebbe funzionare meglio, specialmente nei tumori che si adattano mantenendo più KRAS nello stato attivo.
Progettare un nuovo tipo di uncino molecolare
Gli autori si sono posti l’obiettivo di costruire farmaci a duplice funzione. Si sono concentrati su una piccola cavità vicino a una regione flessibile di KRAS chiamata Switch II, dove già si legano i farmaci correnti. Invece di modificare quanto saldamente le loro molecole si inserissero in quella cavità, hanno re-ingegnerizzato la porzione “warhead” che forma un legame chimico permanente alla cisteina mutante in posizione 12. Attraverso modellizzazione al computer e la sintesi di dozzine di varianti, hanno scoperto un warhead speciale in tre parti che si avvicina alla cisteina con un angolo leggermente diverso. Questo spostamento sottile crea abbastanza spazio per la più ingombrante molecola di GTP, permettendo ai nuovi composti di legarsi a KRAS sia quando porta GDP sia quando porta GTP. Test biochimici hanno confermato che i composti principali possono disturbare l’interazione di KRAS con un partner di segnalazione chiave, RAF, in entrambi gli stati.
Vedere come la proteina si rimodella
Per capire perché queste molecole funzionassero, il team ha determinato strutture cristalline ad alta risoluzione del farmaco legato a KRAS. Questi istantanei hanno mostrato che il nuovo warhead reagisce in un sito insolito sullo scaffold chimico, facendo staccare un atomo di fluoro e formando un legame covalente a un carbonio diverso rispetto ai tipici farmaci oncologici che prendono di mira le cisteine. Questa chimica alterata aiuta il farmaco a adattarsi nella tasca di Switch II anche quando è presente GTP. Le strutture hanno anche rivelato che quando l’inibitore si lega, sposta una piccola molecola d’acqua e riorganizza sottilmente un altro loop, Switch I, che normalmente entra in contatto con le proteine di segnalazione a valle. Questo rimodellamento allosterico avvicina due amminoacidi a formare un ponte salino stretto, deformando la superficie in modo che RAF non possa più agganciarsi e trasmettere i segnali di crescita.
Spegnimento rapido, ma nessun effetto a lungo termine più forte
Muniti di queste intuizioni strutturali, i ricercatori hanno perfezionato due molecole lead che si legano in modo efficiente e selettivo a KRAS G12C, risparmiando in gran parte altre proteine contenenti cisteine. In linee cellulari tumorali, questi inibitori a doppio stato hanno bloccato rapidamente una importante catena di segnalazione nota come via MAPK, misurata dalla perdita di un marcatore chimico sulla proteina ERK e da una forte soppressione della crescita cellulare. Hanno inattivato KRAS nelle cellule più rapidamente rispetto a un farmaco di riferimento che prende di mira solo lo stato inattivo. In modelli murini di tumore, un composto lead ha mostrato buona biodisponibilità orale, ha rapidamente formato legami covalenti con il bersaglio e ha ridotto i tumori o ne ha rallentato la crescita. Tuttavia, quando il team ha confrontato i farmaci a doppio stato e quelli che colpiscono lo stato inattivo su tempi più lunghi, entrambe le classi hanno finito per raggiungere livelli simili di spegnimento di KRAS, inibizione della via e controllo del tumore.
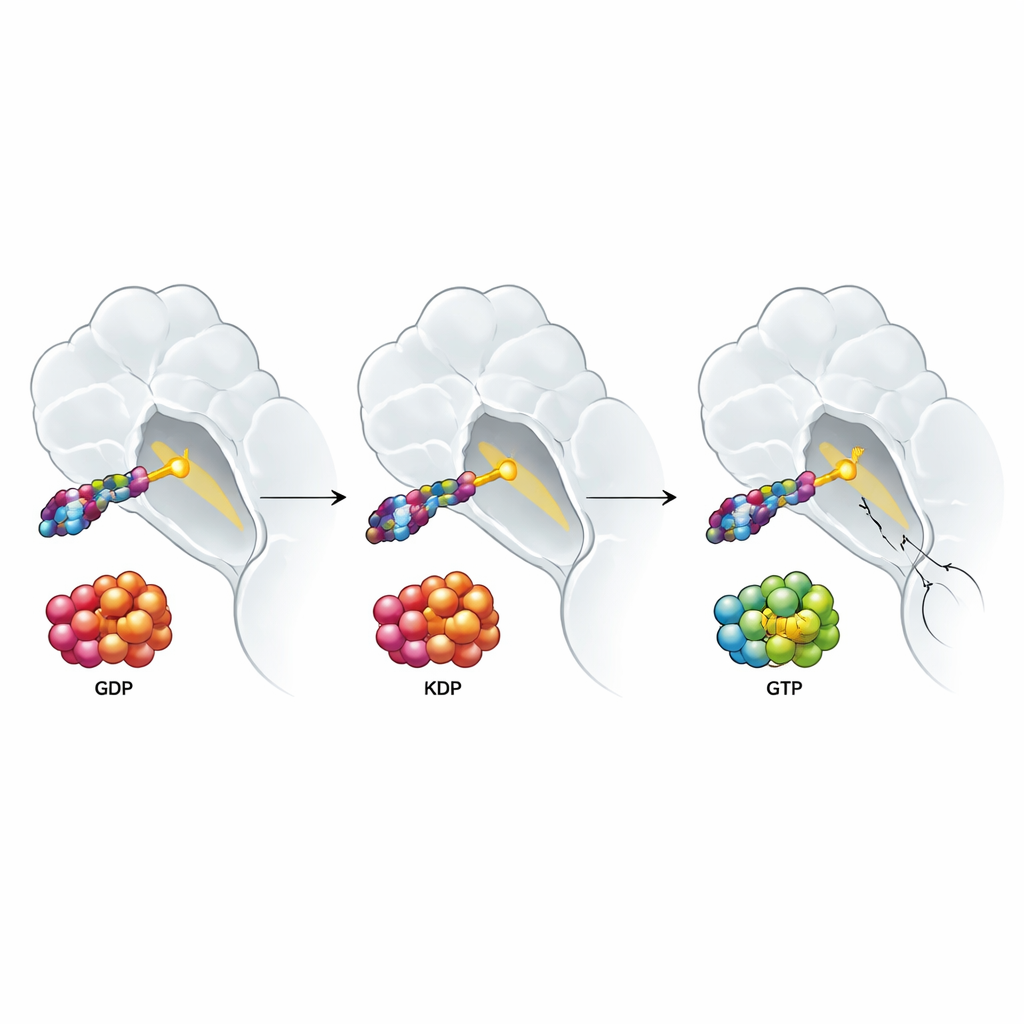
Perché i segnali di crescita dall’ambiente tumorale prevalgono ancora
Lo studio ha anche indagato come i segnali provenienti dall’ambiente del tumore influenzino questi farmaci. Fattori di crescita come EGF e HGF, abbondanti intorno a molti tumori, spingono le proteine RAS verso la forma attiva caricata di GTP e sono noti per attenuare le risposte alle terapie mirate. Si potrebbe pensare che un farmaco che si lega alla forma attiva di KRAS G12C eviti questo problema. Invece, gli autori hanno scoperto che sia gli inibitori a doppio stato sia quelli dello stato inattivo perdono potenza quando tali fattori di crescita sono presenti. Esperimenti dettagliati hanno indicato un colpevole sorprendente: l’attivazione delle forme normali e non mutate di RAS (H‑RAS e N‑RAS), che possono bypassare KRAS G12C e mantenere il flusso dei segnali di crescita. Quando i ricercatori hanno eliminato H‑RAS e N‑RAS in una linea cellulare di cancro polmonare, la resistenza indotta dai fattori di crescita è in larga parte scomparsa per tutti i tipi di farmaci che prendono di mira KRAS G12C, mentre un farmaco che blocca un passaggio a valle della via è risultato meno influenzato fin dall’inizio.
Cosa significa per i pazienti e lo sviluppo di farmaci
Nel complesso, il lavoro dimostra che è chimicamente e strutturalmente fattibile costruire farmaci covalenti per KRAS G12C che afferrino la proteina sia nello stato acceso sia in quello spento, e che questi inibitori a doppio stato possono interrompere la segnalazione più rapidamente rispetto ai farmaci esistenti. Tuttavia, il rapido legame non si è tradotto in un controllo tumorale chiaramente migliore né in una soluzione alla resistenza indotta dai fattori di crescita nei modelli preclinici. Per i pazienti, questo suggerisce che aggiungere semplicemente attività contro la forma attiva di KRAS potrebbe non essere sufficiente; potrebbero essere richieste strategie in combinazione che affrontino anche altri membri della famiglia RAS o nodi di segnalazione a valle. Il nuovo warhead e la mappa strutturale presentati qui ampliano comunque la cassetta degli attrezzi per colpire KRAS e informeranno le future generazioni di terapie oncologiche di precisione.
Citazione: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Parole chiave: KRAS G12C, inibitore covalente, inibizione a doppio stato, segnalazione MAPK, resistenza ai farmaci